Aktivni sastojci: Omalizumab
Xolair 75 mg prašak i otapalo za otopinu za injekciju
Ulošci za paket Xolair dostupni su za veličine pakiranja:- Xolair 75 mg prašak i otapalo za otopinu za injekciju
- Xolair 150 mg prašak i otapalo za otopinu za injekciju
Zašto se koristi Xolair? Čemu služi?
Aktivni sastojak lijeka Xolair je omalizumab. Omalizumab je sintetički protein sličan prirodnim proteinima koje proizvodi tijelo; pripada klasi lijekova koji se zovu monoklonska antitijela.
Koristi se za sprječavanje pogoršanja astme kontroliranjem simptoma teške alergijske astme kod odraslih i adolescenata (12 godina i starijih) i djece (od 6 do manje od 12 godina) koja već primaju lijekove za astmu. nisu dobro kontrolirani lijekovima kao što su inhalacijski steroidi u visokim dozama ili inhalacijski beta-agonisti.
Xolair blokira tvar zvanu imunoglobulin E (IgE), koju proizvodi tijelo. IgE ima ključnu ulogu u izazivanju alergijske astme.
Kontraindikacije Kada se Xolair ne smije koristiti
Ne biste trebali davati Xolair
- ako ste alergični na omalizumab ili neki drugi sastojak ovog lijeka (naveden u dijelu 6).
Ako mislite da ste alergični na neki od sastojaka, obavijestite svog liječnika jer vam se Xolair ne smije davati.
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Xolair
Xolair sadrži protein, a kod nekih ljudi protein može izazvati teške alergijske reakcije.
Znakovi uključuju osip, otežano disanje, oticanje ili osjećaj slabosti. Ako imate alergijsku reakciju nakon uzimanja lijeka Xolair, obratite se liječniku što je prije moguće.
Posebna vrsta alergijske reakcije, nazvana serumska bolest, primijećena je u pacijenata liječenih Xolairom. Simptomi serumske bolesti mogu biti jedan ili više od sljedećih: bol u zglobovima sa ili bez otekline ili ukočenosti, osip, groznica, natečeni limfni čvorovi, bol u mišićima. Ako osjetite bilo koji od ovih simptoma, a osobito ako osjetite kombinaciju ovih simptoma, odmah se obratite svom liječniku.
Churg-Straussov sindrom i eozinofilni sindrom primijećeni su u bolesnika liječenih Xolairom. Simptomi mogu biti jedan ili više od sljedećeg: oticanje, bol ili osip oko krvnih ili limfnih žila, povišena razina određene vrste bijelih krvnih stanica (izražena eozinofilija), pogoršanje problema s disanjem, začepljen nos, srčani problemi, bol, utrnulost , trnci u rukama i nogama. Ako osjetite bilo koji od ovih simptoma, a osobito ako osjetite kombinaciju ovih simptoma, odmah se obratite svom liječniku.
Prije nego što primite Xolair, razgovarajte sa svojim liječnikom:
- ako imate problema s bubrezima ili jetrom
- ako imate poremećaj u kojem vaš imunološki sustav napada dio vašeg tijela (autoimuna bolest)
- ako živite u regijama u kojima su česte infekcije uzrokovane parazitima ili planirate putovati u jednu od ovih regija jer Xolair može smanjiti vašu otpornost na te infekcije.
Xolair ne liječi akutne simptome astme, poput iznenadnog napada astme. Stoga se Xolair ne smije koristiti za liječenje ovih simptoma.
Nemojte koristiti Xolair za sprječavanje ili liječenje drugih poremećaja alergijskog tipa, kao što su iznenadne alergijske reakcije, sindrom hiperimunoglobulina E (nasljedni imunološki poremećaj), aspergiloza (gljivična bolest pluća), alergija na hranu, ekcem ili peludna groznica jer Xolair nije proučavan u ovim uvjetima.
Djeca (mlađa od 6 godina)
Xolair se ne smije davati djeci mlađoj od 6 godina. U ovoj dobnoj skupini nema dovoljno podataka.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak Xolaira
Obavijestite svog liječnika, ljekarnika ili medicinsku sestru ako uzimate, nedavno ste uzimali ili biste mogli uzeti bilo koje druge lijekove.
Ovo je osobito važno ako uzimate:
- lijekove za liječenje infekcije uzrokovane parazitima jer Xolair može smanjiti učinak ovih lijekova,
- inhalacijski kortikosteroidi i drugi lijekovi za alergijsku astmu.
Upozorenja Važno je znati da:
Trudnoća i dojenje
Xolair vam se ne smije davati tijekom trudnoće, osim ako vaš liječnik smatra da je to potrebno.
Ako planirate trudnoću, obavijestite svog liječnika prije početka liječenja lijekom Xolair. Vaš će liječnik razgovarati s vama o prednostima i potencijalnim rizicima uzimanja ovog lijeka tijekom trudnoće.
Ako zatrudnite tijekom uzimanja Xolaira, odmah obavijestite svog liječnika.
Ako dojite, ne smijete dobiti Xolair.
Upravljanje vozilima i strojevima
Nije vjerojatno da će Xolair utjecati na sposobnost upravljanja vozilima i rada sa strojevima.
Doziranje i način uporabe Kako koristiti Xolair: Doziranje
Upute o uporabi Xolaira nalaze se u odjeljku "Informacije za zdravstvene djelatnike".
Vaš će liječnik odrediti koliko vam je Xolaira potrebno i koliko često će vam ga davati. To ovisi o vašoj tjelesnoj težini i rezultatima krvnih pretraga provedenih prije početka liječenja za mjerenje razine IgE u krvi.
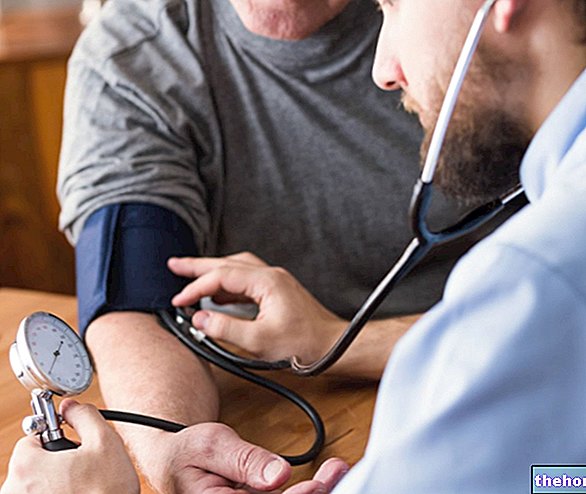
Liječnik ili medicinska sestra daju vam Xolair kao injekciju pod kožu.
Pažljivo slijedite upute svog liječnika ili medicinske sestre.
Administrirani iznos
Dobit ćete 1 do 4 injekcije odjednom, svaka dva tjedna ili svaka četiri tjedna.
Nastavite uzimati trenutne lijekove protiv astme tijekom liječenja lijekom Xolair. Nemojte prestati uzimati lijekove protiv astme bez prethodnog pregleda od svog liječnika.
Možda nećete primijetiti trenutno poboljšanje astme nakon početka terapije Xolairom. Potpuni učinak obično se postiže nakon 12-16 tjedana.
Primjena u djece i adolescenata
Xolair se može koristiti u djece i adolescenata u dobi od 6 godina i starijih koji već uzimaju lijekove za astmu, ali čiji simptomi astme nisu dobro kontrolirani lijekovima poput visokih doza inhalacijskih steroida ili inhalacijskih beta agonista. Liječnik će znati koliko Xolair ima vaše dijete potrebe i koliko će ih često morati uzimati. To će ovisiti o djetetovoj težini i rezultatima krvnih pretraga uzetih prije početka liječenja radi mjerenja količine IgE u djetetovoj krvi.
Ako niste uzeli dozu Xolaira
Kontaktirajte svog liječnika ili bolnicu što je prije moguće kako biste zakazali novi termin.
Ako prestanete uzimati Xolair
Nemojte prestati uzimati Xolair osim ako vam to ne kaže vaš liječnik. Prekid ili prestanak liječenja lijekom Xolair može uzrokovati povratak simptoma astme.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.
Nuspojave Koje su nuspojave Xolaira
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih. Nuspojave uzrokovane lijekom Xolair obično su blage do umjerene, ali povremeno mogu biti ozbiljne.
Ozbiljne nuspojave uključuju:
Rijetke nuspojave (mogu se javiti u do 1 na 1.000 osoba)
- Iznenadne teške alergijske reakcije: ako primijetite iznenadne teške znakove alergije ili kombiniranu pojavu znakova kao što su osip, svrbež ili osip na koži, oticanje lica, usana, jezika, grkljana (glasnica), dušnika ili drugih dijelova tijelo, ubrzan rad srca, omaglica i omaglica, otežano disanje, teško disanje ili otežano disanje ili bilo koji drugi novi simptom, odmah obavijestite svog liječnika ili medicinsku sestru. Ako ste u prošlosti imali teške, nepovezane alergijske reakcije (anafilaksiju) na Xolair, možda imate povećan rizik od razvoja ozbiljne alergijske reakcije nakon uporabe Xolaira.
- Sistemski eritematozni lupus (SLE). Simptomi mogu uključivati bol u mišićima, bol u zglobovima i oticanje te osip. Također se mogu manifestirati i drugi simptomi, poput vrućice, gubitka težine i umora.
Nije poznato (učestalost se ne može procijeniti iz dostupnih podataka)
- Pojava jednog ili više sljedećih simptoma: oticanje, bol ili osip oko krvnih ili limfnih žila, povišena razina određene vrste bijelih krvnih stanica (označena eozinofilija), pogoršanje problema s disanjem, začepljen nos, srčani problemi, bol, utrnulost , trnci u rukama, nogama (znakovi tzv. "Churg-Straussovog sindroma ili hipereozinofilnog sindroma").
- Nizak broj trombocita u krvi sa simptomima kao što su krvarenje ili modrice lakše nego inače.
- Pojava bilo kojeg od sljedećih simptoma, osobito ako je udružena: bol u zglobovima sa ili bez otekline ili ukočenosti, osip, groznica, natečeni limfni čvorovi, bolovi u mišićima (znakovi serumske bolesti).
Ako primijetite bilo koji od ovih simptoma, odmah obavijestite svog liječnika ili medicinsku sestru.
Ostale nuspojave uključuju:
Vrlo česte nuspojave (mogu se javiti u više od 1 na 10 osoba)
- groznica (u djece)
Česte nuspojave (mogu se javiti u do 1 na 10 osoba)
- reakcije na mjestu ubrizgavanja kao što su bol, oteklina, svrbež i crvenilo
- bol u gornjem dijelu trbuha (u djece)
- glavobolja (vrlo česta kod djece)
Manje česte nuspojave (mogu se javiti u do 1 na 100 osoba)
- omaglica, pospanost ili umor
- trnci ili utrnulost u rukama ili stopalima
- nesvjestica, nizak krvni tlak pri sjedenju ili stajanju (posturalna hipotenzija), crvenilo
- grlobolja, kašalj, akutni problemi s disanjem
- mučnina (mučnina), proljev, probavne smetnje
- svrbež, osip, osip, povećana osjetljivost kože na sunce
- debljanje
- simptomi slični gripi
- otečene ruke
Rijetke nuspojave (mogu se javiti u do 1 na 1.000 osoba)
- parazitska infekcija
Nije poznato (učestalost se ne može procijeniti iz dostupnih podataka)
- bolovi u zglobovima, oticanje mišića i zglobova
- gubitak kose
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Nuspojave možete prijaviti i izravno putem nacionalnog sustava za prijavu navedenih u Dodatku V. Nuspojave koje možete pomoći pružiti više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
- Čuvajte ovaj lijek izvan pogleda i dohvata djece.
- Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na naljepnici, jer se rok valjanosti odnosi na zadnji dan tog mjeseca.
- Čuvati u hladnjaku (2 ° C - 8 ° C). Nemojte zamrzavati.
Rok "> Ostale informacije
Što Xolair sadrži
- Aktivni sastojak je omalizumab. Jedna bočica sadrži 75 mg omalizumaba. Nakon rekonstitucije jedna bočica sadrži 125 mg / ml omalizumaba (75 mg u 0,6 ml).
- Pomoćni sastojci su saharoza, L-histidin, L-histidin hidroklorid monohidrat, polisorbat 20.
Kako Xolair izgleda i sadržaj pakiranja
Xolair 75 mg prah i otapalo za otopinu za injekciju isporučuju se u obliku bijelog do gotovo bijelog praha u maloj staklenoj bočici zajedno s bočicom koja sadrži 2 ml vode za injekcije. Prije nego što ga ubrizga liječnik ili medicinska sestra, prašak se rekonstituira u vodi.
Xolair je dostupan u pakiranjima koja sadrže jednu bočicu praška za otopinu za injekciju i jednu ampulu s 2 ml vode za injekcije.
Xolair je također dostupan u bočicama koje sadrže 150 mg omalizumaba.
Rok "> Informacije za zdravstvene djelatnike
Sljedeće informacije namijenjene su samo zdravstvenim djelatnicima:
Liofiliziranom lijeku potrebno je 15-20 minuta da se otopi, iako u nekim slučajevima može potrajati i dulje. Potpuno rekonstituirani lijek izgleda bistro do blago opalescentno, bezbojno do blijedo smeđe-žuto i može imati male mjehuriće ili pjenu oko ruba bočice. Zbog viskoznosti rekonstituiranog lijeka, potrebno je paziti da se sav lijek izvadi iz bočice prije istjerivanja viška zraka ili otopine iz štrcaljke kako bi se dobilo 0,6 ml.
Za pripremu bočica Xolaira 75 mg za potkožnu primjenu slijedite ove upute:
- Iz bočice izvucite 0,9 ml vode za injekcije u štrcaljku opremljenu velikom iglom promjera 18.
- S uspravnom bočicom na ravnoj površini, umetnite iglu i prenesite vodu za injekcije u bočicu koja sadrži liofilizirani prah prema standardnim sterilnim tehnikama, usmjeravajući vodu za injekcije izravno na prah.
- Držeći bočicu uspravno, snažno je okrećite (nemojte tresti) približno 1 minutu kako biste ravnomjerno navlažili prah.
- Kako biste se lakše otopili, nakon dovršetka koraka 3 nježno preokrenite bočicu na 5-10 sekundi, otprilike svakih 5 minuta, kako biste otopili preostale čvrste čestice. Treba napomenuti da u nekim slučajevima može proći i više od 20 minuta da se prah potpuno se otopi. U ovom slučaju ponavljajte korak 4 dok u otopini više ne budu vidljive čestice nalik gelu. Kad se lijek potpuno otopi, u otopini ne bi trebalo biti vidljivih čestica nalik gelu. Mali mjehurići ili pjena oko ruba bočice su uobičajene. Rekonstituirani lijek će izgledati bistro do blago opalescentno, bezbojno do blijedo smeđe žuto. Nemojte koristiti ako postoje čvrste čestice.
- Preokrenite bočicu najmanje 15 sekundi kako bi otopina dospjela do čepa. Novom štrcaljkom od 3 ml, opremljenom velikom iglom promjera 18, umetnite iglu u bočicu okrenutu naopačke. Držeći bočicu naopako, postavite vrh igle na dno otopine u bočici prilikom uvlačenja otopine. štrcaljku. Prije nego izvadite iglu iz bočice, povucite klip do kraja prema kraju cijevi štrcaljke da izvučete svu otopinu iz obrnute bočice.
- Zamijenite iglu promjera 18 s iglom promjera 25 za potkožno ubrizgavanje.
- Izbacite zrak, veće mjehuriće i svu višak otopine kako biste dobili potrebnu otopinu od 0,6 ml. Na vrhu otopine u štrcaljki može ostati tanak sloj malih mjehurića. Budući da je otopina blago viskozna, primjena otopine injekcijom pod kožu može potrajati 5-10 sekundi. Bočica isporučuje 0,6 ml (75 mg) Xolaira.
- Injekcije se daju subkutano u deltoidno područje ruke ili u bedro.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA -
XOLAIR 75 MG PRAH I OTAPALO ZA OTAPANJE KOJE SE NE BRIŽE
02.0 KVALITATIVNI I KOLIČINSKI SASTAV -
Jedna bočica sadrži 75 mg omalizumaba *.
Nakon rekonstitucije jedna bočica sadrži 125 mg / ml omalizumaba (75 mg u 0,6 ml).
* Omalizumab je humanizirano monoklonsko protutijelo proizvedeno tehnologijom rekombinantne DNA u staničnoj liniji jajnika kineskog hrčka (CHO).
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK -
Prašak i otapalo za otopinu za injekcije.
Sivobijeli liofilizirani prah.
04.0 KLINIČKI PODACI -
04.1 Terapeutske indikacije -
Xolair je indiciran u odraslih, adolescenata i djece u dobi od 6 do
Liječenje Xolairom treba razmotriti samo kod pacijenata s poznatom astmom posredovanom IgE (imunoglobulin E) (vidjeti dio 4.2).
Odrasli i adolescenti (12 godina i stariji)
Xolair je indiciran, kao pomoćna terapija, za poboljšanje kontrole astme u bolesnika s teškom perzistentnom alergijskom astmom nego testom kože ili reaktivnošću. in vitro pozitivan na višegodišnji aeroalergen i smanjenu funkciju pluća (dnevni simptomi FEV1 ili noćna buđenja te u bolesnika s dokumentiranim teškim ponovljenim pogoršanjima astme, unatoč dnevnom unosu visokih doza inhalacijskih kortikosteroida, plus dugotrajno djelovanje beta2-agonista udisanjem.
Djeca (od 6 do
Xolair je indiciran, kao pomoćna terapija, za poboljšanje kontrole astme u bolesnika s teškom perzistentnom alergijskom astmom nego testom kože ili reaktivnošću. in vitro pozitivan na višegodišnji aeroalergen i ima česte dnevne simptome ili noćna buđenja te u pacijenata s dokumentiranim ponavljanim teškim egzacerbacijama astme, unatoč dnevnom unosu visokih doza inhalacijskih kortikosteroida, plus dugotrajnog beta2-agonista inhalacijom.
04.2 Doziranje i način primjene -
Liječenje Xolairom trebali bi započeti liječnici s iskustvom u dijagnostici i liječenju teške trajne astme.
Doziranje
Odgovarajuća doza i učestalost primjene Xolaira određuju se početnim razinama IgE (IU / ml), mjerenim prije početka liječenja, i tjelesnom težinom (kg). Prije primjene početne doze, pacijenti bi trebali odrediti svoje razine IgE pomoću bilo kojeg komercijalno dostupnog serumskog testa ukupnog IgE u svrhu određivanja njihove doze. Na temelju ovih određivanja, za svaku primjenu može biti potrebno 75 do 600 mg Xolaira u 1-4 injekcije.
Manje je vjerojatno da će se dobrobiti primijetiti u bolesnika s razinom IgE ispod 76 IU / ml (vidjeti dio 5.1). Prije početka terapije, liječnik mora osigurati da odrasli i adolescenti s razinom IgE ispod 76 IU / ml i djeca (od 6 do in vitro (RAST)) budu višegodišnji alergeni.
Vidi Tablicu 1 za pretvorbu i Tablice 2 i 3 za određivanje doze u odraslih, adolescenata i djece od 6 do
Xolair se ne smije davati pacijentima čija su početna razina IgE ili tjelesna težina u kilogramima izvan granica tablice doza, Xolair se ne smije davati.
Maksimalna preporučena doza je 600 mg omalizumaba svaka dva tjedna.
Tablica 1: Pretvaranje iz doze u broj bočica, broj injekcija i ukupni ubrizgani volumen pri svakoj primjeni
a0,6 ml = maksimalni volumen za ekstrakciju po bočici (Xolair 75 mg).
b1,2 ml = maksimalni volumen za ekstrakciju po bočici (Xolair 150 mg).
ili upotrijebite 0,6 ml iz bočice od 150 mg.
Tablica 2: UPRAVA SVAKA 4 TJEDNA. Doze Xolaira (u miligramima po dozi) koje se daju potkožnom injekcijom svaka 4 tjedna
Tablica 3: UPRAVA SVAKA 2 TJEDNA. Doze Xolaira (u miligramima po dozi) koje se daju potkožnom injekcijom svaka 2 tjedna
Trajanje liječenja, praćenje i prilagodba doze
Xolair je namijenjen dugotrajnom liječenju. Kliničke studije pokazale su da je potrebno najmanje 12-16 tjedana da bi liječenje Xolairom bilo učinkovito. Nakon 16 tjedana od početka terapije lijekom Xolair, liječnik bi trebao pregledati pacijente kako bi provjerio je li liječenje učinkovito prije nego što se daju daljnje injekcije. Odluka o nastavku terapije Xolairom krajem 16. tjedna ili u kasnijim prilikama trebala bi se temeljiti na opažanju značajnog poboljšanja u ukupnoj kontroli astme (vidjeti dio 5.1. Opća procjena učinkovitosti liječnika).
Prekid liječenja lijekom Xolair obično rezultira povratkom na povišene razine slobodnog IgE i povezane simptome. Ukupne razine IgE povišene su tijekom liječenja i ostaju povišene do godinu dana nakon prestanka liječenja. Stoga se ponovno mjerenje razine IgE tijekom liječenja lijekom Xolair ne može koristiti kao vodič za određivanje doze. Određivanje doze nakon "prekida liječenja u trajanju kraćem od jedne godine trebalo bi se temeljiti na serumskim razinama IgE dobivenim u vrijeme određivanja početne doze. Ukupne serumske razine IgE mogu se ponovno izmjeriti radi određivanja doze ako je liječenje Xolairom prekinuto na godinu dana ili više.
Doze treba prilagoditi značajnim promjenama tjelesne težine (vidjeti tablice 2 i 3).
Posebne populacije
Starije osobe (65 godina i starije)
Postoje ograničeni podaci o uporabi Xolaira u bolesnika starijih od 65 godina, ali nema dokaza da starijim pacijentima treba drugačija doza od one kod mlađih odraslih pacijenata.
Oštećena funkcija jetre ili bubrega
Nisu provedena ispitivanja utjecaja oštećenja bubrega ili jetre na farmakokinetiku lijeka Xolair. klirens u omalizumabu dominira retikulo-endotelni sustav (RES), mala je vjerojatnost da će na njega utjecati oštećenje bubrega ili jetre. Iako se ne preporučuje posebna prilagodba doze, Xolair se u ovih bolesnika mora primjenjivati s oprezom (vidjeti dio 4.4).
Pedijatrijska populacija
Sigurnost i djelotvornost Xolaira u djece mlađe od 6 godina nisu utvrđene. Nema dostupnih podataka.
Način primjene
Samo za potkožnu primjenu. Nemojte primjenjivati intravenozno ili intramuskularno.
Injekcije se daju subkutano u deltoidno područje ruke. Alternativno, injekcije se mogu dati u bedro ako postoje razlozi koji onemogućuju primjenu u deltoidnoj regiji.
Postoji ograničeno iskustvo s samostalnom primjenom lijeka Xolair, stoga liječenje treba provoditi samo zdravstveni radnik.
Za upute o rekonstituciji lijeka prije primjene, vidjeti dio 6.6 i odjeljak s podacima za zdravstvene djelatnike u uputama za uporabu.
04.3 Kontraindikacije -
Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1.
04.4 Posebna upozorenja i mjere opreza pri uporabi -
Općenito
Xolair nije indiciran za liječenje akutnih egzacerbacija astme, akutnog bronhospazma ili astme.
Xolair nije ispitivan u bolesnika sa hiperimunoglobulinskim E sindromom ili alergijskom bronhopulmonalnom aspergilozom, niti za sprječavanje anafilaktičkih reakcija, uključujući one uzrokovane alergijom na hranu, atopijskim dermatitisom ili alergijskim rinitisom. Xolair nije indiciran za liječenje ovih stanja.
Terapija Xolairom nije ispitivana u bolesnika s autoimunim bolestima, stanjima posredovanim imunološkim kompleksom ili već postojećom bubrežnom ili jetrenom insuficijencijom (vidjeti dio 4.2). Oprez je u primjeni lijeka Xolair u ovih populacija pacijenata.
Ne preporučuje se naglo prekinuti liječenje sustavnim ili inhalacijskim kortikosteroidima nakon početka terapije Xolairom. Smanjenje doza kortikosteroida trebalo bi biti učinjeno pod izravnim liječničkim nadzorom, a možda će se morati postupno.
Poremećaji imunološkog sustava
Alergijske reakcije tipa I
Lokalne ili sustavne alergijske reakcije tipa I, uključujući anafilaksiju i anafilaktički šok, mogu se pojaviti s omalizumabom, čak i s početkom nakon dugog razdoblja liječenja. Većina se tih reakcija javlja unutar 2 sata od prve i sljedeće injekcije Xolaira, ali neke su se dogodile i nakon 2 sata, pa čak i nakon 24 sata nakon injekcije. Stoga lijekovi za liječenje anafilaktičkih reakcija uvijek trebaju biti dostupni za neposrednu uporabu nakon primjene lijeka Xolair. Pacijente treba upozoriti da su takve reakcije moguće i da je potrebno potražiti hitnu medicinsku pomoć ako se pojave.
Anafilaktičke reakcije bile su rijetke u kliničkim ispitivanjima (vidjeti dio 4.8).
U kliničkim ispitivanjima antitijela na omalizumab otkrivena su u malog broja pacijenata (vidjeti dio 4.8). Klinička važnost anti-Xolair antitijela nije dobro poznata.
Serumska bolest
Serumska bolest i reakcije slične serumskoj bolesti, koje su odgođene alergijske reakcije tipa III, opažene su u pacijenata liječenih humaniziranim monoklonskim protutijelima, uključujući omalizumab. Predloženi patofiziološki mehanizam uključuje stvaranje i taloženje imunoloških kompleksa nakon stvaranja antitijela na omalizumab. obično se javlja 1-5 dana nakon prve ili sljedeće injekcije, čak i nakon dugog liječenja. Simptomi koji ukazuju na serumsku bolest uključuju artritis / artralgiju, osip (urtikarija ili drugi oblici), groznicu i limfadenopatiju Antihistaminici i kortizoni mogu biti od pomoći u sprječavanju ili liječenju ovih poremećaja i bolesnike treba savjetovati da prijave sve sumnjive simptome.
Churg-Straussov sindrom i hipereozinofilni sindrom
Bolesnici s teškom astmom rijetko mogu imati sustavni hipereozinofilni sindrom ili alergijski granulomatozni eozinofilni vaskulitis (Churg-Straussov sindrom), koji se obično liječe sustavnim kortikosteroidima.
U rijetkim slučajevima, pacijenti na lijekovima protiv astme, uključujući omalizumab, mogu imati ili razviti sustavnu eozinofiliju i vaskulitis. Ti su događaji obično povezani sa smanjenjem oralne terapije kortikosteroidima.
Liječnike treba upozoriti da se u takvih pacijenata mogu razviti izražena eozinofilija, vaskulitični osip, pogoršanje plućnih simptoma, abnormalnosti sinusa, srčane komplikacije i / ili neuropatija.
U svim teškim slučajevima s gore navedenim poremećajima imunološkog sustava treba razmotriti prekid primjene omalizumaba.
Parazitske infekcije (helminti)
IgE može biti uključen u imunološki odgovor na neke infekcije helmintima. U bolesnika s kroničnim visokim rizikom od infekcije helmintima, placebom kontrolirano ispitivanje pokazalo je blagi porast stope infekcije omalizumabom, iako tijek, težina i odgovor na liječenje infekcije nisu bili utjecani. Na stopu infekcije to nije utjecalo. cjelokupni klinički program, koji nije osmišljen za otkrivanje takvih infekcija, bio je manji od 1 na 1.000 pacijenata. Međutim, potreban je oprez u pacijenata s visokim rizikom od helmintskih infekcija, osobito na putovanjima u područjima gdje su helmintske infekcije endemske. Ako pacijenti ne reagiraju na preporučeni antihelmintski tretman, potrebno je razmotriti prekid terapije Xolairom.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija -
Budući da IgE može biti uključen u imunološki odgovor na neke infekcije helmintima, Xolair može neizravno smanjiti učinkovitost lijekova u liječenju helmintičkih ili drugih parazitskih infekcija (vidjeti dio 4.4).
Enzimi citokroma P450, efluksne pumpe i mehanizmi vezanja proteina nisu uključeni u klirens omalizumaba; stoga je potencijal interakcije lijek-lijek ograničen. Nisu provedena ispitivanja interakcija lijekova ili cjepiva. Xolair: Nema farmakoloških razloga za očekivanje da uobičajeno propisani lijekovi za astmu djelovat će u interakciji s omalizumabom.
U kliničkim ispitivanjima Xolair se obično koristio u kombinaciji s inhalacijskim i oralnim kortikosteroidima, inhalacijskim beta-agonistima kratkog i dugotrajnog djelovanja, antagonistima leukotriena, teofilinom i oralnim antihistaminicima. Nije bilo naznaka o tome. Promjena sigurnosti Xolaira s ovim drugim uobičajenim koristili lijekove protiv astme. Postoje ograničeni podaci o uporabi Xolaira u kombinaciji sa specifičnom imunoterapijom (terapija s hiposenzibilizacijom). U kliničkom ispitivanju u kojem se Xolair primjenjivao istodobno s imunoterapijom, sigurnost i djelotvornost Xolaira u kombinaciji sa specifičnom imunoterapijom nisu se razlikovali od onih Xolaira. sama.
04.6 Trudnoća i dojenje -
Trudnoća
Postoje ograničeni podaci o uporabi omalizumaba u trudnica. Studije na životinjama ne ukazuju na izravne ili neizravne štetne učinke na reproduktivnu toksičnost (vidjeti dio 5.3). Omalizumab prelazi placentnu barijeru, a potencijalna šteta za fetus nije bila omalizumab povezan sa smanjenjem broja trombocita ovisnih o dobi u primata koji nisu ljudi, s relativno većom osjetljivošću u malodobnih životinja (vidjeti dio 5.3). Xolair se ne smije koristiti tijekom trudnoće osim ako je to nužno potrebno.
Vrijeme za hranjenje
Nije poznato izlučuje li se omalizumab u majčino mlijeko u ljudi. Dostupni podaci o primatima koji ne pripadaju ljudima pokazuju izlučivanje omalizumaba u mlijeko (vidjeti dio 5.3). Ne može se isključiti rizik za novorođenčad / dojenčad. Omalizumab se ne smije primjenjivati tijekom dojenja.
Plodnost
Nema dostupnih podataka o plodnosti omalizumaba u ljudi. U nekliničkim studijama na primatima koji nisu bili ljudi posebno osmišljeni za procjenu učinka na plodnost, uključujući studije parenja, nisu primijećeni učinci na plodnost muškaraca ili žena nakon ponovljene primjene omalizumaba do doza od 75 mg / kg Osim toga, u zasebnim nekliničkim studijama genotoksičnosti nisu uočeni genotoksični učinci (vidjeti dio 5.3).
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima -
Xolair nema ili ima zanemariv utjecaj na sposobnost upravljanja vozilima i rada sa strojevima.
04.8 Nuspojave -
Sažetak sigurnosnog profila
Tijekom kliničkih ispitivanja kod odraslih i adolescenata u dobi od 12 godina i starijih, najčešće prijavljene nuspojave bile su reakcije na mjestu ubrizgavanja, uključujući bol, oteklinu, eritem i pruritus te glavobolju. U kliničkim ispitivanjima u djece od 6 godina do glavobolje, pireksije i bolova u gornjem dijelu trbuha. Većina reakcija bile su blage ili umjerene težine.
Tablica nuspojava
Tablica 4 prikazuje nuspojave zabilježene u kliničkim studijama u ukupnoj sigurnosnoj populaciji liječenoj Xolairom, prema klasifikaciji organskog sustava MedDRA i učestalosti. Unutar svake klase učestalosti, nuspojave su navedene prema padajućoj ozbiljnosti. Učestalosti su definirane kao: vrlo česte (≥1 / 10), česte (≥1 / 100; nakon stavljanja lijeka u promet navedene su nepoznate (učestalost se ne može procijeniti) iz dostupnih podataka).
Tablica 4: Nuspojave
*: vrlo često u djece od 6 do
**: u djece od 6 do
Opis odabranih nuspojava
Poremećaji imunološkog sustava
Za dodatne informacije vidjeti dio 4.4.
Arterijski tromboembolijski događaji (ATE)
U kontroliranim kliničkim ispitivanjima i tijekom privremenih analiza promatračke studije uočena je brojčana neravnoteža arterijskih tromboembolijskih događaja. Definicija složene krajnje točke ATE uključivala je moždani udar, prolazni ishemijski napad, infarkt miokarda, nestabilnu anginu i kardiovaskularnu smrt (uključujući smrt iz nepoznatog uzroka). U konačnoj analizi promatračke studije stopa ATE na 1.000 bolesničkih godina bila je 7, 52 (115 / 15.286 godina pacijenta) za bolesnike liječene Xolairom i 5,12 (51 / 9.963 pacijent godina) za kontrolne bolesnike. U "multivarijantnoj kontrolnoj analizi osnovnih čimbenika kardiovaskularnog rizika, omjer opasnosti bio je 1,32 (interval pouzdanosti 95% 0,91-1,91). U novoj zbirnoj analizi kliničkog ispitivanja koja je uključivala sve u randomizirane dvostruko slijepe, placebom kontrolirane studije koje su trajale 8 tjedana ili dulje, stopa ATE na 1.000 bolesničkih godina iznosila je 2,69 (5 / 1,856 bolesničkih godina) za bolesnike liječene Xolairom i 2,38 (4 /1680 bolesničkih godina) za placebo skupinu (omjer stopa 1,13, 95% interval pouzdanosti 0,24-5,71) .
Trombociti
U kliničkim je ispitivanjima mali broj pacijenata imao broj trombocita ispod donje granice normalnog laboratorijskog raspona. Nijedna od ovih promjena nije bila povezana s epizodama krvarenja ili smanjenim hemoglobinom. Nisu zabilježeni obrasci trajnog smanjenja broja trombocita, poput onog primijećenog kod primata koji nisu ljudi (vidjeti dio 5.3), iako su ljudi (pacijenti stariji od 6 godina) u postmarketinškim opažanjima zabilježeni su izolirani slučajevi idiopatske trombocitopenije, uključujući teške slučajeve.
Parazitske infekcije
U bolesnika s kroničnim visokim rizikom od helmintskih infekcija, placebom kontrolirano ispitivanje pokazalo je blagi brojčani porast stope infekcije u skupini omalizumaba koja nije bila statistički značajna. Tijek, težina i odgovor na liječenje infekcija ostali su nepromijenjeni (vidjeti dio 4.4).
Prijavljivanje sumnji na nuspojave
Izvještavanje o sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijavljuju sve sumnje na nuspojave putem nacionalnog sustava prijavljivanja..
04.9 Predoziranje -
Maksimalna tolerirana doza Xolaira nije utvrđena. Pacijentima su davane pojedinačne intravenozne doze do 4.000 mg bez dokaza o toksičnosti koja ograničava dozu. Najviša kumulativna doza primijenjena pacijentima bila je 44 000 mg u razdoblju od 20 tjedana, a ta doza nije uzrokovala nikakve neočekivane akutne učinke.
Ako se sumnja na predoziranje, bolesnika treba promatrati zbog bilo kakvih abnormalnih znakova ili simptoma. Treba tražiti odgovarajući medicinski tretman.
05.0 FARMAKOLOŠKA SVOJSTVA -
05.1 "Farmakodinamička svojstva -
Farmakoterapijska skupina: drugi lijekovi za sindrome opstruktivnih dišnih putova za sustavnu primjenu, ATC oznaka: R03DX05
Omalizumab je humanizirano monoklonsko protutijelo izvedeno iz rekombinantne DNA koje se selektivno veže na humani imunoglobulin E (IgE). Protutijelo je IgG1 kapa koja sadrži humane potporne regije zajedno s komplementarno određujućim regijama mišjeg protutijela koje se veže na IgE.
Mehanizam djelovanja
Omalizumab se veže za IgE i sprječava vezanje IgE za receptor visokog afiniteta FCεRI, čime se smanjuje količina slobodnog IgE koja može pokrenuti alergijsku kaskadu. U atopičnih osoba liječenje omalizumabom također smanjuje broj FCεRI receptora koji se nalaze na bazofilima.
Farmakodinamički učinci
Puštanje in vitro histamin iz bazofila izoliranih od subjekata liječenih Xolairom smanjen je za približno 90% nakon stimulacije alergenom u usporedbi s vrijednostima prije liječenja.
U kliničkim ispitivanjima razine slobodnog IgE u serumu smanjile su se na dozno ovisan način unutar jednog sata od prve primjene i ostale su stabilne između doza. Godinu dana nakon prestanka doziranja Xolairom, razine IgE vratile su se na razinu prije liječenja, a nakon razdoblja eliminacije lijeka nije primijećen povratni učinak na razinu IgE.
Klinička učinkovitost i sigurnost
Odrasli i adolescenti u dobi ≥12 godina
Učinkovitost i sigurnost lijeka Xolair dokazani su u 28-tjednom dvostruko slijepom, placebom kontroliranom istraživanju (studija 1) u kojem je sudjelovalo 419 pacijenata s teškom alergijskom astmom, u dobi od 12 do 79 godina, koji su imali smanjenu funkciju pluća (predviđeni FEV1 40-80%) i slaba kontrola simptoma astme unatoč liječenju visokim dozama inhalacijskih kortikosteroida i dugotrajnim beta2-agonistom. Pacijenti koji ispunjavaju uvjete imali su višestruka astmatična pogoršanja koja su zahtijevala sistemsko liječenje kortikosteroidima ili su bili hospitalizirani ili su otišli na hitnu pomoć zbog teškog pogoršanja astme u prethodnoj godini, unatoč nastavku liječenja visokim dozama kortikosteroida inhalacijom i s dugotrajnim beta2-agonistom. Potkožni xolair ili placebo davani su kao dodatna terapija> 1000 mikrograma beklometazon dipropionata (ili ekvivalenta) uz dugotrajno djelujući beta2-agonist. Terapije održavanja oralnim kortikosteroidima, teofilinom i antagonistima leukotriena (22%, 27% , odnosno 35% pacijenata).
Učestalost pogoršanja astme koja zahtijeva liječenje relativno visokim dozama sistemskih kortikosteroida bila je primarna krajnja točka. Omalizumab je smanjio učestalost egzacerbacija astme za 19% (p = 0,153). Dodatne procjene koje su pokazale statističku značajnost (p
U analizi podskupina, bolesnici s ukupnim IgE ≥76 IU / mL prije liječenja imali su veću vjerojatnost da će postići klinički značajnu korist uz Xolair. U tih je bolesnika u studiji 1 Xolair smanjio učestalost egzacerbacija astme za 40% (p = 0,002) Osim toga, dodatni pacijenti u populaciji s ukupnim IgE ≥76 IU / mL u programu Xolair u teškoj astmi imali su klinički značajne odgovore. Tablica 5 uključuje rezultate za cijelu populaciju istraživanja 1.
Tablica 5: Rezultati istraživanja 1
* izrazito poboljšanje ili potpuna kontrola
** p-vrijednost za opću raspodjelu procjene
Studija 2 procjenjivala je učinkovitost i sigurnost lijeka Xolair u populaciji od 312 pacijenata s teškom alergijskom astmom koja je odgovarala ispitivanoj populaciji 1. Liječenje lijekom Xolair u ovoj otvorenoj studiji rezultiralo je smanjenjem učestalosti od 61%. Klinički značajna pogoršanja astme u usporedbi s tekućim samo terapija astme.
Četiri dodatne velike placebom kontrolirane potporne studije u trajanju od 28 do 52 tjedna na 1722 odraslih i adolescenata (studije 3, 4, 5, 6) procjenjivale su učinkovitost i sigurnost lijeka Xolair u bolesnika s teškom perzistentnom astmom. Neki bolesnici nisu bili adekvatno kontrolirani, međutim, oni su primali smanjenu istodobnu terapiju astme u usporedbi s bolesnicima u studijama 1 ili 2. Studije 3-5 su koristile egzacerbaciju kao primarnu krajnju točku, dok je studija 6 uglavnom procjenjivala smanjenje inhalacijskih kortikosteroida.
U studijama 3, 4 i 5, pacijenti liječeni Xolairom imali su smanjenje učestalosti pogoršanja astme za 37,5% (p = 0,027), 40,3% (p
U studiji 6, značajno teži bolesnici s alergijskom astmom liječeni Xolairom uspjeli su smanjiti dozu flutikazona na ≤500 mcg / dan bez pogoršanja kontrole astme (60,3%) u usporedbi s placebom (45,8%, p
Kvaliteta života mjerena je pomoću Upitnika o kvaliteti života povezanog sa astmom smreke. Za svih šest studija, došlo je do statistički značajnog poboljšanja u odnosu na početne rezultate u ocjeni kvalitete života pacijenata s Xolairom u usporedbi s placebom ili kontrolnim skupinama.
Opću procjenu učinkovitosti liječenja od strane liječnika:
Opća procjena liječnika provedena je u pet gore navedenih studija, kao opća mjera kontrole astme koju je izrazio liječnik koji je liječio. Liječnik je mogao uzeti u obzir vršni ekspiratorni protok (PEF), dnevne i noćne simptome, upotrebu lijekova za spašavanje , spirometrija i egzacerbacije. U svih pet studija vjerovalo se da je značajno veći udio pacijenata liječenih Xolairom postigao značajno poboljšanje ili potpunu kontrolu astme u odnosu na bolesnike liječene placebom.
Djeca od 6 do
Ključni podaci koji podupiru sigurnost i djelotvornost Xolaira u razdoblju od 6
Studija 7 je placebom kontrolirana studija koja je uključivala specifičnu podskupinu (N = 235) pacijenata kako je definirano u ovoj indikaciji, liječenih visokim dozama inhalacijskih kortikosteroida (≥500 μg / dan flutikazon ili ekvivalent) uz dugotrajno djelovanje beta-agonist.
Klinički značajno pogoršanje definirano je kao pogoršanje simptoma astme u kliničkoj prosudbi istraživača i uključivalo je udvostručavanje od početne doze inhalacijskog kortikosteroida tijekom najmanje 3 dana i / ili ublažavanje lijeka sustavnim kortikosteroidima (oralno ili intravenozno) tijekom najmanje 3 dana.
U specifičnoj podskupini pacijenata koji su primali visoke doze inhalacijskih kortikosteroida, stopa egzacerbacija astme bila je značajno niža u skupini koja je primala omalizumab nego u skupini koja je primala placebo. U 24. tjednu razlika između stope pogoršanja u dvije liječene skupine bila je 34% smanjenje u bolesnika liječenih omalizumabom u usporedbi s placebom (omjer postotaka 0,662, p = 0,047). U drugom 28-tjednom razdoblju dvostruko slijepog liječenja razlika između stopa pogoršanja u dvije liječene skupine bila je smanjenje od 63% za bolesnici liječeni omalizumabom u usporedbi s placebom (omjer postotaka 0,37, str
Tijekom 52. tjedna dvostruko slijepog razdoblja liječenja (koje se sastoji od 24 tjedna liječenja fiksnom dozom steroida i 28 tjedana liječenja promjenjivom dozom steroida) razlika u postocima između tretiranih skupina bila je jedno relativno smanjenje 50% (omjer postotaka 0,504, str
Na kraju 52 tjedna liječenja, skupina omalizumaba pokazala je veće smanjenje korištenja beta-agonista prema potrebi od skupine koja je primala placebo, iako razlika između dvije liječene skupine nije bila statistički značajna. Ukupna procjena učinkovitosti liječenja na kraj 52-tjednog dvostruko slijepog razdoblja liječenja u podskupini teških bolesnika s visokim dozama inhalacijskih kortikosteroida u kombinaciji s dugotrajnim beta-agonistima postotak pacijenata s učinkovitošću liječenja ocijenjenim s "izvrsno" bio je veći, dok je postotak bolesnici s učinkovitošću liječenja ocijenjeni "umjerenim" ili "lošim" bili su niži u skupini liječenoj omalizumabom nego u skupini liječenoj placebom; razlika između dviju skupina bila je statistički značajna (p
05.2 "Farmakokinetička svojstva -
Farmakokinetika omalizumaba proučavana je kod odraslih i adolescenata s alergijskom astmom.
Apsorpcija
Nakon potkožne primjene, omalizumab se apsorbira sa prosječnom apsolutnom bioraspoloživošću od 62%. Nakon supkutane primjene pojedinačne doze u odraslih i adolescenata s astmom, omalizumab se sporo apsorbirao, dostigavši najveće serumske koncentracije nakon prosječno 7-8 dana. Farmakokinetika omalizumaba je linearna u dozama iznad 0,5 mg / kg. Nakon više doza omalizumaba, stacionarna područja ispod krivulje serumska koncentracija-vrijeme od dana 0 do dana 14 bila su do 6 puta veća od onih zabilježenih nakon prve doze.
Primjena Xolaira u tekućim i liofiliziranim pripravcima rezultirala je sličnim koncentracijom-vremenskim profilom omalizumaba u serumu.
Distribucija
In vitro, omalizumab tvori male komplekse s IgE. Nisu uočeni oborinski kompleksi i kompleksi molekulske mase veće od milijun daltona in vitro ili in vivo. Prividni volumen distribucije u pacijenata nakon potkožne primjene bio je 78 ± 32 ml / kg.
Uklanjanje
Očišćenje omalizumaba uključuje procese klirensa IgG -a, kao i klirens putem specifičnog vezanja i kompleksa s njegovim ciljnim ligandom, IgE. Hepatičko uklanjanje IgG -a uključuje razgradnju u retikuloendotelnom sustavu i endotelnim stanicama. Nepromijenjeni IgG izlučuje se i žuči. U bolesnika s astmom, poluvrijeme eliminacije omalizumaba u serumu je u prosjeku 26 dana, sa prosječnim očitim klirensom od 2,4 ± 1,1 ml / kg / dan. Nadalje, udvostručenje tjelesne težine približno je udvostručilo prividni klirens.
Karakteristike u populaciji pacijenata
Dob, rasa / etnička pripadnost, spol, indeks tjelesne mase
Analizirana je populacijska farmakokinetika Xolaira kako bi se procijenili učinci demografskih karakteristika. Analiza ovih ograničenih podataka pokazuje da nije potrebna prilagodba doze na temelju dobi (6-76 godina), rase / etničke pripadnosti, spola ili indeksa tjelesne mase (vidjeti dio 4.2).
Bubrežna i jetrena insuficijencija
Nema farmakokinetičkih ili farmakodinamičkih podataka u bolesnika s oštećenjem bubrega ili jetre (vidjeti dijelove 4.2 i 4.4).
05.3 Pretklinički sigurnosni podaci -
Sigurnost omalizumaba proučavana je na majmunima cynomolgus, jer se omalizumab veže za cynomolgus i humani IgE sa sličnim afinitetom. Protutijela na omalizumab pronađena su kod nekih majmuna nakon ponovljene potkožne ili intravenozne primjene. Međutim, nije primijećena nikakva očita toksičnost, poput bolesti posredovane imunološkim kompleksom ili citotoksičnosti ovisne o komplementu. Anafilaktički odgovor zbog degranulacije mastocita u majmuna cynomolgus.
Kronična primjena omalizumaba do doza od 250 mg / kg (najmanje 14 puta najveća preporučena klinička doza u mg / kg prema tablici s preporučenim dozama) dobro se podnosila kod primata koji nisu ljudi (odrasle i mlade životinje), sa osim smanjenja broja trombocita povezanih s dozom, ovisno o dobi, s većom osjetljivošću na mlade životinje. Koncentracija u serumu potrebna za postizanje smanjenja trombocita za 50% od početne vrijednosti kod odraslih majmuna cynomolgus bila je približno 4 do 20 puta veća od predviđenog maksimuma kliničke koncentracije u serumu Osim toga, kod majmuna cynomolgus primijećena su akutna krvarenja i upale na mjestima ubrizgavanja.
Nisu provedena formalna ispitivanja karcinogenosti s omalizumabom.
U reprodukcijskim studijama na majmunima cynomolgus, potkožne doze do 75 mg / kg tjedno (najmanje 8 puta najveća preporučena klinička doza u mg / kg tijekom razdoblja od 4 tjedna) nisu uzrokovale toksičnost za majku, embriotoksičnost ili teratogenost pri primjeni. tijekom cijelog razdoblja organogeneze i nije izazvao štetne učinke na fetalni ili neonatalni rast kada se primjenjuje tijekom kasne gestacije, poroda i laktacije.
Omalizumb se izlučuje u majčino mlijeko majmuna cynomolgus. Razine omalizumaba otkrivene u mlijeku bile su 0,15% koncentracije u majčinom serumu.
06.0 FARMACEUTSKE INFORMACIJE -
06.1 Pomoćne tvari -
Prah
Saharoza
L-histidin
L-histidin hidroklorid monohidrat
Polisorbat 20
Otapalo
Voda za injekcije
06.2 Inkompatibilnost "-
Ovaj lijek se ne smije miješati s drugim lijekovima osim s onima navedenim u odjeljku 6.6.
06.3 Rok valjanosti "-
4 godine.
Nakon rekonstitucije
Kemijska i fizička stabilnost rekonstituiranog lijeka pokazana je 8 sati na 2 ° C do 8 ° C i 4 sata na 30 ° C.
S mikrobiološkog gledišta, lijek se mora upotrijebiti odmah nakon rekonstitucije. Ako se ne upotrijebi odmah, vrijeme i uvjeti skladištenja prije uporabe odgovornost su korisnika i obično ne bi trebali biti duži od 8 sati na 2 ° C - 8 ° C ili 2 sata na 25 ° C.
06.4 Posebne mjere pri skladištenju -
Čuvati u hladnjaku (2 ° C - 8 ° C).
Nemojte zamrzavati.
Za uvjete skladištenja nakon rekonstitucije, vidjeti dio 6.3.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja -
Bočica u prahu: Bistra, bezbojna, staklena bočica tipa I s gumenim čepom i sivom brtvom koja se otvara.
Bočica s otapalom: Bistra, bezbojna, staklena bočica tipa I koja sadrži 2 ml vode za injekcije.
Karton sadrži jednu bočicu praška za otopinu za injekciju i jednu ampulu vode za injekcije.
06.6 Upute za uporabu i rukovanje -
Liofiliziranom lijeku potrebno je 15-20 minuta da se otopi, iako ponekad može potrajati i dulje. Potpuno rekonstituirani lijek izgleda bistro ili blago neprozirno i može imati male mjehuriće ili pjenu oko ruba bočice. Zbog viskoznosti rekonstituiranog lijeka, potrebno je paziti da se sav proizvod izvuče iz bočice prije nego što se iz štrcaljke izbaci višak zraka ili otopine kako bi se dobilo 0,6 ml.
Za pripremu bočica Xolaira 75 mg za potkožnu primjenu slijedite ove upute:
1. Iz bočice izvucite 0,9 ml vode za injekcije u štrcaljku opremljenu velikom iglom promjera 18.
2. Držeći bočicu uspravno na ravnoj površini, umetnite iglu i prenesite vodu za injekcije u bočicu koja sadrži liofilizirani prah, slijedeći standardne sterilne tehnike, usmjeravajući vodu za injekcije izravno na prah.
3. Držeći bočicu uspravno, više puta snažno preokrenite (ne tresite) približno jednu minutu kako biste ravnomjerno navlažili prah.
4. Kako biste olakšali otapanje, nakon dovršetka koraka 3 nježno preokrenite bočicu 5-10 sekundi, otprilike svakih 5 minuta, kako biste otopili preostale čvrste čestice.
Treba napomenuti da u nekim slučajevima može proći i više od 20 minuta da se prah potpuno otopi. Ako je tako, ponavljajte korak 4 dok u otopini više ne budu vidljive čestice nalik gelu.
Kad se lijek potpuno otopi, u otopini ne bi trebale biti vidljive čestice nalik gelu. Česti su mali mjehurići ili pjena oko ruba bočice. Rekonstituirani lijek bit će bistar ili blago neproziran. Nemojte koristiti ako postoje čvrste čestice.
5. Preokrenite bočicu najmanje 15 sekundi kako bi otopina dospjela do čepa. Novom štrcaljkom od 3 ml, opremljenom velikom iglom promjera 18, umetnite iglu u bočicu okrenutu naopačke. Držeći bočicu naopako, postavite vrh igle na dno otopine u bočici prilikom uvlačenja otopine u bočicu. injekcija. Prije nego uklonite iglu iz bočice, povucite klip do kraja prema kraju cijevi štrcaljke kako biste izvukli svu otopinu iz obrnute bočice.
6. Zamijenite iglu promjera 18 s iglom promjera 25 za potkožno ubrizgavanje.
7. Izbacite zrak, veće mjehuriće i svu višak otopine kako biste dobili potrebnu otopinu od 0,6 ml. Na vrhu otopine u štrcaljki može ostati tanak sloj malih mjehurića. Budući da je otopina blago viskozna, primjena otopine injekcijom pod kožu može potrajati 5-10 sekundi.
Bočica isporučuje 0,6 ml (75 mg) Xolaira.
8. Injekcije se daju subkutano u deltoidnu regiju ruke ili natkoljenice.
Xolair 75 mg prašak za otopinu za injekciju isporučuje se u bočici za jednokratnu upotrebu.
S mikrobiološkog gledišta, lijek se mora upotrijebiti odmah nakon rekonstitucije (vidjeti dio 6.3).
Neiskorišteni lijek i otpad dobiven iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 NOSITELJ "Odobrenja za stavljanje u promet" -
Novartis Europharm Limited
Poslovni park Frimley
Camberley GU16 7SR
UK
08.0 BROJ DOZVOLE ZA PROMET -
EU/1/05/319/001
036892026
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA -
Datum prve autorizacije: 25. listopada 2005
Datum posljednje obnove: 25. listopada 2010
10.0 DATUM REVIZIJE TEKSTA -
D.CCE lipanj 2015










.jpg)