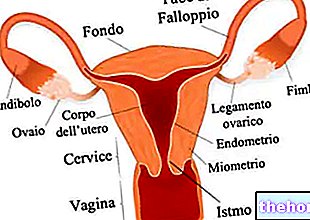
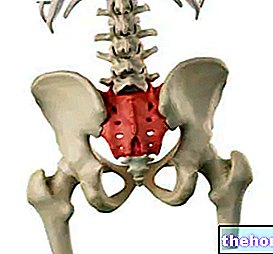
Aktivni sastojci: Docetaksel
TAXOTERE 20 mg / 0,5 ml koncentrata i otapala za otopinu za infuziju
Ulošci za paket Taxotere dostupni su za pakiranja:- TAXOTERE 20 mg / 0,5 ml koncentrata i otapala za otopinu za infuziju
- TAXOTERE 80 mg / 2 ml koncentrata i otapalo za otopinu za infuziju
- TAXOTERE 20 mg / 1 ml koncentrata za otopinu za infuziju
- TAXOTERE 80 mg / 4 ml koncentrat za otopinu za infuziju
- TAXOTERE 160 mg / 8 ml koncentrat za otopinu za infuziju
Zašto se koristi Taxotere? Čemu služi?
Naziv ovog lijeka je TAXOTERE. Naziv aktivnog sastojka je docetaksel.
Docetaksel je tvar dobivena iz igličastih listova biljke tise i pripada skupini lijekova protiv raka koji se zovu taksani.
Vaš liječnik je propisao lijek TAXOTERE za liječenje raka dojke, određenih oblika raka pluća (karcinom malih stanica pluća), raka prostate, raka želuca ili raka glave i vrata:
- Za liječenje uznapredovalog raka dojke, TAXOTERE se može primijeniti sam ili u kombinaciji s doksorubicinom, trastuzumabom ili kapecitabinom.
- Za liječenje ranog raka dojke sa ili bez zahvaćenosti limfnih čvorova, TAXOTERE se može primijeniti u kombinaciji s doksorubicinom i ciklofosfamidom.
- Za liječenje raka pluća, TAXOTERE se može primijeniti sam ili u kombinaciji s cisplatinom.
- za liječenje raka prostate, TAXOTERE se daje u kombinaciji s prednizonom ili prednizolonom.
- za liječenje metastatskog raka želuca, TAXOTERE se primjenjuje u kombinaciji s cisplatinom i 5-fluorouracilom.
- za liječenje raka glave i vrata, TAXOTERE se daje u kombinaciji s cisplatinom i 5-fluorouracilom.
Kontraindikacije Kada se Taxotere ne smije koristiti
Ne smijete uzimati TAXOTERE
- ako ste alergični (preosjetljivi) na docetaksel ili neki drugi sastojak lijeka Taxotere;
- ako vam je broj bijelih krvnih stanica prenizak;
- ako imate teške probleme s jetrom;
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Taxotere
Prije svakog liječenja lijekom TAXOTERE potrebno je provesti krvne pretrage kako bi se utvrdilo ima li dovoljno krvnih stanica i je li jetra dovoljno aktivna.U slučaju promjena u bijelim krvnim zrncima može doći i do povišene temperature ili infekcija.
Obavijestite svog liječnika, bolničkog ljekarnika ili medicinsku sestru ako imate problema s vidom. Ako imate bilo kakvih problema s vidom, osobito zamagljenog vida, trebate odmah pregledati oči i vid.
Ako razvijete akutne plućne probleme ili ako se postojeći simptomi pogoršaju (groznica, otežano disanje ili kašalj), odmah obavijestite svog liječnika, bolničkog ljekarnika ili medicinsku sestru. Vaš liječnik može odmah prekinuti liječenje.
Od vas će se tražiti da jedan dan prije primjene lijeka TAXOTERE poduzmete preventivni tretman oralnim kortikosteroidima, poput deksametazona, a zatim nastavite jedan ili dva dana nakon toga, kako biste smanjili neke nuspojave koje se mogu pojaviti nakon infuzije lijeka TAXOTERE, osobito alergijske reakcije i zadržavanje tekućine (oticanje šaka, stopala, nogu ili debljanje).
Tijekom liječenja možda će vam trebati lijekovi za održavanje krvne slike.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak Taxotera
Obavijestite svog liječnika ili bolničkog ljekarnika ako uzimate ili ste nedavno uzimali bilo koje druge lijekove, uključujući i lijekove koji se prodaju bez recepta. To je zato što TAXOTERE ili drugi lijekovi možda neće djelovati kako se očekivalo, pa ste možda skloniji nuspojavama.
Upozorenja Važno je znati da:
Trudnoća, dojenje i plodnost
Prije uzimanja bilo kojeg lijeka pitajte svog liječnika za savjet.
TAXOTERE se NE smije primjenjivati ako ste trudni, osim ako to nije jasno naznačio vaš liječnik.
Ne smijete zatrudnjeti tijekom liječenja ovim lijekom i tijekom terapije morate koristiti odgovarajuće mjere kontracepcije jer TAXOTERE može biti opasan za dijete. Ako zatrudnite tijekom liječenja, odmah obavijestite svog liječnika. Ne smijete dojiti dok uzimate TAXOTERE.
Ako ste muškarac koji se liječi lijekom TAXOTERE, savjetuje se da se ne razmnožavaju tijekom i do 6 mjeseci nakon liječenja te da se prije tretmana raspitate o skladištenju sperme jer docetaksel može narušiti plodnost muškaraca.
Upravljanje vozilima i strojevima:
Nisu provedena ispitivanja utjecaja na sposobnost upravljanja vozilima i rada sa strojevima.
Doziranje i način uporabe Kako koristiti Taxotere: Doziranje
TAXOTERE će vam dati zdravstveni radnik.
Uobičajena doza:
Doziranje će ovisiti o vašoj težini i općem zdravstvenom stanju. Vaš će liječnik izračunati površinu vašeg tijela u kvadratnim metrima (m2) i odrediti dozu koju ćete morati primiti.
Način i put primjene:
TAXOTERE će vam se dati intravenoznom infuzijom (intravenozna primjena). Infuzija će trajati otprilike 1 sat i odvijat će se u bolnici.
Učestalost primjene:
Infuzija će vam se obično davati svaka 3 tjedna.
Vaš liječnik može promijeniti dozu i učestalost davanja u odnosu na vaše krvne pretrage, opće stanje i vaš odgovor na TAXOTERE. Posebno recite svom liječniku ako imate proljev, bol u ustima, utrnulost, trnce, groznicu i pokažite rezultate krvnih pretraga. Ti će mu podaci omogućiti da odluči je li potrebno smanjenje doze. Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku ili bolničkom ljekarniku.
Nuspojave Koje su nuspojave Taxotera
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih.
Vaš liječnik će o tome razgovarati s vama i objasniti potencijalne rizike i koristi liječenja.
Najčešće prijavljene nuspojave samog lijeka TAXOTERE su: smanjen broj crvenih ili bijelih krvnih stanica, gubitak kose, mučnina, povraćanje, upala u ustima, proljev i umor
Ako vam se TAXOTERE daje u kombinaciji s drugim kemoterapeutskim lijekovima, ozbiljnost nuspojava može se povećati.
Tijekom infuzije u bolnici mogu se pojaviti sljedeće alergijske reakcije (mogu se javiti u više od 1 na 10 osoba):
- ispiranje, reakcije na koži, svrbež
- stezanje u prsima, otežano disanje
- groznica ili zimica
- bol u leđima
- niski pritisak
Mogu se javiti ozbiljnije reakcije.
Bolničko osoblje tijekom liječenja pažljivo će pratiti vaše stanje. Odmah obavijestite bolničko osoblje ako primijetite bilo koji od ovih učinaka.
Dolje navedene nuspojave mogu se pojaviti u vremenu između dvije infuzije TAXOTERE -a, a učestalost može varirati ovisno o kombiniranim lijekovima koje uzimate:
Vrlo često (mogu se javiti u više od 1 na 10 osoba):
- infekcije, smanjeni broj crvenih krvnih stanica (anemija) ili bijelih krvnih stanica (potonje su važne u borbi protiv infekcija) i trombocita
- groznica: u tom slučaju morate odmah obavijestiti svog liječnika
- gore opisane alergijske reakcije
- gubitak apetita (anoreksija)
- nesanica
- osjećaj utrnulosti ili trnci ili bol u zglobovima ili mišićima
- glavobolja
- promijenjen osjećaj okusa
- upala oka ili pojačano suzenje oka
- oticanje uzrokovano nedovoljnom limfnom drenažom
- otežano disanje
- gubitak sluzi iz nosa; upala grla i nosa; kašalj
- krvarenja iz nosa
- upala u ustima
- želučane tegobe uključujući mučninu, povraćanje i proljev, zatvor
- bolovi u trbuhu
- probavne smetnje
- gubitak kose (rast kose se u većini slučajeva vraća u normalu)
- crvenilo i oticanje dlanova ili tabana, što može uzrokovati ljuštenje kože (to se može dogoditi i na rukama, licu ili tijelu)
- promjena boje noktiju, koja se može oguliti
- bolovi u mišićima; bolovi u leđima ili u kostima
- promjene ili izostanak menstruacije
- oticanje šaka, stopala, nogu
- umor ili simptomi gripe
- povećanje ili gubitak tjelesne težine
Česte (mogu se javiti u do 1 na 10 osoba):
- kandidijaza usne šupljine
- dehidracija
- vrtoglavica
- oštećen sluh
- smanjenje krvnog tlaka; nepravilan ili ubrzan rad srca
- zastoj srca
- ezofagitis
- suha usta
- poteškoće ili bol pri gutanju
- hemoragija
- povišeni jetreni enzimi (stoga je potrebna redovita analiza krvi)
Manje često (mogu se javiti u do 1 na 100 osoba):
- nesvjestica
- na koži reakcije kože, flebitis (upala vena) ili oteklina
- upala debelog crijeva, tankog crijeva; crijevna perforacija.
- stvaranje krvnih ugrušaka
Učestalost nije poznata:
- intersticijska bolest pluća (upala pluća koja može uzrokovati kašalj i otežano disanje. Upala pluća može se razviti i kada se liječenje docetakselom daje istodobno s radioterapijom)
- upala pluća (infekcije pluća)
- plućna fibroza (ožiljci i zadebljanje u plućima uzrokuju nedostatak daha)
- zamagljen vid zbog oticanja retine unutar oka (cistoidni makularni edem)
- smanjenje natrija u krvi.
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku, bolničkom ljekarniku ili medicinskoj sestri.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Nuspojave možete prijaviti i izravno putem nacionalnog sustava za prijavljivanje navedenog u Dodatku V *. Prijavljivanjem nuspojava možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece.
Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na kutiji, blisteru i bočici.
Ne čuvati na temperaturi iznad 25 ° C ili ispod 2 ° C.
Čuvajte lijek u originalnom pakiranju kako biste ga zaštitili od izravnog svjetla
Prethodno razrijeđena otopina mora se upotrijebiti odmah nakon pripreme, čak i ako je kemijsko-fizička stabilnost navedene otopine dokazana tijekom 8 sati ako se čuva između + 2 ° C i + 8 ° C ili na sobnoj temperaturi (ispod 25 C) .
Otopinu treba upotrijebiti u roku od 4 sata ako se čuva na sobnoj temperaturi (ispod 25 ° C).
Što bočica TAXOTERE koncentrata sadrži:
Aktivni sastojak je docetaksel (kao trihidrat). Svaki ml otopine docetaksela sadrži 40 mg docetaksela (bezvodnog). Jedna bočica sadrži 20 mg / 0,5 ml docetaksela. Pomoćni sastojci su polisorbat 80 i limunska kiselina.
Što sadrži bočica s otapalom:
13% (w / w) 95% etanola u vodi za injekcije.
Opis izgleda TAXOTERE i sadržaj pakiranja:
TAXOTERE 20 mg / 0,5 ml koncentrat za otopinu za infuziju je bistra, viskozna, žuta do žuto-smeđa otopina.
Svako pakiranje sadrži
- bočica s jednom dozom koncentrata i,
- bočica s jednom dozom otapala
Sljedeće informacije namijenjene su samo zdravstvenim radnicima.
VODIČ ZA PRIPREMU TAKSOTERA 20 mg / 0,5 ml KONCENTRAT ZA OTAPANJE ZA INFUZIJU I POVEZANO OTAPALO ZA TAXOTERE
Važno je da prije pripreme otopine TAXOTERE i otopine TAXOTERE za infuziju pročitate cijeli sadržaj ovog vodiča.
1. FORMULACIJA
TAXOTERE 20 mg / 0,5 ml koncentrat za otopinu za infuziju je bistra, viskozna žuta do žuto-smeđa otopina koja sadrži 40 mg / ml docetaksela (bezvodnog) u polisorbatu 80 i limunskoj kiselini. Otapalo TAXOTERE je 13% (w / w) otopina 95% etanola u vodi za injekcije.
2. PREZENTACIJA
TAXOTERE se isporučuje u bočicama s jednom dozom.
Svako pakiranje sadrži jednu bočicu TAXOTERE -a (20 mg / 0,5 ml) i jednu bočicu odgovarajućeg otapala za TAXOTERE u blister pakiranjima.
Bočice TAXOTERE -a moraju se čuvati na temperaturi od + 2 ° C do + 25 ° C, zaštićene od svjetlosti.
TAXOTERE se ne smije upotrijebiti nakon isteka roka valjanosti navedenog na kutiji, blisteru i bočici.
2.1 Bočice TAXOTERE 20 mg / 0,5 ml:
- Bočica TAXOTERE 20 mg / 0,5 ml, kapaciteta 7 ml, izrađena je od prozirnog stakla sa uklonjivim zelenim čepom.
- Bočica TAXOTERE 20 mg / 0,5 ml sadrži otopinu docetaksela u polisorbatu 80 u koncentraciji od 40 mg / ml.
- Svaka bočica TAXOTERE 20 mg / 0,5 ml sadrži 0,5 ml 40 mg / ml otopine docetaksela u polisorbatu 80 (volumen punjenja: 24,4 mg / 0,61 ml). Ovo predoziranje je utvrđeno tijekom razvoja TAXOTERE -a kako bi se nadoknadio gubitak tekućine tijekom pripreme prethodno razrijeđene otopine (vidi odjeljak 4) zbog pjenjenja, prianjanja na stijenke bočice i 'mrtvog prostora'. Ovo predoziranje osigurava da nakon razrjeđivanja s cijeli sadržaj bočice s otapalom zatvorenog s TAXOTERE -om, minimalni volumen ekstrahirane prethodno razrijeđene otopine je 2 ml, koji sadrži 10 mg / ml docetaksela, što odgovara sadržaju navedenom na naljepnici od 20 mg / 0,5 ml po bočici.
2.2 Otapalo za bočice TAXOTERE 20 mg / 0,5 ml:
- Otapalo za TAXOTERE 20 mg / 0,5 ml nalazi se u prozirnoj staklenoj bočici od 7 ml s prozirnim poklopcem.
- Otapalo za TAXOTERE 20 mg / 0,5 ml sastoji se od 13% (w / w) otopine 95% etanola u vodi za injekcije.
- Svaka bočica s otapalom za TAXOTERE 20 mg / 0,5 ml sadrži 1,98 ml otopine. Ovaj volumen izračunat je na temelju stvarnog volumena bočica TAXOTERE 20 mg / 0,5 ml. Dodavanjem cijelog sadržaja bočice s otapalom sadržaju TAXOTERE 20 mg / 0,5 ml osigurava se dobivanje prethodno razrijeđene otopine od 10 mg / ml docetaksela.
3. PREPORUKE ZA SIGURNO RUKOVANJE
TAXOTERE je antineoplastični lijek i, kao i kod drugih potencijalno otrovnih proizvoda, treba biti oprezan pri rukovanju i pripremi otopina. Preporučuje se uporaba rukavica.
Ako TAXOTERE u koncentriranom, prethodno razrijeđenom obliku ili otopini za infuziju dođe u dodir s kožom, odmah i temeljito operite sapunom i vodom. Ako TAXOTERE u koncentriranom, prethodno razrijeđenom obliku ili u otopini za infuziju dođe u dodir sa sluznicom, odmah i temeljito isperite vodom.
4. PRIPREMA ZA INTRAVENSKU UPRAVU
4.1 Priprema prethodno razrijeđene otopine TAXOTERE -a (10 mg docetaksela / ml)
4.1.1 Ako se bočice čuvaju u hladnjaku, ostavite potreban broj kutija TAXOTERE -a na sobnoj temperaturi (ispod 25 ° C) 5 minuta.
4.1.2 Korištenjem graduirane štrcaljke s iglom, aseptično izvucite cijeli sadržaj bočice s otapalom za TAXOTERE djelomičnim preokretanjem bočice.
4.1.3 Ubrizgati cijeli sadržaj štrcaljke u odgovarajuću bočicu lijeka TAXOTERE
4.1.4 Izvadite štrcaljku i iglu te ručno promiješajte otopinu okretanjem 45 sekundi. Ne tresti.
4.1.5 Ostavite bočicu s prethodno razrijeđenom otopinom da odstoji 5 minuta na sobnoj temperaturi (ispod 25 ° C), a zatim provjerite je li otopina bistra i homogena (pjenjenje je normalno čak i nakon 5 minuta zbog sadržaja polisorbata 80 u tekstu) .
Prethodno razrijeđena otopina sadrži 10 mg / ml docetaksela i mora se upotrijebiti odmah nakon pripreme, čak i ako je kemijsko-fizička stabilnost ove otopine dokazana tijekom 8 sati, ako se čuva na temperaturi od + 2 ° C do + 8 ° C ili pri sobnoj temperaturi temperatura (ispod 25 C).
4.2 Priprema otopine za infuziju
4.2.1 Za dobivanje potrebne doze za pacijente može biti potrebno više bočica s prethodno razrijeđenom otopinom. Na temelju potrebne doze pacijenta u mg, aseptički izvucite odgovarajući volumen prethodno razrijeđene otopine koja sadrži 10 mg / ml docetaksela iz odgovarajućeg broja bočica pomoću stupnjevane štrcaljke s iglom. Na primjer, za dozu od 140 mg docetaksela, potrebno je povući 14 ml prethodno razrijeđene otopine docetaksela.
4.2.2 Ubrizgati potrebni volumen prethodno razrijeđene otopine u vrećicu ili bočicu od 250 ml koja sadrži 5% otopinu glukoze ili 9 mg / ml otopine natrijevog klorida (0,9%) za infuziju. Ako je potrebna doza docetaksela veća od 200 mg, upotrijebite veći volumen otopine za infuziju tako da koncentracija docetaksela ne prelazi 0,74 mg / ml.
4.2.3 Ručno miješajte vrećicu ili bocu uvrnućim pokretom.
4.2.4 TAXOTERE otopinu za infuziju treba upotrijebiti u roku od 4 sata i primijeniti je kao 1 -satnu infuziju, aseptično, na sobnoj temperaturi (ispod 25 C) i u normalnim svjetlosnim uvjetima. Dokument je AIFA učinila dostupnom 27. 05. 2015. 243
4.2.5 Kao i kod svih proizvoda za parenteralnu primjenu, prethodno razrijeđena otopina i infuzijska otopina TAXOTERE -a moraju se prije upotrebe vizualno pregledati, otopine koje sadrže taloge moraju se odbaciti.
5. METODA UKIDANJA
Sve uređaje koji su korišteni za razrjeđivanje ili primjenu TAXOTERE -a treba tretirati u skladu sa standardnim postupcima. Ne bacajte lijekove u kanalizaciju. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
TAXOTERE 20 MG / 0,5 ML
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Svaka bočica s jednom dozom koncentrata TAXOTERE 20 mg / 0,5 ml koja sadrži docetaksel u obliku trihidrata, što odgovara 20 mg docetaksela (bezvodnog). Viskozna otopina sadrži 40 mg / ml docetaksela (bezvodni).
Pomoćna tvar: Svaka bočica s jednom otopinom otapala sadrži 13% (w / w) 95% etanola u vodi za injekcije.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK
Koncentrat i otapalo za otopinu za infuziju.
Koncentrat je bistra, viskozna, žuta do žuto-smeđa otopina.
Otapalo je bezbojna otopina.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Rak dojke:
TAXOTERE u kombinaciji s doksorubicinom i ciklofosfamidom indiciran je za pomoćno liječenje pacijenata sa:
- operativni limfni čvor pozitivan na rak dojke;
- operativni čvor negativan karcinom dojke.
U bolesnica s operativnim čvor-negativnim karcinomom dojke, adjuvantno liječenje treba biti ograničeno na pacijentice koje su kandidati za kemoterapiju prema međunarodnim kriterijima za primarno liječenje raka dojke u ranoj fazi. (vidjeti dio 5.1).
TAXOTERE u kombinaciji s doksorubicinom indiciran je za liječenje pacijenata s lokalno uznapredovalim ili metastatskim rakom dojke koji prije nisu primili citotoksičnu terapiju za ovu bolest.
TAXOTERE kao monoterapija indiciran je za liječenje bolesnica s lokalno uznapredovalim ili metastatskim rakom dojke nakon neuspjeha citotoksične terapije. Prethodna kemoterapija morala je sadržavati antraciklin ili alkilirajuće sredstvo.
TAXOTERE u kombinaciji s trastuzumabom indiciran je za liječenje bolesnica s metastatskim rakom dojke s prekomjernom ekspresijom HER2 i koje prethodno nisu primale kemoterapiju za metastatsku bolest.
TAXOTERE u kombinaciji s kapecitabinom indiciran je za liječenje bolesnica s lokalno uznapredovalim ili metastatskim rakom dojke nakon neuspjeha citotoksične kemoterapije.
Prethodna kemoterapija morala je sadržavati antraciklin. Rak pluća bez malih stanica TAXOTERE je indiciran za liječenje pacijenata s lokalno uznapredovalim ili metastatskim karcinomom malih stanica pluća nakon neuspjeha prethodne kemoterapije.
TAXOTERE je u kombinaciji s cisplatinom indiciran za liječenje pacijenata s neresektabilnim, lokalno uznapredovalim ili metastatskim karcinomom malih stanica pluća koji nisu prethodno primali kemoterapiju za ovo stanje.
Rak prostate:
TAXOTERE u kombinaciji s prednizonom ili prednizolonom indiciran je za liječenje pacijenata s hormonski refraktornim metastatskim karcinomom prostate.
Adenokarcinom želuca:
TAXOTERE u kombinaciji s cisplatinom i 5-fluorouracilom indiciran je za liječenje pacijenata s metastatskim želučanim adenokarcinomom, uključujući adenokarcinom gastroezofagealnog spoja, koji prethodno nisu primali kemoterapiju zbog svoje metastatske bolesti.
Rak glave i vrata:
TAXOTERE u kombinaciji s cisplatinom i 5-fluorouracilom indiciran je za indukcijsko liječenje pacijenata s lokalno uznapredovalim karcinomom pločastih stanica glave i vrata.
04.2 Doziranje i način primjene
Primjena docetaksela treba biti ograničena na odjele specijalizirane za primjenu citotoksičnih terapija, a njegova primjena trebala bi biti pod nadzorom liječnika specijaliziranog za primjenu kemoterapije protiv raka (vidjeti dio 6.6).
Preporučena doza:
Za karcinom dojke, rak pluća bez malih stanica, adenokarcinom želuca i rak glave i vrata, premedikaciju oralnim kortikosteroidom, poput deksametazona 16 mg / dan (npr. 8 mg dva puta dnevno) tijekom 3 dana, počevši 1 dan prije primjene docetaksela (vidjeti dio 4.4) Profilaksa G-CSF-om može se koristiti za smanjenje rizika od hematološke toksičnosti.
Za rak prostate, s obzirom na istodobnu primjenu prednizona ili prednizolona, preporučena premedikacija je oralni deksametazon 8 mg 12 sati, 3 sata i 1 sat prije infuzije docetaksela (vidjeti dio 4.4).
Docetaksel se daje u obliku jednosatne infuzije svaka tri tjedna.
Rak dojke:
Za adjuvantnu terapiju operativnog čvora pozitivnog i čvora negativnog raka dojke, preporučena doza docetaksela je 75 mg / m2 primijenjena 1 sat nakon doksorubicina 50 mg / m2 i ciklofosfamida 500 mg / m2 svaka 3 tjedna tijekom 6 ciklusa. (TAC režim ) (vidi također Prilagodba doze tijekom liječenja).
Za liječenje bolesnica s lokalno uznapredovalim ili metastatskim rakom dojke, preporučena doza monoterapije docetakselom je 100 mg / m2. U liječenju prve linije, docetaksel 75 mg / m2 primjenjuje se u kombinaciji s doksorubicinom (50 mg / m2).
U kombinaciji s trastuzumabom preporučena doza docetaksela je 100 mg / m2 svaka 3 tjedna, pri čemu se trastuzumab primjenjuje tjedno.U ključnoj studiji početna infuzija docetaksela započela je dan nakon prve primjene trastuzumaba, a sljedeće doze docetaksela primijenjene su neposredno nakon infuzije trastuzumaba ako se prethodna doza trastuzumaba dobro podnosila. Za dozu i primjenu trastuzumaba pogledajte sažetak opisa svojstava trastuzumaba.
U kombinaciji s kapecitabinom preporučena doza docetaksela je 75 mg / m2 svaka tri tjedna, u kombinaciji s kapecitabinom u dozi od 1250 mg / m2 dva puta dnevno (unutar 30 minuta nakon obroka) tijekom 2 tjedna, nakon čega slijedi interval od 1 tjedna . Za izračun doze kapecitabina prema površini tijela pogledajte sažetak karakteristika lijeka kapecitabina.
Rak pluća bez malih stanica:
U pacijenata koji nikada nisu primali kemoterapiju za karcinom pluća bez malih stanica, preporučena doza je docetaksel 75 mg / m2, nakon čega slijedi odmah cisplatin 75 mg / m2 tijekom 30-60 minuta. Za liječenje nakon neuspjeha prethodne kemoterapije koja sadrži platinu, preporučena doza je 75 mg / m2 kao monoterapija.
Rak prostate:
Preporučena doza docetaksela je 75 mg / m2. Za vrijeme liječenja primjenjuje se prednizon ili prednizolon 5 mg oralno dva puta dnevno (vidjeti dio 5.1).
Adenokarcinom želuca:
Preporučena doza docetaksela je 75 mg / m2 u obliku jednosatne infuzije, nakon čega slijedi 75 mg / m2 cisplatina, u obliku infuzije u trajanju od 1 do 3 sata (oba samo 1. dan), nakon čega slijedi 5-fluorouracil 750 mg. / M2 po dan koji se daje kao kontinuirana 24-satna infuzija tijekom 5 dana, počevši od završetka infuzije cisplatina. Liječenje se ponavlja svaka tri tjedna. Pacijenti bi trebali primiti premedikaciju s antiemeticima i odgovarajuću hidrataciju za primjenu. cisplatina.
Za ublažavanje rizika od hematološke toksičnosti treba koristiti profilaksu G-CSF-om (vidi također Prilagodba doze tijekom liječenja).
Rak glave i vrata:
Pacijenti bi trebali primati antiemetike prije liječenja i odgovarajuću hidrataciju (prije i nakon primjene cisplatina). Profilaksa G-CSF-a može se provesti na način da se umanji rizik od hematološke toksičnosti. Svi pacijenti liječeni docetakselom u studijama TAX 323 i TAX 324 primili su profilaksa antibioticima.
Indukcijska kemoterapija nakon koje slijedi radioterapija (TAX 323):
Za indukcijsko liječenje pacijenata s lokalno uznapredovalim neresektabilnim karcinomom pločastih stanica glave i vrata (SCCHN), preporučena doza docetaksela je 75 mg / m2 u obliku jednosatne infuzije, nakon čega slijedi 75 mg / m2 cisplatina tijekom više od 1 sata, nakon 1. dan, nakon čega slijedi 5-fluorouracil 750 mg / m2 dnevno primijenjen kao kontinuirana 24-satna infuzija tijekom 5 dana. Ovaj raspored doziranja primjenjuje se svaka 3 tjedna kroz 4 ciklusa. Nakon kemoterapije, pacijenti moraju primiti radioterapiju.
Indukcijska kemoterapija nakon koje slijedi kemoradioterapija (TAX 324):
Za indukcijsko liječenje pacijenata s lokalno uznapredovalim karcinomom pločastih stanica glave i vrata (SCCHN) (tehnički neoperabilan, s malom vjerojatnošću kirurškog uspjeha i s ciljem očuvanja organa) preporučena doza docetaksela je 75 mg / m2 kao 1 -satna infuzija prvog dana, nakon čega slijedi 100 mg / m2 cisplatina primijenjenog kao infuzija u trajanju od 30 minuta do tri sata, nakon čega slijedi 5 -fluorouracil 1000 mg / m2 dnevno, primijenjen u kontinuiranoj infuziji od 1 - 4 dana. Ovaj raspored doziranja daje se svaka tri tjedna kroz tri ciklusa. Nakon kemoterapije, pacijenti bi trebali primati kemoradioterapiju.
Za izmjene doze 5-fluorouracila i cisplatina vidjeti specifični Sažetak opisa svojstava lijeka. Prilagodba doze tijekom liječenja:
Općenito
Docetaksel treba primijeniti kada je broj neutrofila 3 1500 stanica / mm3.
U bolesnika koji su doživjeli febrilnu neutropeniju, neutrofilnu tešku perifernu neuropatiju tijekom terapije docetakselom, dozu docetaksela treba smanjiti sa 100 mg / m2 na 75 mg / m2 i / ili sa 75 na 60 mg / m2. Ako pacijent, pri 60 mg / m2, nastavi osjećati te reakcije, liječenje treba prekinuti.
Pomoćna terapija za rak dojke:
Primarnu profilaksu G-CSF-a treba razmotriti kod pacijenata koji primaju adjuvantnu terapiju docetakselom, doksorubicinom i ciklofosfamidom (TAC) za karcinom dojke. U pacijenata s febrilnom neutropenijom i / ili neutropeničnom infekcijom dozu docetaksela treba smanjiti na 60 mg / m2 u svim sljedećim tijekovima (vidjeti dijelove 4.4 i 4.8). U pacijenata sa stomatitisom 3. ili 4. stupnja dozu treba smanjiti na 60 mg / m2
U suradnji s cisplatinom:
Za pacijente koji su u početku liječeni docetakselom 75 mg / m2 u kombinaciji s cisplatinom i čiji je broj trombocita bio niži u prethodnom tijeku terapije
U kombinaciji s kapecitabinom:
Za prilagodbu doze kapecitabina pogledajte Sažetak opisa svojstava lijeka za kapecitabin.
U bolesnika kod kojih se pojavi prva pojava toksičnosti 2. stupnja koja traje u vrijeme sljedeće primjene docetaksela / kapecitabina, liječenje treba odgoditi do povlačenja na stupanj 0-1, a zatim nastaviti sa 100% početne doze.
U pacijenata koji razviju drugu pojavu toksičnosti 2. stupnja ili prvu pojavu toksičnosti 3. stupnja u bilo kojem trenutku tijekom terapije, liječenje treba odgoditi do povlačenja na stupanj 0-1, a zatim nastaviti s docetakselom 55 mg / m2 .
Za svaku naknadnu pojavu toksičnosti ili za bilo koju toksičnost stupnja 4, prekinite terapiju docetakselom.
Za izmjene doze trastuzumaba pogledajte Sažetak opisa svojstava trastuzumaba.
U suradnji s cisplatinom i 5-fluorouracilom:
Ako se unatoč upotrebi G-CSF-a pojavi epizoda febrilne neutropenije, produljene neutropenije ili neutropenije infekcije, dozu docetaksela treba smanjiti sa 75 na 60 mg / m2. Ako se jave daljnje epizode komplicirane neutropenije, dozu docetaksela treba smanjiti do 45 mg / m2. Za trombocitopeniju 4. stupnja dozu docetaksela treba smanjiti sa 75 na 60 mg / m2. Pacijente se ne smije ponovno liječiti daljnjim tijekovima docetaksela dok se neutrofili ne vrate na razinu> 1.500 stanica / mm3 i dok se trombociti ne vrate do razine> 100.000 stanica / mm3. Prekinite liječenje ako te toksičnosti potraju (vidjeti dio 4.4). Preporučene izmjene doze zbog toksičnosti u bolesnika liječenih docetakselom u kombinaciji s cisplatinom i 5-fluorouracilom (5-FU):
Za izmjene doze cisplatina i 5-fluorouracila pogledajte poseban Sažetak opisa svojstava lijeka.
U ključnoj SCCHN studiji kod pacijenata koji su doživjeli kompliciranu neutropeniju (uključujući produljenu neutropeniju, febrilnu neutropeniju ili infekciju), predloženo je da se upotrebom GCSF-a osigura profilaktička pokrivenost (npr., 6-15. Dan) u svim sljedećim ciklusima.
Posebne populacije:
Bolesnici s jetrenom insuficijencijom:
Na temelju farmakokinetičkih podataka s docetakselom u dozi od 100 mg / m2 koji se daje kao jednokratno liječenje, u bolesnika s povišenjem transaminaza (ALT i / ili AST) većim od 1,5 puta gornje granice normalne i alkalne fosfataze veće od 2,5 puta gornje granice normale , preporučena doza docetaksela je 75 mg / m2 (vidjeti dijelove 4.4 i 5.2). Za bolesnike s bilirubinom u serumu iznad gornje granice normale i / ili ALT i AST> 3,5 puta gornjom granicom normale povezane s alkalnom fosfatazom većom od 6 puta gornjom granicom normale, ne može se preporučiti smanjenje doze, a docetaksel neće mora se primijeniti osim u slučajevima kada je to strogo naznačeno.
U kombinaciji s cisplatinom i 5-fluorouracilom za liječenje pacijenata s adenokarcinomom želuca, ključna klinička studija isključila je bolesnike s ALT i / ili AST> 1,5 puta gornjom granicom normale povezane s vrijednošću alkalne fosfataze.> 2,5 puta gornjom granicom normalne i pri vrijednosti bilirubina> 1 puta gornjoj granici normale; za te se bolesnike ne može preporučiti smanjenje doze i docetaksel se ne smije koristiti osim ako je to strogo indicirano. Nema podataka o bolesnicima s oštećenjem jetre koji su liječeni docetakselom u kombinaciji s drugim indikacijama.
Pedijatrijska populacija:
Sigurnost i djelotvornost lijeka TAXOTERE kod raka nazofarinksa u djece u dobi od 1 mjeseca do manje od 18 godina nisu utvrđene.
Nema podataka o upotrebi TAXOTERE-a u pedijatrijskoj populaciji za indikacije raka dojke, raka malih stanica pluća, raka prostate, raka želuca te raka glave i vrata, isključujući manje diferencirani karcinom tipa II i III nazofarinksa.
Umirovljenici.
Na temelju populacijske farmakokinetike, nema posebnih uputa za uporabu u starijih osoba.
U kombinaciji s kapecitabinom u bolesnika starijih od 60 godina i starijih, preporučuje se smanjenje početne doze na 75% (vidjeti Sažetak opisa svojstava lijeka za kapecitabin).
04.3 Kontraindikacije
Preosjetljivost na djelatnu tvar ili bilo koju pomoćnu tvar.
Docetaksel se ne smije primjenjivati u bolesnika s početnim brojem neutrofila
Docetaksel se ne smije primjenjivati u bolesnika s teškim oštećenjem jetre zbog nedostatka dostupnih podataka (vidjeti dijelove 4.2 i 4.4).
Kontraindikacije za druge lijekove vrijede i kada se koriste u kombinaciji s docetakselom.
04.4 Posebna upozorenja i mjere opreza pri uporabi
Osim ako nije kontraindicirano, premedikacija oralnim kortikosteroidima, poput deksametazona 16 mg dnevno (npr. 8 mg dva puta dnevno) tijekom 3 dana, počevši dan prije primjene docetaksela, tijekom 3 dana, počevši dan prije primjene docetaksela za karcinom dojke i nedrobnostanične karcinome pluća, može smanjiti "učestalost i težinu zadržavanja tekućine, kao i ozbiljnost reakcija preosjetljivosti. Za rak prostate, premedikacija je oralni deksametazon 8 mg, 12 sati, 3 sata i 1 sat prije infuzije docetaksela (vidjeti odlomak 4.2).
Hematologija:
Neutropenija je najčešća nuspojava primijećena s docetakselom. Nadiri neutrofila pojavili su se nakon 7 dana (srednja vrijednost), ali se u pacijenata koji su bili prethodno liječeni ovaj interval može skratiti. U svih pacijenata koji primaju docetaksel potrebno je često provoditi potpunu kontrolu krvne slike. Pacijente se ne smije ponovno liječiti docetakselom dok se vrijednost neutrofila ne vrati na 3 1.500 stanica / mm3 (vidjeti dio 4.2).
U slučaju teške neutropenije (
U bolesnika liječenih docetakselom u kombinaciji s cisplatinom i 5-fluorouracilom (TCF), febrilna neutropenija i neutropenična infekcija dogodile su se s manjom učestalošću kad su bolesnici primali profilaktički G-CSF. Pacijenti liječeni TCF-om trebali bi primiti G-CSF kao profilaksu za umanjivanje rizika od komplicirane neutropenije (febrilna neutropenija, produljena neutropenija ili neutropenična infekcija). Bolesnike koji primaju TCF potrebno je pomno pratiti (vidjeti dijelove 4.2 i 4.8).
U bolesnika liječenih docetakselom u kombinaciji s doksorubicinom i ciklofosfamidom (TAC režim), febrilna neutropenija i / ili neutropenična infekcija dogodila se s "manjom učestalošću kad su pacijenti primali primarnu profilaksu G-CSF. Primarnu profilaksu G-CSF-a treba razmotriti u CSF-a. primati adjuvantnu CT terapiju za rak dojke kako bi se umanjio rizik od komplicirane neutropenije (febrilna neutropenija, produljena neutropenija ili neutropenična infekcija). Pacijentice koje se podvrgavaju CT pretrazi moraju se pomno pratiti (vidjeti dijelove 4.2 i 4.8).
Reakcije preosjetljivosti:
Bolesnike treba pomno pratiti radi moguće pojave reakcija preosjetljivosti, osobito tijekom prve i druge infuzije. Reakcije preosjetljivosti mogu se pojaviti unutar nekoliko minuta od početka infuzije docetaksela, stoga bi trebala biti dostupna sredstva za liječenje hipotenzije i bronhospazma. Ako se jave reakcije preosjetljivosti s manjim simptomima, poput ispiranja ili lokalizirane kožne reakcije, nije potrebno prekinuti terapiju. Međutim, teške reakcije, poput teške hipotenzije, bronhospazma ili generaliziranog osipa / eritema, zahtijevaju hitan prekid infuzije docetaksela i odgovarajuće liječenje. Pacijenti koji imaju teške reakcije preosjetljivosti ne smiju više uzimati docetaksel.
Reakcije na koži:
Uočeni su lokalizirani eritemi kože u ekstremitetima (dlan i potplat) s edemom praćenim deskvamacijom. Prijavljeni su teški simptomi poput osipa praćenog ljuštenjem koji dovodi do privremenog ili trajnog prekida liječenja docetakselom (vidjeti dio 4.2).
Zadrzavanje tekucine:
Pacijente s teškim zadržavanjem tekućine, poput pleuralnog, perikardijalnog i ascitesnog izljeva, treba pomno pratiti.
Bolesnici s disfunkcijom jetre:
U bolesnika liječenih docetakselom u dozi od 100 mg / m2 koji se primjenjuju sami i čija je razina transaminaze u serumu (ALT i / ili AST) veća od 1,5 puta gornja granica norme istodobno s razinama alkalne fosfataze u serumu većom od 2,5 puta gornjoj granici normale, c "veći je rizik od razvoja ozbiljnih nuspojava, poput toksične smrti, uključujući gastrointestinalnu sepsu i krvarenje koje može biti fatalno, febrilnu neutropeniju, infekcije, trombocitopeniju, stomatitis i asteniju. Stoga je u bolesnika s visokim testovima jetre preporučena doza docetaksela Prije početka liječenja i prije svakog ciklusa potrebno je provesti 75 mg / m2 i ispitivanje funkcije jetre (vidjeti dio 4.2).
U pacijenata koji imaju vrijednosti bilirubina u serumu veće od gornje granice normale i / ili vrijednosti ALT i AST veće od 3,5 puta gornje granice normale s alkalnom fosfatazom većom od 6 puta gornje granice normale, smanjenje doze ne može se preporučiti, a docetaksel se ne smije koristiti osim ako je strogo naznačeno.
U kombinaciji s cisplatinom i 5-fluorouracilom za liječenje pacijenata s adenokarcinomom želuca, ključna klinička studija isključila je bolesnike s ALT i / ili AST> 1,5 puta gornjom granicom normale povezane s vrijednošću alkalne fosfataze.> 2,5 puta gornjom granicom normalne i pri vrijednosti bilirubina> 1 puta gornjoj granici normale; za te se bolesnike ne može preporučiti smanjenje doze i docetaksel se ne smije koristiti osim ako je to strogo indicirano. Nema podataka o bolesnicima s oštećenjem jetre liječenima u kombinaciji s docetakselom u drugim indikacijama.
Pacijenti s oštećenom funkcijom bubrega:
Nema dostupnih podataka o bolesnicima s teškim oštećenjem bubrega koji primaju terapiju docetakselom.
Živčani sustav:
Pojava teške periferne neurotoksičnosti zahtijeva smanjenje doze (vidjeti dio 4.2).
Srčana toksičnost:
U bolesnika liječenih docetakselom u kombinaciji s trastuzumabom, osobito nakon kemoterapije koja sadrži antracikline (doksorubicin ili epirubicin), primijećeno je zatajenje srca.
Utvrđeno je da je to umjereno do teško i povezano je sa smrću (vidjeti dio 4.8).
Kad su pacijenti kandidati za docetaksel u kombinaciji kontrastuzumaba, trebali bi proći osnovnu srčanu procjenu. Tijekom liječenja (npr. Svaka tri mjeseca) potrebno je dodatno pratiti rad srca kako bi se identificirali pacijenti kod kojih se mogu razviti srčane abnormalnosti. Za više pojedinosti pogledajte sažetak opisa svojstava trastuzumaba.
Ostalo:
Tijekom liječenja i muškaraca i žena i muškaraca treba koristiti mjere kontracepcije najmanje šest mjeseci nakon prestanka liječenja (vidjeti dio 4.6).
Dodatne mjere opreza za adjuvantno liječenje raka dojke
Komplicirana neutropenija:
U bolesnika s kompliciranom neutropenijom (produljena neutropenija, febrilna neutropenija ili infekcija) potrebno je razmotriti terapiju G-CSF-om i smanjenje doze (vidjeti dio 4.2).
Gastrointestinalni štetni događaji:
Simptomi kao što su bol u trbuhu i malaksalost, groznica, proljev sa ili bez neutropenije, mogu biti rane manifestacije teške gastrointestinalne toksičnosti i treba ih odmah procijeniti i liječiti.
Kongestivno zatajenje srca:
Bolesnike je potrebno pratiti zbog simptoma koji mogu dovesti do kongestivnog zatajenja srca tijekom terapije i razdoblja praćenja.
Leukemija:
U bolesnika liječenih docetakselom, doksorubicinom i ciklofosfamidom (TAC) rizik od odgođene mijelodisplazije ili mijeloične leukemije zahtijeva hematološko praćenje.
Pacijenti s 4 ili više pozitivnih limfnih čvorova:
Omjer koristi i rizika CT terapije u bolesnika s 4 ili više pozitivnih limfnih čvorova nije u potpunosti utvrđen privremenom analizom (vidjeti dio 5.1).
Umirovljenici:
Dostupni su ograničeni podaci o bolesnicima starijim od 70 godina koji su liječeni docetakselom u kombinaciji s doksorubicinom i ciklofosfamidom.
U studiji raka prostate na 333 bolesnika liječena docetakselom svaka tri tjedna, 209 je bilo u dobi od 65 godina ili starijih i 68 pacijenata starijih od 75 godina. U bolesnika liječenih docetakselom svaka tri tjedna, učestalost promjena ploča noktiju povezanih s lijekovima, u bolesnika starijih od 65 godina bili su više od 10% veći nego u mlađih bolesnika. Učestalost groznice povezane s lijekovima, proljeva, anoreksije i perifernog edema u pacijenata starijih od 75 godina bila je više od 10% veća nego u bolesnika mlađih od 65 godina.
Među 300 pacijenata (221 u studiji faze III i 79 u studiji faze II) liječenih docetakselom u kombinaciji s cisplatinom i 5-fluorouracilom u studiji raka želuca, 74 su imala 65 ili više godina, a 4 su bila 75 ili starija. Učestalost ozbiljnih nuspojava bila je veća u starijih osoba u odnosu na mlađe bolesnike.Učestalost nuspojava bila je veća u starijih nego u mladih bolesnika. Incidencija sljedećih nuspojava (svih stupnjeva): letargija, stomatitis i neutropenična infekcija dogodila se s učestalošću> 10% u bolesnika starijih od 65 godina u usporedbi s mlađim bolesnicima. Starije bolesnike liječene TCF -om potrebno je pažljivo pratiti.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
In vitro studije pokazale su da se metabolizam docetaksela može promijeniti istovremenom primjenom spojeva koji induciraju ili inhibiraju citokrom P450-3A ili koji se metaboliziraju (pa stoga mogu konkurentno inhibirati enzim), poput ciklosporina, terfenadina, ketokonazola , eritromicin i troleandomicin Stoga je potreban oprez pri istodobnoj terapiji pacijenata s takvim lijekovima zbog potencijalnog rizika od važnih interakcija.
Docetaksel se jako veže za proteine (> 95%). Iako moguća in vivo interakcija između docetaksela i istodobnih terapija nije posebno ispitana, in vitro interakcije između blisko vezanih lijekova, poput eritromicina, difenhidramina, propranolola, propafenona, fenitoina, salicilata, sulfametoksazola i natrijevog valproata nisu utjecali na vezanje docetaksela u proteine. Nadalje, deksametazon ne mijenja vezanje docetaksela na proteine. Docetaksel ne utječe na vezanje digitoksina. Farmakokinetika docetaksela, doksorubicina i ciklofosfamida nije utjecala na njihovu istodobnu primjenu. Čini se da ograničeni podaci iz jedne nekontrolirane studije ukazuju na interakciju između docetaksela i karboplatina. Kada se koristi u kombinaciji s docetakselom, klirens karboplatina bio je približno 50% veći od prethodno navedenih vrijednosti za samo primjenu.
Farmakokinetika docetaksela u prisutnosti prednizona proučavana je u bolesnika s metastatskim rakom prostate. Docetaksel se metabolizira pomoću CYP3A4, a prednizon izaziva indukciju CYP3A4. Nije uočen statistički značajan učinak prednizona na farmakokinetiku docetaksela.
Docetaksel treba davati s oprezom pacijentima koji istodobno uzimaju snažan inhibitor CYP3A4 (npr. Inhibitori proteaze poput ritonavira, azolnih antimikotika poput ketokonazola ili itrakonazola). Studija interakcije lijekova provedena kod pacijenata koji su uzimali ketokonazol i docetaksel pokazala je da je klirens docetaksela smanjen za polovicu zbog ketokonazola, vjerojatno zato što metabolizam docetaksela uključuje CYP3A4 kao dominantni metabolički put.Može doći do oslabljene tolerancije na docetaksel, čak i pri malim dozama.
04.6 Trudnoća i dojenje
Nema podataka o uporabi docetaksela u trudnica. U studijama na štakorima i zečevima docetaksel je embriotoksičan i fetotoksičan te smanjuje plodnost u štakora. Kao i drugi citotoksični lijekovi, docetaksel može uzrokovati oštećenje ploda kada se daje trudnicama. razlog zašto se docetaksel ne smije davati trudnicama osim ako je jasno naznačeno.
Žene u reproduktivnoj dobi / kontracepcija:
Žene reproduktivne dobi koje se liječe docetakselom trebaju se savjetovati da izbjegnu rizik od trudnoće i da odmah obavijeste svog liječnika ako se to dogodi.
Tijekom liječenja treba koristiti učinkovitu metodu kontracepcije.
U nekliničkim studijama, docetaksel ima genotoksične učinke i može umanjiti plodnost muškaraca (vidjeti dio 5.3). Stoga se muškarcima koji se liječe docetakselom preporučuje da se ne razmnožavaju tijekom i do 6 mjeseci nakon liječenja te da se raspitaju o skladištenju sperme prije liječenja.
Vrijeme za hranjenje:
Docetaksel je lipofilna tvar, ali nije poznato izlučuje li se u majčino mlijeko. Slijedom toga, s obzirom na mogućnost nuspojava u dojenčeta, dojenje treba prekinuti tijekom liječenja docetakselom.
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Nisu provedena ispitivanja utjecaja na sposobnost upravljanja vozilima i rada sa strojevima.
04.8 Nuspojave
Nuspojave za koje se smatralo da su vjerojatno ili su vjerojatno povezane s primjenom docetaksela dobivene su u:
1312 i 121 pacijent koji su primali docetaksel 100 mg / m2, odnosno 75 mg / m2 kao monoterapiju.
258 pacijenata koji su primali docetaksel u kombinaciji s doksorubicinom.
406 pacijenata koji su primali docetaksel u kombinaciji s cisplatinom.
92 pacijenta liječena docetakselom u kombinaciji s trastuzumabom.
255 pacijenata koji su primali docetaksel u kombinaciji s kapecitabinom.
332 pacijenta koji su primali docetaksel u kombinaciji s prednizonom ili prednizolonom (prikazani su klinički relevantni nuspojave povezane s liječenjem).
1276 pacijenata (744 i 532 u TAX 316 odnosno GEICAM 9805) koji su primali docetaksel u kombinaciji s doksorubicinom i ciklofosfamidom (prikazani su klinički relevantni nuspojave povezane s liječenjem).
300 pacijenata s adenokarcinomom želuca (221 u studiji faze III i 79 u studiji faze II) liječenih docetakselom u kombinaciji s cisplatinom i 5-fluorouracilom (pojavili su se klinički važni nuspojave povezane s liječenjem).
174 bolesnika s rakom glave i vrata liječenih docetakselom u kombinaciji s cisplatinom i 5-fluorouracilom (pojavile su se klinički važne nuspojave povezane s liječenjem).
Ove su reakcije opisane s NCI zajedničkim kriterijima toksičnosti (stupanj 3 = G3; stupanj 3- -4 = G3 / 4; stupanj 4 = G4) i s izrazima COSTART i MedDRA. Učestalosti su definirane kao:
vrlo često (≥ 1/10); česte (≥ 1/100 do
Unutar svake klase učestalosti, nuspojave se prijavljuju prema padajućem redoslijedu ozbiljnosti.
Najčešće prijavljene nuspojave tijekom primjene samo docetaksela su: neutropenija (reverzibilna i ne-kumulativna; prosječan dan do nadira bio je 7. dan i srednje trajanje teške neutropenije (anemija, alopecija, mučnina, povraćanje, stomatitis, proljev i astenija) Težina nuspojava docetaksela može se povećati kada se docetaksel primjenjuje u kombinaciji s drugim kemoterapijskim sredstvima.
Za kombinaciju s trastuzumabom, nuspojave (svih stupnjeva) prijavljene su kao postotak od 10%. Povećana je učestalost ozbiljnih nuspojava (40% vs 31%) i nuspojave 4. stupnja (34% vs 23%) u skupini koja je primala trastuzumab u odnosu na monoterapiju docetakselom. Za kombinaciju s kapecitabinom zabilježene su najčešće nuspojave povezane s liječenjem (≥ 5%) zabilježene u kliničkoj studiji faze III na pacijentima s rakom dojke nakon neuspjeha terapije antraciklinima (vidjeti sažetak karakteristika lijeka. Kapecitabina).
S docetakselom su se često javljale sljedeće nuspojave:
Poremećaji imunološkog sustava:
Reakcije preosjetljivosti obično su se javljale unutar nekoliko minuta od početka infuzije docetaksela i bile su općenito blage do umjerene težine. Najčešće prijavljeni simptomi bili su valunzi, osip sa ili bez svrbeža, stezanje u prsima, bolovi u leđima, dispneja te groznica ili zimica. Teške reakcije karakterizirale su hipotenzija i / ili bronhospazam ili generalizirani osip / eritem (vidjeti dio 4.4)
Poremećaji živčanog sustava:
Razvoj teške periferne neurotoksičnosti zahtijeva smanjenje doze (vidjeti dijelove 4.2 i 4.4).
Blagi do umjereni senzorineuralni znakovi karakterizirani su parestezijom, disestezijom ili boli uključujući pečenje. Neuromotorne događaje karakterizira uglavnom slabost.
Poremećaji kože i potkožnog tkiva:
Uočene su reverzibilne kožne reakcije i općenito se smatraju blage do umjerene težine. Reakcije su karakterizirale osip, uključujući lokalizirane erupcije uglavnom na stopalima i šakama (uključujući teški sindrom šaka-stopalo), ali i na rukama, licu ili prsima, često povezane sa svrbežom. Erupcije su se općenito dogodile unutar jednog tjedna od infuzije docetaksela. Rjeđe su prijavljeni teški simptomi poput erupcija praćenih deskvamacijom koji su rijetko zahtijevali privremeni ili trajni prekid liječenja (vidjeti dijelove 4.2 i 4.4). Prijavljeni su ozbiljni simptomi. hipopigmentacijom ili hiperpigmentacijom, ponekad bolom i oniholizom.
Opći poremećaji i stanja na mjestu primjene:
Reakcije na mjestu infuzije bile su općenito blage i karakterizirane su hiperpigmentacijom, upalom, crvenilom i suhoćom kože, flebitisom ili ekstravazacijom, "povećanom propusnošću" vene.
Zadržavanje tekućine koje uključuje slučajeve perifernog edema i rjeđe slučajeve pleuralnog, perikardnog izljeva, ascitesa i debljanja. Periferni edem obično se javlja počevši od donjih ekstremiteta i može se generalizirati s povećanjem tjelesne težine od 3 kg ili više. Zadržavanje tekućine kumulativno je po učestalosti i intenzitetu (vidjeti dio 4.4).
TAXOTERE 100 mg / m2 kao monoterapija
Poremećaji krvi i limfnog sustava
Rijetko: epizode krvarenja povezane s trombocitopenijom stupnja 3/4.
Poremećaji živčanog sustava
Podaci o reverzibilnosti dostupni su u 35,3% pacijenata koji su razvili neurotoksičnost nakon liječenja monoterapijom docetakselom 100 mg / m2. Događaji su se spontano reverzibilni unutar 3 mjeseca.
Poremećaji kože i potkožnog tkiva
Vrlo rijetko: jedan slučaj nepovratne alopecije na kraju studije. 73% kožnih reakcija bilo je reverzibilno u roku od 21 dana.
Opći poremećaji i stanja na mjestu primjene
Prosječna kumulativna doza pri prestanku liječenja bila je veća od 1.000 mg / m2, a srednje vrijeme do reverzibilnosti zadržavanja tekućine bilo je 16,4 tjedna (raspon od 0 do 42 tjedna). Početak umjerene do teške retencije (srednja kumulativna doza: 818,9 mg / m2) odgođen je u pacijenata koji su primili premedikaciju u usporedbi s bolesnicima bez premedikacije (srednja kumulativna doza: 489,7 mg / m2); međutim, u nekih je pacijenata zabilježeno tijekom prvih tečajeva terapije.
TAXOTERE 75 mg / m2 kao monoterapija
TAXOTERE 75 mg / m2 u kombinaciji s doksorubicinom
TAXOTERE 75 mg / m2 u kombinaciji s cisplatinom
TAXOTERE 100 mg / m2 u kombinaciji s trastuzumabom
Srčane patologije
Simptomatsko zatajenje srca prijavljeno je u 2,2% pacijenata koji su primali docetaksel u kombinaciji s trastuzumabom, u usporedbi s 0% pacijenata koji su primali samo docetaksel. U skupini koja je primala docetaksel i trastuzumab 64% pacijenata prethodno je primalo antracikline kao pomoćnu terapiju u usporedbi s 55% pacijenata liječenih samo docetakselom.
Poremećaji krvi i limfnog sustava
Vrlo često: Hematološka toksičnost povećana je u bolesnika liječenih trastuzumabom i docetakselom u usporedbi s onima koji su liječeni samo docetakselom (neutropenija stupnja 3/4 32% naspram 22% prema NCI-CTC kriterijima). Imajte na umu da je to vjerojatno podcjenjivanje jer je poznato da samo docetaksel u dozi od 100 mg / m2 dovodi do neutropenije u 97% pacijenata, 4. stupnja u 76%, na temelju najniže vrijednosti neutrofila. Učestalost febrilne neutropenije / neutropenične sepse također je povećana u bolesnika liječenih Herceptinom i docetakselom (23% naspram 17% pacijenata liječenih samo docetakselom).
TAXOTERE 75 mg / m2 u kombinaciji s kapecitabinom
TAXOTERE 75 mg / m2 u kombinaciji s prednizonom ili prednizolonom
Pomoćna terapija lijekom TAXOTERE 75 mg / m2 u kombinaciji s doksorubicinom i ciklofosfamidom u bolesnika s čvorom pozitivnim (TAX 316) i čvorom negativnim (GEICAM 9805) karcinom dojke - kumulativni podaci:
Poremećaji živčanog sustava
Tijekom praćenja, 12 od 83 bolesnika koji su doživjeli perifernu osjetnu neuropatiju na kraju kemoterapije i dalje su imali simptome periferne senzorne neuropatije.
Srčane patologije
Kongestivno zatajenje srca (CHF) prijavljeno je u 18 od 1276 pacijenata tijekom razdoblja praćenja. U čvorno pozitivnom ispitivanju (TAX316) po jedan je pacijent u svakoj terapijskoj skupini umro od zatajenja srca.
Poremećaji kože i potkožnog tkiva
Tijekom praćenja, 25 od 736 pacijenata koji su doživjeli alopeciju na kraju kemoterapije i dalje je imalo alopeciju.
Bolesti reproduktivnog sustava i dojke
Tijekom praćenja, 140 od 251 pacijenta koji su doživjeli amenoreju na kraju kemoterapije i dalje su imali simptome amenoreje.
Opći poremećaji i stanja na mjestu primjene
Tijekom praćenja, 18 od 112 pacijenata koji su doživjeli periferni edem na kraju kemoterapije u studiji TAX 316 i dalje su imali simptome perifernog edema, dok su 4 od 5 pacijenata koji su doživjeli limfedem na kraju kemoterapije u lijeku GEICAM 9805 još uvijek imali simptome perifernog edema. simptomi limfedema.
Akutna leukemija / mijelodisplastični sindrom.
Pri prosječnom praćenju od 77 mjeseci, akutna leukemija se javila u 1 od 532 (0,2%) bolesnika koji su primali docetaksel, doksorubicin i ciklofosfamid u lijeku GEICAM 9805. Nisu zabilježeni slučajevi u pacijenata koji su primali fluorouracil., Doksorubicin i ciklofosfamid. Nijedan od liječenih skupina nije dijagnosticirao slučajeve mijelodisplastičnog sindroma. Donja tablica pokazuje da je učestalost neutropenije 4. stupnja, febrilne neutropenije i neutropenične infekcije smanjena u bolesnika koji su primali primarnu profilaksu G -CSF nakon što je to postalo obvezno u TAC kraku - GEICAM studiji.
Neutropenične komplikacije u pacijenata koji su primili CT sa ili bez primarne G-CSF profilakse (GEICAM 9805)
TAXOTERE 75 mg / m2 u kombinaciji s cisplatinom i 5-fluorouracilom za adenokarcinom želuca
Poremećaji krvi i limfnog sustava
Febrilna neutropenija i neutropenična infekcija dogodile su se u 17,2% odnosno 13,5% pacijenata, bez obzira na upotrebu G-CSF-a. G-CSF je korišten za sekundarnu profilaksu u 19,3% pacijenata (10,7% tečajeva). Febrilna neutropenija i neutropenična infekcija dogodile su se respektivno u 12,1% odnosno 3,4% pacijenata koji su primali G-CSF kao profilaksu, u 15,6% i 12,9% pacijenata bez profilakse s G-CSF (vidjeti dio 4.2).
TAXOTERE 75 mg / m2 u kombinaciji s cisplatinom i 5-fluorouracilom za karcinom glave i vrata
Indukcijska kemoterapija nakon koje slijedi radioterapija (TAX 323)
Indukcijska kemoterapija nakon koje slijedi kemoterapija (TAX324)
Postmarketinško iskustvo:
Dobroćudne, zloćudne i neodređene neoplazme (uključujući ciste i polipe)
Vrlo rijetki slučajevi akutne mijeloične leukemije i mijelodisplastičnog sindroma zabilježeni su kada se docetaksel koristi u kombinaciji s drugim kemoterapijskim i / ili radioterapijskim sredstvima.
Poremećaji krvi i limfnog sustava
Prijavljene su supresije koštane srži i druge hematološke nuspojave. Često se prijavljuje diseminirana intravaskularna koagulacija povezana sa sepsom ili zatajenjem više organa.
Poremećaji imunološkog sustava
Prijavljeno je nekoliko slučajeva anafilaktičkog šoka, neki sa smrtnim ishodom.
Poremećaji živčanog sustava
Rijetki su slučajevi konvulzija ili privremenog gubitka svijesti nakon primjene docetaksela. Te se reakcije ponekad pojavljuju tijekom infuzije.
Poremećaji oka
Vrlo rijetki slučajevi prolaznih vizualnih promjena (bljeskovi, bljeskovi svjetlosti, skotom) i povezani s reakcijama preosjetljivosti obično su se javljali tijekom infuzije lijeka. Oni su bili reverzibilni nakon prestanka infuzije. Rijetko su prijavljeni slučajevi suzenja sa ili bez konjunktivitisa, poput slučajeva začepljenja suznog kanala kao posljedica prekomjernog kidanja.
Poremećaji uha i labirinta
Prijavljeni su rijetki slučajevi ototoksičnosti, oštećenja sluha i / ili gubitka sluha.
Srčane patologije
Prijavljeni su rijetki slučajevi infarkta miokarda.
Vaskularne patologije
Rijetko su prijavljeni venski tromboembolijski događaji.
Poremećaji disanja, prsnog koša i medijastinuma
Rijetko su prijavljeni akutni respiratorni distres sindrom, intersticijska upala pluća i plućna fibroza. Rijetki slučajevi upale pluća izazvane zračenjem zabilježeni su u pacijenata koji su također podvrgnuti terapiji zračenjem.
Gastrointestinalni poremećaji
Rijetke epizode dehidracije zabilježene su kao posljedica gastrointestinalnih smetnji, gastrointestinalne perforacije, ishemijskog kolitisa, kolitisa i neutropeničnog enterokolitisa. Zabilježeni su rijetki slučajevi ilealne i crijevne opstrukcije.
Hepatobiliarni poremećaji
Vrlo rijetki slučajevi hepatitisa, ponekad smrtonosni, prijavljeni su uglavnom u bolesnika s već postojećom bolešću jetre.
Poremećaji kože i potkožnog tkiva
Slučajevi eritematozni lupus kožne i bulozne erupcije poput multiformnog eritema, Stevens-Johnsonovog sindroma, toksične epidermalne nekrolize. U nekim slučajevima, drugi popratni čimbenici mogli su pridonijeti razvoju ovih učinaka. Tijekom liječenja docetakselom zabilježene su manifestacije slične Schlerodermi, kojima je obično prethodio periferni limfedem.
Opći poremećaji i stanja na mjestu primjene
Rijetko su zabilježeni fenomeni prisjećanja zračenja.
Zadržavanje tekućine nije bilo povezano s akutnim epizodama oligurije ili hipotenzije. Rijetko su prijavljeni dehidracija i plućni edem.
04.9 Predoziranje
Prijavljeni su neki slučajevi predoziranja. Nema poznatih protuotrova za predoziranje docetakselom. U slučaju predoziranja, bolesnika treba držati u specijaliziranoj jedinici i pomno pratiti vitalne funkcije.U slučaju predoziranja može se očekivati pogoršanje nuspojava. Glavne komplikacije koje se mogu očekivati pri predoziranju su supresija koštane srži, periferna neurotoksičnost i mukozitis. Pacijenti bi trebali dobiti terapijski G-CSF što je prije moguće nakon dokaza o predoziranju. Po potrebi treba poduzeti i druge odgovarajuće simptomatske mjere.
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: taksani, ATC oznaka: L01CD 02
Pretklinički podaci:
Docetaksel je antineoplastični lijek koji djeluje promicanjem agregacije tubulina u stabilne mikrotubule i inhibira njihovu razgradnju, što dovodi do značajnog smanjenja slobodnog tubulina. Vezanje docetaksela na mikrotubule ne mijenja broj protofilamenata. Docetaksel in vitro razbija stanični mikrotubularni sustav koji je bitan za vitalne stanične funkcije poput mitoze i interfaze.
Docetaksel in vitro citotoksičan je za različite tumorske linije miševa i ljudi i humane tumore nedavno uklonjene u provedenim klonogenim testovima. Docetaksel postiže visoke i dugotrajne unutarstanične koncentracije. Nadalje, docetaksel je aktivan na nekim staničnim linijama (ali ne na svim) koje izražavaju višak p-glikoproteina, kodiran genom za otpornost na više lijekova. In vivo, docetaksel eksperimentalno ima širok spektar djelovanja protiv uznapredovalih tumora miševa i cijepljenih tumora čovjeka, bez obzira na režim doziranja.
Klinički podaci:
Rak dojke
TAXOTERE u kombinaciji s doksorubicinom i ciklofosfamidom: pomoćno liječenje.
Bolesnice s operativnim čvorom pozitivnim karcinomom dojke (TAX 316)
Podaci iz otvorene, randomizirane multicentrične studije podržavaju uporabu docetaksela kao pomoćnog lijeka u bolesnica s karcinomom dojke pozitivnim na operativne čvorove i KPS 3 80% u dobi od 18 do 70 godina. Nakon stratifikacije prema broju pozitivnih limfnih čvorova (1-3 , više od 4), 1491 pacijent je randomiziran za primanje docetaksela 75 mg / m2 primijenjenog 1 sat nakon doksorubicina 50 mg / m2 i ciklofosfamida 500 mg / m2 (TAC skupina) ili doksorubicina 50 mg / m2, a zatim iz fluorouracila 500 mg / m2 i ciklofosfamid 500 mg / m2 (FAC grupa) .Oba režima primjenjivana su jednom svaka 3 tjedna tijekom 6 ciklusa. Docetaksel je davan kao 1-satna infuzija, svi drugi lijekovi davani su kao intravenozni bolus 1. dana. G-CSF je davan kao sekundarna profilaksa kod pacijenata sa kompliciranom neutropenijom (febrilna neutropenija, produljena neutropenija ili infekcija).
Pacijenti u TAC skupini primali su antibiotsku profilaksu uz 500 mg ciprofloksacina oralno ili ekvivalentne antibiotike dva puta dnevno tijekom 10 dana, počevši od 5. dana svakog ciklusa. U obje skupine, nakon posljednjeg tijeka kemoterapije, pacijenti pozitivni na receptore estrogena i / ili progestagena primali su tamoksifen 20 mg / dan tijekom 5 godina. Adjuvantna terapija zračenjem propisana je prema smjernicama u svakom centru sudionici i primijenjena je na 69 pacijenata. % pacijenata koji su primili TAC i do 72% pacijenata koji su primili FAC.
Privremena analiza provedena je uz medijan praćenja od 55 mjeseci. Preživljavanje bez bolesti značajno je povećano u TAC skupini u odnosu na FAC skupinu.
Učestalost recidiva u petogodišnjem razdoblju smanjena je u pacijenata koji su primali TAC u usporedbi s onima koji su primali FAC (25% naspram 32% respektivno), odnosno apsolutno smanjenje rizika od 7% (p = 0,001). Sveukupno preživljavanje nakon 5 godina također je bilo značajno povećana s TAC -om u usporedbi s FAC -om (87% vs 81% respektivno) tj apsolutno smanjenje rizika od 6% (p = 0,008). Analizirane su podskupine pacijenata liječenih TAC -om u skladu s glavnim prognostičkim čimbenicima definiranim a priori:
* omjer opasnosti manji od 1 ukazuje na to da je TAC povezan s preživljavanjem bez bolesti i ukupnim preživljavanjem superiornijim od FAC-a
U privremenoj analizi nije dokazana terapijska prednost TAC -a u bolesnika s 4 ili više limfnih čvorova (37% populacije).Čini se da je terapijska prednost TAC-a manje evidentna od one koja se vidi u bolesnika s 1-3 pozitivna limfna čvora. Stoga omjer rizika i koristi u bolesnika s 4 ili više pozitivnih limfnih čvorova u ovoj fazi analize nije u potpunosti definiran.
Pacijenti s operativnim čvorovima negativnim karcinomom dojke kandidati za kemoterapiju (GEICAM 9805):
Podaci iz multicentrične, otvorene, randomizirane studije podržavaju uporabu TAXOTERE-a za adjuvantnu terapiju u pacijenata s operativnim čvorom negativnim karcinomom dojke koji su kandidati za kemoterapiju. 1060 pacijenata randomizirano je za primanje TAXOTERE-a 75 mg / m2 primijenjeno 1 sat nakon doksorubicina. 50 mg / m2 i ciklofosfamid 500 mg / m2 (539 pacijenata u TAC kraku), ili doksorubicin 50 mg / m2 nakon čega slijede fluorouracil 500 mg / m2 i ciklofosfamid 500 mg / m2 (521 pacijent u grupi FAC) kao pomoćna terapija kod raka operabilnog limfnog čvora dojke s visokim rizikom od recidiva prema kriterijima St. Gallena iz 1998. (veličina tumora> 2 cm i / ili ER i PR negativan i / ili visok histološki / nuklearni stupanj (stupanj 2 do 3) i / ili dob
Prosječno trajanje praćenja bilo je 77 mjeseci. Za TAC-skupinu je pokazano statistički značajno povećanje preživljavanja bez bolesti u usporedbi s FAC-om. Pacijenti liječeni TAC-om imali su 32% smanjenje rizika od recidiva u usporedbi s onima liječenima FAC (omjer opasnosti = 0,68, 95% CI (0,49-0,93), p = 0,01). Sveukupno preživljavanje (OS) također je bilo duže u skupini koja je primala TAC sa 24% smanjenjem rizika od smrti za pacijente liječene TAC-om u odnosu na FAC (omjer opasnosti = 0,76, 95% CI (0,46-1, 26, p = 0,29) Međutim, raspodjela ukupnog preživljavanja nije se značajno razlikovala između dvije skupine.
Podgrupe pacijenata liječenih TAC -om analizirane su podijeljene prema prospektivno definiranim glavnim prognostičkim čimbenicima (vidi tablicu u nastavku):
Analiza podskupina-Studija adjuvantne terapije u bolesnica s čvorno negativnim karcinomom dojke (Analiza namjere liječenja)
* omjer opasnosti (TAC / FAC) manji od 1 ukazuje da je TAC povezan s dužim preživljavanjem bez bolesti od FAC-a.
Provedene su istraživačke analize podskupina za preživljavanje bez bolesti u pacijenata koji zadovoljavaju kriterije kemoterapije St. Gallen iz 2009. (populacija ITT -a) i prikazani su u donjoj tablici:
TAC = docetaksel, doksorubicin i ciklofosfamid
FAC = 5-fluorouracil, doksorubicin i ciklofosfamid
CI = interval pouzdanosti; ER = receptor za estrogen
PR = receptor za progesteron
ER / PR-negativan ili stupanj 3 ili veličina tumora> 5 cm
Omjer opasnosti procijenjen je s Coxovim proporcionalnim modelom opasnosti koristeći terapijsku skupinu kao faktor.
TAXOTERE kao jedini tretman
Dvije randomizirane usporedne studije faze III s docetakselom u preporučenim dozama i režimom od 100 mg / m2 svaka 3 tjedna provedene su u bolesnica s metastatskim rakom dojke, od čega 326 nakon neuspjeha liječenja alkiliranjem i 392 nakon neuspjeha liječenja antraciklinima.
U bolesnika kod kojih je utvrđeno da je liječenje alkilirajućim tvarima neučinkovito, docetaksel je uspoređen s doksorubicinom (75 mg / m2 svaka 3 tjedna). Docetaksel je povećao stopu odgovora (52% naspram 37%, p = 0,01) i smanjio vrijeme odgovora (12 tjedana u odnosu na 23 tjedna, p = 0,007), bez promjene vremena preživljavanja (15 mjeseci za docetaksel naspram 14 mjeseci za doksorubicin, p = 0,38) ili vrijeme do progresije (27 tjedana za docetaksel naspram 23 tjedna za doksorubicin, p = 0,54). Tri pacijenta liječena docetakselom (2%) morala su prekinuti liječenje zbog zadržavanja tekućine, dok je 15 pacijenata liječenih doksorubicinom (9%) moralo prekinuti liječenje zbog srčane toksičnosti (tri smrti zbog kongestivnog zatajenja srca).
U bolesnika kod kojih je liječenje antraciklinima bilo neučinkovito, docetaksel je uspoređen s kombinacijom mitomicina C i vinblastina (12 mg / m2 svakih 6 tjedana i 6 mg / m2 svaka 3 tjedna). Docetaksel je povećao stopu odgovora (33% vs 12%, str
Profil podnošljivosti docetaksela tijekom ove dvije studije III faze bio je u skladu s profilom podnošljivosti nađenim u studijama faze II (vidjeti dio 4.8).
Randomizirano, otvoreno, multicentrično ispitivanje faze III koje je uspoređivalo monoterapiju docetakselom s paklitakselom provedeno je u liječenju uznapredovalog raka dojke u pacijenata u kojih je prethodna terapija već uključivala "antraciklin. Ukupno je 449 pacijenata randomizirano na monoterapiju docetakselom 100" mg / m2 kao infuzija od 1 sata ili paklitaksel 175 mg / m2 kao infuzija od 3 sata, pri čemu se dva tretmana primjenjuju svaka 3 tjedna.
Docetaksel je produžio medijan vremena do progresije (24,6 tjedana u odnosu na 15,6 tjedana; str
TAXOTERE u kombinaciji s doksorubicinom
Randomizirano ispitivanje faze III provedeno je na 429 pacijenata s neliječenim metastatskim rakom uspoređujući doksorubicin (50 mg / m2) u kombinaciji s docetakselom (75 mg / m2) (AT krak) s doksorubicinom (60 mg / m2) u kombinaciji s ciklofosfamid (600 mg / m2) (AC krak). Oba režima primjenjivana su 1. dana svaka tri tjedna.
Vrijeme do progresije (TTP) značajno je povećano u kraku AT u usporedbi s razdobljem u skupini AC, p = 0,0138. Medijan TTP iznosio je 37,3 tjedana (95% CI: 33,4 - 42,1) u AT grupi i 31,9 tjedana (95% CI: 27,4 - 36,0) u AC grupi.
Opažena stopa odgovora bila je značajno veća u kraku AT nego u skupini AC, p = 0,009. Ta je stopa bila 59,3% (95% CI: 52,8 - 65,9) u AT grupi u usporedbi s 46,5% (95% CI: 39,8 - 53,2) u AC grupi.
U ovoj studiji, AT grupa imala je veću učestalost teške neutropenije (90% vs 68,6%), febrilne neutropenije (33,3% vs 10%), infekcija (8% vs 2,4%), proljeva (7,5% vs. 1,4%), astenija (8,5%vs 2,4%) i bol (2,8%naspram 0%). S druge strane, AC skupina pokazala je veću učestalost teške anemije od AT grupe (15,8% naspram 8,5%) i veću učestalost srčane toksičnosti: kongestivno zatajenje srca (3,8% naspram 2,8%), apsolutno smanjenje LVEF 3 20% (13,1% naspram 6,1%), apsolutno smanjenje LVEF -a ≥ 30% (6,2% naspram 1,1%). Toksična smrt dogodila se u 1 pacijenta u kraku AT (kongestivno zatajenje srca) i u 4 bolesnika u skupini AC (1 zbog septičkog šoka i 3 zbog kongestivnog zatajenja srca).
U obje ruke, kvaliteta života, mjerena EORTC upitnikom, bila je usporediva i stabilna tijekom liječenja i praćenja.
TAXOTERE u kombinaciji s trastuzumabom
Docetaksel u kombinaciji s trastuzumabom procijenjen je u liječenju pacijenata s metastatskim rakom dojke s prekomjernom ekspresijom HER2 i koji nisu prethodno primali kemoterapiju za metastatsku bolest. 186 pacijenata randomizirano je za primanje docetaksela (100 mg / m2) sa ili bez trastuzumaba; 60% pacijenata prethodno je primalo adjuvantnu kemoterapiju s antraciklinima. Docetaksel s trastuzumabom bio je učinkovit u pacijenata koji su prethodno imali ili nisu primali adjuvantnu terapiju antraciklinima. Najčešće korišteni test za određivanje HER2 pozitivnosti u ovoj ključnoj studiji bila je imunohistokemija (IHC). Fluorescentni in situ test (FISH) korišten je za manji broj pacijenata. U ovoj studiji 87% pacijenata imalo je bolest koja je bila IHC 3+, a 95% uključenih pacijenata imalo je IHC 3+ bolest i / ili FISH pozitivnu. Rezultati učinkovitosti sažeti su u donjoj tablici:
TTP = vrijeme do progresije; "ne" označava da se ne može procijeniti ili još nije bilo
posegnuo.
1 Populacija koja se namjerava liječiti
2 Procijenjeno medijan preživljavanja
TAXOTERE u kombinaciji s kapecitabinom
Podaci iz multicentričnog, randomiziranog, kontroliranog kliničkog ispitivanja faze III podržavaju uporabu docetaksela u kombinaciji s kapecitabinom za liječenje pacijenata s lokalno uznapredovalim ili metastatskim rakom dojke nakon neuspjeha citotoksične kemoterapije koja je uključivala antraciklin. U ovom je istraživanju 255 pacijenata randomizirano na liječenje docetakselom (75 mg / m2 kao 1-satna intravenska infuzija svaka 3 tjedna) i kapecitabinom (1250 mg / m2 dva puta dnevno tijekom 2 tjedna, nakon čega slijedi 1-tjedni odmor.). 256 pacijenata je randomizirano na liječenje samo docetakselom (100 mg / m2 kao 1 -satna intravenska infuzija svaka 3 tjedna). Opstanak je bio bolji u skupini koja je primala docetaksel + kapecitabin (p = 0,0126). Prosječno preživljenje iznosilo je 442 dana (docetaksel + kapecitabin) u usporedbi s 352 dana (samo docetaksel). Ukupna objektivna stopa odgovora u cijeloj randomiziranoj populaciji (procjena istraživača) bila je 41,6% (docetaksel + kapecitabin) u odnosu na 29,7% (samo docetaksel); p = 0,0058. Vrijeme do progresije bolesti bilo je superiorno u skupini koja je primala docetaksel + kapecitabin (p
Rak pluća bez malih stanica
Pacijenti koji su prethodno bili liječeni kemoterapijom sa ili bez radioterapije
U kliničkoj studiji faze III, u prethodno liječenih pacijenata, vrijeme do progresije (12,3 tjedna u odnosu na 7 tjedana) i preživljenje značajno su povećani uz docetaksel na 75 mg / m2 u usporedbi s najboljim potpornim tretmanom (MTS).
Stopa jednogodišnjeg preživljavanja bila je značajno veća s docetakselom (40%) nego s MTS-om (16%).
Manje morfija korišteno je u bolesnika liječenih docetakselom u dozi od 75 mg / m2 (p ne-morfij analgetici (p
U pacijenata koji se mogu ocijeniti, ukupna stopa odgovora bila je 6,8%, a prosječno trajanje odgovora bilo je 26,1 tjedan.
TAXOTERE u kombinaciji s derivatima platine u pacijenata koji nikada nisu liječeni kemoterapijom
U studiji faze III, 1218 bolesnika s neoperabilnim staničnim karcinomom pluća malih stadija IIIB ili IV, s Karnofskyjevim stanjem uspješnosti od 70% i više, koji nisu prethodno primali kemoterapiju za ovo stanje, randomizirano je na docetaksel (T) 75 mg / m2 kao jednosatna infuzija, nakon čega slijedi odmah cisplatin (TCis) 75 mg / m2 tijekom 30-60 minuta svaka tri tjedna, docetaksel 75 mg / m2 kao jednosatna infuzija u kombinaciji s karboplatinom (AUC 6 mg / ml). min) tijekom 30-60 minuta svaka tri tjedna, ili vinorelbin (VCis) 25 mg / m2 primijenjen tijekom 6-10 minuta 1., 8., 15., 22. dana, nakon čega slijedi 100 mg / m2 cisplatina primijenjenog prvog dana ciklusa svaka 4 tjedna.
Podaci o preživljavanju, srednjem vremenu do progresije i stopi odgovora za dvije grupe studija prikazani su u donjoj tablici.
*: Ispravljeno za više usporedbi i prilagođeno faktorima stratifikacije (stadij bolesti i regija liječenja), na temelju procjenjive populacije pacijenata.
Sekundarne krajnje točke uključivale su promjenu boli, globalnu procjenu kvalitete života prema EuroQoL-5D, Ljestvicu simptoma raka pluća (LCSS) i promjenu statusa Karnofskog. Rezultati ovih ciljeva potvrdili su rezultate primarnih ciljeva.
Za kombinaciju docetaksel / karboplatin nije bilo moguće dokazati ekvivalentnost ili ne inferiornost učinkovitosti u odnosu na referentni tretman: kombinaciju VCis.
Rak prostate
Podnošljivost i djelotvornost docetaksela u kombinaciji s prednizonom ili prednizolonom u bolesnika s hormonski refraktornim metastatskim karcinomom prostate ocijenjeni su u multicentričnoj randomiziranoj studiji faze III. Ukupno 1006 pacijenata s KPS 60 randomizirano je u sljedeće terapijske skupine:
Docetaksel 75 mg / m2 svaka 3 tjedna tijekom 10 ciklusa.
Docetaksel 30 mg / m2 primjenjuje se tjedno prvih 5 tjedana 6-tjednog ciklusa tijekom ukupno 5 ciklusa.
Mitoksantron 12 mg / m2 svaka 3 tjedna tijekom 10 ciklusa.
Sva tri režima primjenjivana su u kombinaciji s prednizonom ili prednizolonom od 5 mg dva puta dnevno, kontinuirano.
Pacijenti koji su primali docetaksel svaka tri tjedna pokazali su značajno duže ukupno preživljavanje od pacijenata liječenih mitoksantronom. Povećanje preživljavanja uočeno u skupini liječenoj docetakselom svaki tjedan nije bilo statistički značajno u usporedbi s kontrolnom skupinom liječenom mitoksantronom. Parametri učinkovitosti dobiveni u skupinama liječenim docetakselom u usporedbi s kontrolnom skupinom sažeti su u sljedećoj tablici:
† Stratificirani test ranga dnevnika
* Granica za statističku značajnost = 0,0175
** PSA: Prostat-specifični antigen
Budući da je docetaksel svaki tjedan imao nešto bolji profil podnošljivosti od docetaksela svaka 3 tjedna, moguće je da će neki pacijenti imati koristi od tjedne terapije docetakselom.
Nije bilo statistički značajne razlike u ukupnoj kvaliteti života između tretiranih skupina.
Adenokarcinom želuca
Provedena je multicentrična, randomizirana, otvorena studija kako bi se procijenila sigurnost i djelotvornost docetaksela u liječenju pacijenata s metastatskim želučanim adenokarcinomom, uključujući adenokarcinom gastroezofagealnog spoja, koji prethodno nisu primali kemoterapiju zbog metastatske bolesti. Ukupno 445 pacijenata s KPS> 70 liječeno je docetakselom (T) (75 mg / m2 1. dana) u kombinaciji s cisplatinom (C) (75 mg / m2 1. dana) i 5-fluorouracilom (F) (750 mg / m2 dnevno tijekom 5 dana) ili s cisplatinom (100 mg / m2 1. dana) i 5-fluorouracilom (1000 mg / m2 dnevno tijekom 5 dana). Trajanje ciklusa liječenja bilo je 3 tjedna za TCF grupu i 4 tjedna za CF skupinu. Prosječan broj ciklusa koji su primijenjeni po pacijentu bio je 6 (s rasponom 1-16) za TCF krak i 4 (s rasponom 1-12) za CF skupinu. Primarna krajnja točka bila je vrijeme do progresije (TTP). Smanjenje rizika od progresije bilo je 32,1% i bilo je povezano sa značajno dužim TTP -om (p = 0,0004) za krak TCF -a. Sveukupno preživljavanje također je bilo značajno duže (p = 0,0201) za skupinu TCF sa smanjenjem rizika od mortaliteta za 22,7%. Rezultati učinkovitosti sažeti su u sljedećoj tablici:
Učinkovitost docetaksela u liječenju pacijenata s adenokarcinomom želuca
* Nestratificirani logrank test
Analize podskupina prema dobi, spolu i rasi dosljedno su favorizirale TCF krak u odnosu na CF skupinu.
Ažurirana analiza preživljavanja provedena sa prosječnim vremenom praćenja od 41,6 mjeseci više nije pokazala statistički značajnu razliku, iako uvijek u korist režima TCF-a, te je naglasila da je korist TCF-a nad CF evidentna. Između 18 i 30 mjeseci praćenja -gore.
Sveukupno, kvaliteta života (QoL) i rezultati kliničke dobrobiti dosljedno su ukazivali na poboljšanje u korist TCF grupe. Pacijenti liječeni TCF-om imali su 5% duže vrijeme do pogoršanja zdravstvenog stanja u upitniku QLQ-C30 (p = 0.0121) i duže vrijeme do definitivnog pogoršanja Karnofskyjevog učinka (p = 0, 0088) u usporedbi s bolesnicima liječenim od CF .
Rak glave i vrata
Indukcijska kemoterapija nakon koje slijedi radioterapija (TAX 323)
Sigurnost i djelotvornost docetaksela u indukcijskom liječenju pacijenata sa karcinomom pločastih stanica glave i vrata (SCCHN) procijenjeni su u otvorenoj, multicentričnoj randomiziranoj studiji faze III (TAX323). U ovoj studiji 358 pacijenata s lokalnim napredni neoperabilni SCCHN sa statusom učinka WHO -a 0 - 1. randomizirani su iz jedne do dvije grupe. Pacijenti koji su primali docetaksel (T) 75 mg / m2, a zatim cisplatin (P) 75 mg / m2, a zatim 5- fluorouracil (F) 750 mg / m2 dnevno kao kontinuirana infuzija tijekom 5 dana Ovaj režim doziranja primjenjuje se svaka tri tjedna kroz 4 ciklusa, nakon 2 ciklusa primijećen je minimalni odgovor (> 25% skupljanja tumora mjereno u dvije dimenzije). Na kraju kemoterapije, uz minimalni interval od 4 tjedna, a najviše sedam tjedana, pacijenti kod kojih bolest ne napreduje primaju radioterapiju (RT), u skladu s institucionalnim smjernicama, 7 tjedana. i (TPF / RT). Pacijenti u usporednoj skupini primali su cisplatin (P) 100 mg / m2, a zatim 5-fluorouracil (F) 1000 mg / m2 dnevno tijekom 5 dana. Ovaj režim doziranja primjenjivao se svaka tri tjedna tijekom 4 ciklusa ako je nakon 2 ciklusa primijećen barem jedan odgovor (≥ 25% smanjenje izmjerene dvodimenzionalne veličine tumora). Na kraju kemoterapije, s minimalnim razmakom od 4 tjedna i maksimalnim razmakom od 7 tjedana, pacijenti kod kojih bolest nije napredovala primali su radioterapiju (RT) prema smjernici 7 tjedana (PF / RT). Lokoregionalna radioterapija primijenjena je na konvencionalnu frakciju (1,8 Gy-2,0 Gy jednom dnevno, 5 dana u tjednu za ukupnu dozu od 66 do 70 Gy) ili na ubrzane / hiperfrakcionirane režime radioterapije (dva puta dnevno, s minimalnim razmakom od frakcije od 6 sati, od 5 dana u tjednu). Ukupno je predloženo 70 Gy za ubrzane režime i 74 Gy za hiperfrakcionirane sheme. Kirurška resekcija dopuštena je nakon kemoterapije, prije ili nakon radioterapije. Pacijenti u grupi sa TPF -om primali su oralno ciprofloksacin 500 mg dva puta dnevno tijekom 10 dana, počevši od 5. dana svakog ciklusa, ili ekvivalentno, kao profilaksu. Primarna krajnja točka u ovoj studiji, preživljenje bez progresije bolesti (PFS), bila je značajno duža u skupini sa TPF -om nego u skupini s PF -om, p = 0,0042 (medijan PFS: 11,4 naspram 8,3 mjeseca, respektivno) sa prosječnim vremenom od 33,7 mjeseci. preživljavanje je također bilo značajno duže u skupini koja je primala TPF u usporedbi s PF (medijan OS: 18,6 naspram 14,5 mjeseci, respektivno) sa smanjenjem rizika od mortaliteta za 28%, p = 0,0128. Rezultati učinkovitosti prikazani su u donjoj tablici:
Učinkovitost docetaksela u indukcijskom liječenju pacijenata s lokalno uznapredovalim neoperabilnim SCCHN -om. (Analiza namjere liječenja).
Omjer opasnosti manji od 1 u korist kombinacije docetaksel + cisplatin + 5-FU
* Coxov model (prilagodba za primarno mjesto tumora, stupnjevanje na T i N i PS-WHO)
** Logrank test
*** Hi-kvadrat test
Parametri koji definiraju kvalitetu života.
Pacijenti liječeni TPF-om pokazuju značajno smanjenje pogoršanja općeg zdravstvenog stanja u usporedbi s onima liječenim PF-om (p = 0,01, koristeći EORTC QLQ-C30 ljestvicu).
Parametri za definiranje kliničkih prednosti
Utvrđeno je da je ljestvica performansi za glavu i vrat (PSS-HN), koja je imala za cilj mjerenje razumijevanja govora, mogućnosti jedenja u javnosti i normalnosti prehrane, značajno u korist grupe TPF u usporedbi s grupom PF . Prosječno vrijeme do prvog pogoršanja stanja učinka WHO -a bilo je značajno duže u skupini s TPF -om u usporedbi s grupom PF. Ljestvica intenziteta boli pokazuje poboljšanje tijekom liječenja u obje skupine, što ukazuje na to da je liječenje boli odgovarajuće.
Indukcijska kemoterapija nakon koje slijedi kemoradioterapija (TAX324)
Sigurnost i djelotvornost docetaksela u indukcijskom liječenju pacijenata s lokalno uznapredovalim karcinomom pločastih stanica glave i vrata (SCCHN) procijenjena je u fazi III, randomiziranom, otvorenom, multicentričnom kliničkom ispitivanju (TAX 324), 501 pacijent s lokalno napredni SCCHN sa statusom uspješnosti WHO -a 0 ili 1. randomizirani su u jedan od dva kraka. Istraživačka populacija također je uključivala tehnički neoperabilne pacijente, pacijente s malom vjerojatnošću uspješne kirurške resekcije i pacijente koji su imali za cilj očuvanje organa. profil sigurnosti i djelotvornosti uzimao je u obzir samo krajnje točke preživljavanja, dok se uspjeh u očuvanju organa nije formalno razmatrao.
Pacijenti liječeni docetakselom primali su docetaksel (T) 75 mg / m2 u obliku intravenske infuzije prvog dana nakon čega je slijedila 100 mg cisplatina (P) u obliku intravenske infuzije u trajanju od 30 minuta do tri sata, nakon čega je uslijedila kontinuirana intravenska infuzija od 5 dana fluorouracil (F) 1000 mg / m2 / dan od 1. do 4. dana. Ciklusi su se ponavljali svaka tri tjedna tijekom 3 ciklusa.
Svi pacijenti koji nisu imali progresiju bolesti trebali su primati kemoterapiju (CRT) prema protokolu (TPF / CRT). Pacijenti u usporednoj skupini primali su cisplatin (P) 100 mg / m2 primijenjen kao infuzija u trajanju od 30 minuta do tri sata 1. dana, nakon čega je slijedila 5-fluorouracil (F) 1000 mg / m2 / dan od 1. do 5. dana. Ciklusi su se ponavljali svaka tri tjedna tijekom 3 ciklusa. Svi pacijenti koji nisu imali progresiju bolesti trebali su primati CRT-ove usklađene s protokolom (PF / CRT).
Bolesnici u oba kraka liječenja primali su 7 dana CRT -a nakon indukcijske kemoterapije s minimalnim razmakom od 3 tjedna i ne dulje od 8 tjedana nakon početka posljednjeg ciklusa (22. dan do 56. dan. Tijekom radioterapije davan je karboplatin (AUC 1,5) kao jednosatna intravenska infuzija do 7 doza. Zračenje je davano visokonaponskim instrumentom uz svakodnevno frakcioniranje (2Gy dnevno, 5 dana u tjednu tijekom 7 tjedana, za ukupnu dozu od 70-72 Gy). Operacija na mjestu primarnog tumora i / ili vratu mogla bi se razmotriti u bilo koje vrijeme nakon završetka CRT -a. Svi ispitivani pacijenti u grupi s docetakselom primali su antibiotsku profilaksu. Primarna krajnja točka učinkovitosti ove studije, preživljenje (OS) bilo je znatno duže (log-rank test p = 0,0058) s režimom koji je sadržavao docetaksel u usporedbi s PF (medijan OS: 70,6 vs 30,1 mjeseci, respektivno), uz smanjenje od 30% u riziku od smrti od PF (omjer opasnosti (HP) = 0,70, 95% interval pouzdanosti (CI) = 0,54-0,90) pri medijanu praćenja od 41,9 mjeseci. Sekundarna krajnja točka, PFS, pokazala je smanjenje za 29% rizik od progresije ili smrti i poboljšanje medijane PFS -a od 22 mjeseca (35,5 mjeseci za TPF i 13,1 za PF). To je također bilo statistički značajno s HR od 0,71, 95% CI 0,56-0,90; log-rank test p = 0,004. Rezultati učinkovitosti prikazani su u sljedećoj tablici:
Omjer opasnosti manji od 1 u korist kombinacije docetaksel + cisplatin + 5-fluorouracil
* prilagodba testa ranga dnevnika
** prilagodba testa ranga dnevnika, bez prilagodbi za više usporedbi
*** Hi-kvadrat test, bez prilagodbi za više usporedbi
NA - nije primjenjivo
Europska agencija za lijekove odobrila je odricanje od obveze pružanja rezultata studija s lijekom TAXOTERE u svim podskupinama pacijenata pedijatrijske populacije oboljelih od raka dojke, raka malih stanica pluća, raka prostate, raka želuca i raka glave i vrata, isključujući manje diferenciran nazofaringealni karcinom tipa II i tipa III (vidjeti dio 4.2 za informacije o pedijatrijskoj uporabi).
05.2 "Farmakokinetička svojstva
Farmakokinetika docetaksela proučavana je u pacijenata s rakom nakon primjene 20-115 mg / m2 u studijama faze I. Kinetički profil docetaksela ne ovisi o dozi i u skladu je s farmakokinetičkim modelom s tri odjeljka, s poluživotom po fazama a, b i b od 4 min., 36 min. i 11,1 sati. Kasna faza djelomično je posljedica relativno sporog vraćanja docetaksela iz perifernog odjeljka. Nakon primjene 100 mg / m2 u obliku jednosatne infuzije, postignuta je srednja vršna razina u plazmi od 3,7 mcg / ml, s odgovarajućom AUC od 4,6 h mcg / ml. Srednje vrijednosti ukupnog klirensa i volumen distribucije u stanju ravnoteže bile su 21 1 / h / m2 i 113 L. Interindividualne promjene u ukupnom klirensu bile su približno 50%. Docetaksel se više od 95% veže za proteine plazme.
Studija s 14C-docetakselom provedena je kod tri bolesnika s rakom. Docetaksel se izlučuje urinom i izmetom oksidacijom terc-butil estera posredovanom citokromom P 450; u roku od sedam dana približno 6% i 75% primijenjene radioaktivnosti izlučuje se urinom, odnosno izmetom. Otprilike 80% radioaktivnosti nađene u izmetu izlučuje se u prvih 48 sati kao jedan glavni metabolit i tri neaktivna mala metabolita te vrlo male količine matičnog lijeka.
Populacijska farmakokinetička studija provedena je na 577 pacijenata. Farmakokinetički parametri izračunati modelom bili su vrlo bliski onima uočenim u studijama faze I. Farmakokinetika docetaksela nije se mijenjala prema dobi ili spolu pacijenta. U malog broja pacijenata (n = 23) s biokemijskim rezultatima. Što ukazuje na umjerenu jetrenu vrijednost disfunkcija (ALAT, ASAT 3 1,5 puta gornja granica normale, povezana s alkalnom fosfatazom 3 2,5 gornja granica normale), ukupni klirens smanjen je u prosjeku za 27% (vidjeti dio 4.2). Klirens docetaksela nije pogođen u bolesnika s blagom ili umjerenom zadržavanje tekućine Nema podataka o bolesnicima s teškim zadržavanjem tekućine.
Kada se koristi u kombinaciji, docetaksel ne utječe na klirens doksorubicina i razine doksorubicinola u plazmi (metabolit doksorubicina). Njihova istodobna primjena ne utječe na farmakokinetiku docetaksela, doksorubicina i ciklofosfamida.
Studija prve faze koja je procjenjivala učinke kapecitabina na farmakokinetiku docetaksela i obrnuto pokazala je da nema učinka kapecitabina na farmakokinetiku docetaksela (Cmax i AUC) i da nema učinka docetaksela na farmakokinetiku metabolita. relevantno za kapecitabin, 5 "-DFUR.
Klirens docetaksela u kombiniranoj terapiji s cisplatinom bio je sličan onomu primijećenom tijekom monoterapije. Farmakokinetički profil cisplatina primijenjenog nedugo nakon infuzije docetaksela sličan je onom primijećenom samo sa cisplatinom.
Kombinirana primjena docetaksela, cisplatina i 5-fluorouracila u 12 pacijenata sa solidnim tumorima nije imala utjecaja na farmakokinetiku pojedinih lijekova.
Učinak prednizona na farmakokinetiku docetaksela primijenjenog sa standardnom premedikacijom s deksametazonom proučavan je u 42 bolesnika. Nije uočen učinak prednizona na farmakokinetiku docetaksela.
05.3 Pretklinički podaci o sigurnosti
Kancerogeni potencijal docetaksela nije proučavan.
U testu se pokazalo da je docetaksel mutagen in vitro kromosomske aberacije u CHO-K1 stanicama e in vivo u testu mikronukleusa miša. Međutim, docetaksel nije mutagen u Ames testu ili testu mutacije gena CHO / HGPRT. Ovi su rezultati u skladu s farmakološkom aktivnošću docetaksela.
Neželjeni učinci na muške spolne organe, uočeni u studijama toksičnosti na glodavcima, ukazuju na to da docetaksel može umanjiti plodnost muškaraca.
06.0 FARMACEUTSKE INFORMACIJE
06.1 Pomoćne tvari
Bočica koncentrata:
polisorbat 80, limunska kiselina.
Bočica s otapalom:
95% etanol, voda za injekcije.
06.2 Nekompatibilnost
Lijek se ne smije miješati s drugim proizvodima osim s onima spomenutim u odjeljku 6.6.
06.3 Razdoblje valjanosti
2 godine.
Prethodno pomiješana otopina: prethodno razrijeđena otopina sadrži 10 mg / ml docetaksela i mora se upotrijebiti odmah nakon pripreme, čak i ako je kemijsko-fizička stabilnost ove otopine dokazana tijekom 8 sati ako se čuva na temperaturi od + 2 ° C C i +8 ° C ili na sobnoj temperaturi (ispod 25 ° C).
Otopina za infuziju: Otopinu za infuziju, pohranjenu na sobnoj temperaturi (ispod 25 ° C), treba upotrijebiti u roku od 4 sata.
06.4 Posebne mjere pri skladištenju
Ne čuvati na temperaturi iznad 25 ° C ili ispod 2 ° C.
Čuvati u originalnom pakiranju kako bi se zaštitilo od svjetlosti.
Za uvjete skladištenja razrijeđenog lijeka vidjeti dio 6.3.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
Svaki blister sadrži:
jednu bočicu koncentrata s jednom dozom i jednu bočicu otapala s jednom dozom.
Bočica TAXOTERE 20 mg / 0,5 ml koncentrata za otopinu za infuziju:
7 ml bočica od prozirnog stakla tipa I sa zelenim poklopcem.
Bočica sadrži otopinu docetaksela u 0,5 ml polisorbata 80 i koncentraciju od 40 mg / ml (volumen punjenja: 24,4 mg / 0,61 ml). Ovaj volumen ispune ustanovljen je tijekom razvoja TAXOTERE -a kako bi se nadomjestio gubitak tekućine tijekom pripreme prethodno razrijeđene otopine zbog pjenjenja, prianjanja na stijenke bočice i 'mrtvog prostora'. Prekomjerno punjenje osigurava da nakon razrjeđenja cijelim sadržajem bočice s otapalom zatvorene TAXOTERE -om, minimalni volumen ekstrahirane prethodno razrijeđene otopine je 2 ml, koji sadrži 10 mg / ml docetaksela, što odgovara sadržaju navedenom na naljepnici od 20 mg / 0,5 ml po bočici.
Bočica s otapalom:
Bočica od prozirnog stakla tipa I od 7 ml s bezbojnim prozirnim poklopcem.
Bočica s otapalom sadrži 1,5 ml 13% (w / w) otopine 95% etanola u vodi za injekcije (volumen punjenja: 1,98 ml). Dodavanjem cijelog sadržaja bočice s otapalom sadržaju TAXOTERE 20 mg / 0,5 ml, koncentrat za otopinu za infuziju osigurava dobivanje prethodno miješane otopine s koncentracijom od 10 mg / ml docetaksela.
06.6 Upute za uporabu i rukovanje
TAXOTERE je antineoplastični lijek i, kao i kod drugih potencijalno otrovnih proizvoda, treba biti oprezan pri rukovanju i pripremi otopina. Preporučuje se uporaba rukavica. Ako TAXOTERE u koncentriranom, prethodno razrijeđenom obliku ili otopini za infuziju dođe u dodir s kožom, odmah i temeljito operite sapunom i vodom. Ako TAXOTERE u koncentriranom, prethodno razrijeđenom obliku ili otopini za infuziju ako dođu u dodir sa sluznicom, odmah i temeljito isperite vodom.
Priprema za intravenoznu primjenu
a) Priprema gotove otopine TAXOTERE (10 mg docetaksela / ml)
Ako se bočice čuvaju u hladnjaku, ostavite potreban broj kutija TAXOTERE -a na sobnoj temperaturi (ispod 25 ° C) 5 minuta.
Pomoću graduirane štrcaljke s iglom izvucite cijeli sadržaj bočice s otapalom za TAXOTERE djelomičnim preokretanjem bočice.
Ubrizgajte cijeli sadržaj štrcaljke u odgovarajuću bočicu lijeka TAXOTERE.
Izvadite štrcaljku i iglu i miješajte otopinu ručno obrnutim okretanjem tijekom 45 sekundi. Ne tresti.
Ostavite bočicu s prethodno razrijeđenom otopinom da odstoji 5 minuta na sobnoj temperaturi (ispod 25 ° C), a zatim provjerite je li otopina bistra i homogena. (Pjena je normalna čak i nakon 5 minuta zbog sadržaja polisorbata 80 u formulaciji).
Prethodno razrijeđena otopina sadrži 10 mg / ml docetaksela i mora se upotrijebiti odmah nakon pripreme, čak i ako je kemijsko-fizička stabilnost ove otopine dokazana tijekom 8 sati ako se čuva na temperaturi od + 2 ° C do + 8 ° C ili na sobnoj temperaturi (ispod 25 ° C).
b) Priprema otopine za infuziju
Za dobivanje potrebne doze za pacijente može biti potrebno više bočica s prethodno razrijeđenom otopinom. Na temelju doze potrebne za pacijenta izražene u mg, aseptički izvucite odgovarajući volumen prethodno razrijeđene otopine koja sadrži 10 mg / ml docetaksela iz odgovarajućeg broja bočica s prethodno razrijeđenom otopinom pomoću graduirane štrcaljke s iglom. Na primjer, za dozu od 140 mg docetaksela, potrebno je povući 14 ml prethodno razrijeđene otopine docetaksela. Ubrizgajte potrebni volumen prethodno razrijeđene otopine u vrećicu ili bočicu od 250 ml koja sadrži 5% otopinu glukoze ili otopinu za infuziju s 9 mg / ml natrijevog klorida (0,9%).
Ako je potrebna doza docetaksela veća od 200 mg, upotrijebite veći volumen infuzijske otopine tako da koncentracija docetaksela ne prelazi 0,74 mg / ml. Ručno miješajte vrećicu ili bočicu uvijanjem.
TAXOTERE otopinu za infuziju treba upotrijebiti u roku od 4 sata i primijeniti je kao infuziju od 1 sata, aseptično, na sobnoj temperaturi (ispod 25 ° C) i u normalnim svjetlosnim uvjetima.
Kao i kod svih proizvoda za parenteralnu primjenu, prethodno razrijeđena otopina i perfuzijska otopina TAXOTERE -a moraju se prije uporabe vizualno pregledati, otopine koje sadrže taloge moraju se odbaciti.
Neiskorišteni proizvod i otpad dobiveni iz ovog lijeka moraju se zbrinuti u skladu s lokalnim zakonskim zahtjevima.
07.0 Nositelj odobrenja za stavljanje u promet
Aventis Pharma S.A., 20 Avenue Raymond Aron, 92165 Antony Cedex, Francuska
08.0 BROJ DOZVOLE ZA PROMET
EU/1/95/002/001
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Datum prve autorizacije: 27. studenog 1995. godine
Datum posljednje obnove: 27. studenog 2005.