Aktivni sastojci: Mesalazin (5-ASA)
PENTASA 500 mg tablete s modificiranim otpuštanjem
PENTASA 1 g granula s produljenim oslobađanjem
Ulošci za paket Pentasa dostupni su za veličine pakiranja: - PENTASA 500 mg tablete s modificiranim otpuštanjem, PENTASA 1 g granule s produljenim oslobađanjem
- PENTASA 1 g čepići
- PENTASA 4 g / 100 ml rektalne suspenzije
Indikacije Zašto se koristi Pentasa? Čemu služi?
Pentasa sadrži djelatnu tvar mesalazin, koja pripada skupini lijekova koji se nazivaju salicilati, crijevna protuupalna sredstva koja se koriste za liječenje ulceroznog kolitisa i Crohnove bolesti.
Ulcerozni kolitis je bolest debelog crijeva (debelog crijeva) i rektuma u kojoj unutarnja sluznica crijeva postaje crvena i natečena (upaljena), sa simptomima kao što su učestalo pražnjenje crijeva i krvava stolica, popraćeni grčevima u želucu.
Kada se daje za akutnu epizodu ulceroznog kolitisa, Pentasa djeluje duž cijelog debelog crijeva i rektuma za liječenje upale i smanjenje simptoma. Tablete se također mogu uzeti kako bi se spriječilo vraćanje ulceroznog kolitisa.
U teškoj aktivnoj fazi može biti poželjna povezanost s kortizonskim lijekovima.
Kontraindikacije Kada se Pentasa ne smije koristiti
Nemojte koristiti Pentasa
- ako ste alergični na djelatnu tvar ili bilo koji drugi sastojak ovog lijeka (naveden u odjeljku 6)
- ako ste alergični na klasu lijekova poznatih kao salicilati (npr. aspirin)
- u djece mlađe od 6 godina
- tijekom posljednjih tjedana trudnoće i tijekom dojenja (vidi "Trudnoća, dojenje i plodnost")
- ako imate teške probleme s bubrezima ili jetrom.
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Pentasa
Prije upotrebe Pentase razgovarajte sa svojim liječnikom ili ljekarnikom:
- ako ste alergični na sulfasalazin (alergija na salicilate)
- ako vaša jetra radi slabo ili loše
- ako patite od bubrežnih problema. Mesalazin izaziva nefrotoksičnost (bubrežnu toksičnost), pa se mora prekinuti u bolesnika kod kojih se tijekom liječenja razvije bubrežna disfunkcija.
- ako se liječite lijekovima koji mogu utjecati na rad bubrega, poput nesteroidnih protuupalnih lijekova (NSAID) i azatioprina, jer mogu povećati rizik od bubrežnih reakcija
- ako se liječite azatioprinom ili 6-merkaptopurinom i tiogvaninom jer su to lijekovi koji mogu povećati rizik od krvnih diskrazija (poremećaja krvi). Liječenje treba smanjiti ili prekinuti u prisutnosti ovih nuspojava
- ako imate osobito usporenu probavu želuca ili ste nositelj pilorične stenoze (suženje dijela želuca koji vodi u tanko crijevo)
- ako imate problema s disanjem poput astme.
Posebno tijekom početne faze liječenja, vaš liječnik može zatražiti pretrage urina i krvi kako bi procijenio funkciju vaših bubrega, jetre.
Djeca i adolescenti
Pentasa se ne preporučuje za uporabu u djece mlađe od 6 godina.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak Pentase
Obavijestite svog liječnika ako koristite, nedavno ste koristili ili biste mogli koristiti bilo koje druge lijekove, uključujući i one koji se mogu uzimati bez recepta.
To je osobito važno ako uzimate lijekove kao što su:
- Azatioprin, 6-merkaptopurin i tioguanin (poznati kao "imunosupresivni" lijekovi koji smanjuju aktivnost vašeg imunološkog sustava).
- Kumarinski antikoagulansi (lijekovi koji povećavaju vrijeme potrebno za zgrušavanje krvi). Na primjer, varfarin.
Pentasa s hranom i pićem
Ovaj lijek se može uzimati s hranom i pićem (vidjeti dio 3).
Upozorenja Važno je znati da:
Trudnoća, dojenje i plodnost
Ako ste trudni ili dojite, mislite da ste trudni ili planirate trudnoću, prije upotrebe ovog lijeka obratite se svom liječniku ili ljekarniku za savjet.
Pentasa se mora koristiti s oprezom tijekom trudnoće ili dojenja, i samo ako je to apsolutno potrebno (vidjeti također dio 2 "Nemojte koristiti Pentasa").
Krvni poremećaji uočeni su u dojenčadi majki liječenih Pentasom.
Ne mogu se isključiti alergijske reakcije poput proljeva u novorođenčadi.
Ako dojenče doživi proljev, dojenje treba prekinuti.
Upravljanje vozilima i strojevima
Liječenje lijekom Pentasa obično ne utječe na sposobnost upravljanja vozilima i / ili rada sa strojevima.
Doza, način i vrijeme primjene Kako se koristi Pentasa: Doziranje
Uvijek koristite ovaj lijek točno onako kako vam je rekao vaš liječnik ili ljekarnik. Ako ste u nedoumici, obratite se svom liječniku ili ljekarniku.
Preporučena doza je:
Odrasli:
Kod ulceroznog kolitisa
Akutno liječenje: do 4 g mesalamina jednom dnevno ili podijeljeno u 2-4 primjene
Liječenje održavanja: preporučuje se započeti s 1500 mg mesalamina dnevno, podijeljeno u 3 doze.
Kod Crohnove bolesti
Akutno liječenje: do 3-4 g mesalamina dnevno, podijeljeno u 2-3 primjene.
Liječenje održavanja: preporučuje se započeti s 3 g mesalamina dnevno, podijeljeno u 3 primjene.
Primjena u djece
Djeca od 6 godina starosti
Općenito se preporučuje da se polovica doze za odrasle daje djeci do 40 kg tjelesne težine, a normalna doza za odrasle onima iznad 40 kg tjelesne težine.
- Akutno liječenje: počevši od 30-50 mg / kg / dan u odvojenim davanjima. Maksimalna doza: 75 mg / kg / dan u odvojenim davanjima. Ukupna doza ne smije prelaziti 4 g / dan (maksimalna doza za odrasle).
- Liječenje održavanja: počevši od 15-30 mg / kg / dan u odvojenim davanjima. Ukupna doza ne smije prelaziti 2 g / dan (preporučena doza za odrasle).
Tablete ili vrećice mogu se uzeti tijekom ili neposredno nakon obroka. Pentasa se može uzeti s vodom ili jogurtom. Tablete se mogu progutati cijele, ili se također mogu razbiti ili otopiti u čaši ili žlici s malo vode.
Pentasa tablete ili granule ne smiju se žvakati. Nakon otvaranja vrećice, granule se moraju uzeti u roku od 24 sata (pogledajte "Kako čuvati Pentasa").
Ako ste zaboravili uzeti Pentasu
Ako ste zaboravili uzeti dozu Pentase, uzmite sljedeću redovnu redovnu dozu u uobičajeno vrijeme.
Nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljenu dozu.
Ako prestanete uzimati Pentasu
Vaš će vam liječnik reći koliko će trajati liječenje. Obratite se svom liječniku prije nego što prekinete liječenje ovim lijekom.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku ili ljekarniku.
Predoziranje Što učiniti ako ste uzeli previše Pentase
Ako ste uzeli više tableta ili vrećica nego što ste trebali, odmah se obratite liječniku ili idite u najbližu bolnicu.
Nuspojave Koje su nuspojave Pentase
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih.
Česte nuspojave (mogu se javiti u do 1 na 10 osoba):
- Glavobolja
- Proljev
- Bol u trbuhu
- Mučnina
- Povukao se
- Nadutost (crijevni plinovi)
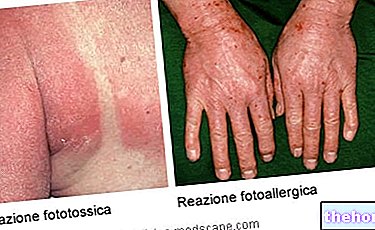
- Osip na koži, poput osipa, eritema.
Rijetke nuspojave (mogu se javiti u do 1 na 1.000 osoba):
- Vrtoglavica
- Mio i perikarditis (upala određenih dijelova srca)
- Akutni pankreatitis (akutna upala gušterače) i povećane amilaze (enzimi gušterače).
Vrlo rijetke nuspojave (mogu se javiti u do 1 na 10 000 osoba):
- Poremećaji krvi, kao što je eozinofilija (povećanje vrste bijelih krvnih zrnaca koja se nazivaju eozinofili), anemija (smanjenje crvenih krvnih zrnaca), aplastična anemija (oblik anemije koju karakterizira nedovoljna proizvodnja krvnih stanica svih vrsta u koštanoj srži) , leukopenija (smanjenje bijelih krvnih stanica), trombocitopenija (smanjenje trombocita), agranulocitoza (smanjenje vrste bijelih krvnih stanica zvanih granulociti), pancitopenija (smanjenje svih krvnih stanica)
- Reakcije preosjetljivosti (alergije) uključujući alergijski osip, anafilaktičku reakciju, reakciju na lijek s eozinofilijom i sistemske simptome (DRESS), multiformni eritem i Steavens-Johnsonov sindrom (SJS)
- Ljekovita groznica
- Periferna neuropatija (patološko stanje koje utječe na živce šaka i stopala)
- Alergijski alveolitis, alergijske reakcije i plućni poremećaji (plućne fibrozne reakcije, uključujući otežano disanje (dispneja), kašalj, bronhospazam, eozinofilna upala pluća, intersticijska bolest pluća, plućna infiltracija, upala pluća)
- Pankolitis (upala debelog crijeva)
- Poremećaji jetre (povećani jetreni enzimi, holestatski indeksi i bilirubin, hepatoksičnost, uključujući hepatitis, kolestatski hepatitis, ciroza, zatajenje jetre)
- Alopecija (gubitak kose ili stanjivanje) je reverzibilna
- Bol u mišićima (mijalgija), bol u zglobovima (artralgija), slučajevi imunoloških reakcija sličnih eritematoznom lupusu
- Poremećaji bubrega (akutni i kronični intersticijski nefritis, nefrotski sindrom, zatajenje bubrega, promjena boje urina)
- Oligospermija (niska koncentracija spermija u sjemenu) reverzibilna.
Neke od nuspojava mogu se pripisati i samoj bolesti.
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku ili ljekarniku.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Također možete prijaviti nuspojave izravno putem nacionalnog sustava za prijavljivanje na www.agenziafarmaco.gov.it/it/responsabili. Izvještavanjem o nuspojavama možete pomoći u pružanju više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece.
Nakon otvaranja vrećica, granule se mogu čuvati 24 sata, nakon čega se moraju baciti.
Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na pakiranju iza "EXP". Datum isteka odnosi se na zadnji dan tog mjeseca. Ovaj datum se odnosi na proizvod u netaknutom pakiranju, pravilno uskladišten.
Nemojte bacati lijekove u otpadne vode ili kućni otpad. Pitajte ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Rok "> Ostale informacije
Što Pentasa sadrži
Tableta s izmijenjenim oslobađanjem:
- Aktivni sastojak je mesalamin
- Pomoćni sastojci su: polivinilpirolidon, etilceluloza, magnezijev stearat, talk, mikrokristalna celuloza.
Vrećica granula s produženim otpuštanjem:
- Aktivni sastojak je mesalamin
- Pomoćni sastojci su: etilceluloza, mikrokristalna celuloza.
Opis izgleda Pentasa i sadržaj pakiranja
Pentasa 500 mg tablete s prilagođenim oslobađanjem: Tablete su predstavljene malim bijelo-sivim do svijetlosmeđim mrljama i razdjelnom crtom. 500 mg je utisnuto s jedne strane, a PENTASA s druge strane.Kutija s 50 tableta.
Vrećice Pentasa 1 g granula s produljenim otpuštanjem: bijelo-sive do bijelo-svijetlosmeđe granule. Pakiranje od 50 vrećica.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA -
PENTASA
02.0 KVALITATIVNI I KOLIČINSKI SASTAV -
Jedna tableta s modificiranim otpuštanjem sadrži: 500 mg mesalamina (5-amino-salicilna kiselina).
Jedna vrećica granula s produljenim oslobađanjem sadrži: mesalazin (5-amino-salicilna kiselina) 1 g.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK -
Tablete s urezanim oslobađanjem, s malim bijelo-sivim do svijetlosmeđim mrljama, razdjelnicom i otiskom: 500 mg s jedne strane, PENTASA s druge strane.
Granule s produljenim otpuštanjem, bijelo-sive do bijelo-svijetlosmeđe boje.
04.0 KLINIČKI PODACI -
04.1 Terapeutske indikacije -
Ulcerozni kolitis. Crohnova bolest.
Pentasa je indicirana i u liječenju aktivne faze bolesti i u sprječavanju recidiva. U teškoj aktivnoj fazi može se preporučiti povezanost s liječenjem kortizonom.
04.2 Doziranje i način primjene -
Doziranje
Doziranje treba prilagoditi pojedinačnom bolesniku ovisno o težini bolesti. Kod ulceroznog kolitisa
Akutno liječenje: do 4 g mesalamina jednom dnevno ili podijeljeno u 2-4 primjene.
Liječenje održavanja: preporučuje se započeti s 1500 mg mesalamina dnevno, podijeljeno u 3 doze.
Kod Crohnove bolesti
Akutno liječenje: do 3-4 g mesalamina dnevno, podijeljeno u 2-3 primjene.
Liječenje održavanja: preporučuje se započeti s 3 g mesalamina dnevno, podijeljeno u 3 primjene.
Pedijatrijska populacija
Postoji samo ograničena dokumentacija o učinku kod djece (6-18 godina) .Djeca od šest godina
Akutno liječenje: mora se odrediti pojedinačno, počevši od 30-50 mg / kg / dan u zasebnim davanjima. Maksimalna doza: 75 mg / kg / dan u odvojenim davanjima. Ukupna doza ne smije prelaziti 4 g / dan (maksimalna doza za odrasle).
Liječenje održavanja: mora se odrediti pojedinačno, počevši od 15-30 mg / kg / dan u odvojenim davanjima. Ukupna doza ne smije prelaziti 2 g / dan (preporučena doza za odrasle).
Općenito se preporučuje da se polovica doze za odrasle daje djeci do 40 kg tjelesne težine, a normalna doza za odrasle onima iznad 40 kg tjelesne težine.
Način primjene
Pentasa tablete ili granule ne smiju se žvakati.
Tablete ili vrećice mogu se uzeti tijekom ili neposredno nakon obroka. Također možete razbiti tablete ili ih pustiti da se raspadnu u čaši ili na žlici s vodom. Pentasa se može uzeti s vodom ili jogurtom.
04.3 Kontraindikacije -
Preosjetljivost na djelatnu tvar, salicilate ili neku od pomoćnih tvari navedenih u dijelu 6.1.
Djeca mlađa od 6 godina.
Posljednji tjedni trudnoće i dojenja (vidjeti dio 4.6). Teška bubrežna ili jetrena insuficijencija.
04.4 Posebna upozorenja i mjere opreza pri uporabi -
Relapsi objektivnih i subjektivnih simptoma mogu se pojaviti i nakon prekida terapije i tijekom neodgovarajućeg održavanja. Moguća pojava reakcija preosjetljivosti uključuje trenutnu obustavu terapije. U pacijenata koji imaju usporenu probavu ili su nositelji pilorične stenoze, ponekad može biti moguće oslobađanje 5-ASA već u želucu, s posljedičnom iritacijom želuca i gubitkom učinkovitosti lijeka.
Pentasa se mora koristiti s oprezom u bolesnika alergičnih na sulfasalazin (rizik od alergije na salicilate). U slučaju reakcija akutne netolerancije, poput grčeva u trbuhu, akutne boli u trbuhu, vrućice, jake glavobolje i osipa, liječenje treba odmah prekinuti.
Savjetuje se oprez u bolesnika s oštećenom funkcijom jetre. Parametre funkcije jetre, kao što su ALT ili AST, treba procijeniti na početku i tijekom liječenja, prema procjeni liječnika.
Primjena Pentase ne preporučuje se u bolesnika s bubrežnim poremećajima. Potrebno je redovito kontrolirati funkciju bubrega (npr. Serumski kreatinin), osobito tijekom početne faze liječenja. Mesalazin izaziva nefrotoksičnost, stoga ga treba prekinuti u bolesnika kod kojih se tijekom liječenja razvije bubrežna disfunkcija U slučaju istodobne primjene drugih nefrotoksičnih lijekova, poput NSAID -a i azatioprina, potrebno je povećati učestalost praćenja bubrežne funkcije.
Bolesnike s plućnim bolestima, osobito astmom, potrebno je pomno pratiti tijekom liječenja.
Rijetko su prijavljene reakcije preosjetljivosti srca na mesalamin (moj i perikarditis) i vrlo rijetko teške krvne diskrazije. Na početku i tijekom liječenja, prema procjeni liječnika, preporučuju se krvni testovi za diferencijalnu krvnu sliku. Istodobno liječenje mesalaminom može povećati rizik od krvne diskrazije u bolesnika koji primaju azatioprin ili 6-merkaptopurin ili tiogvanin. (Vidjeti dio 4.5) Liječenje treba prekinuti ako se sumnja ili se jave ove nuspojave.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija -
Istodobna terapija PENTASA-om i azatioprinom ili 6-merkaptopurinom ili tiogvaninom pokazala je veću učestalost mijelosupresivnih učinaka u nekoliko studija, pa iako mehanizam interakcije nije u potpunosti uspostavljen, čini se da postoji korelacija. Preporučuje se redovito praćenje. Bijelih krvnih stanica a dozu tiopurina treba prilagoditi u skladu s tim.
Mesalamin može smanjiti antikoagulantni učinak varfarina.
04.6 Trudnoća i dojenje -
Pentasa se mora koristiti s oprezom tijekom trudnoće ili dojenja i samo ako potencijalne koristi premašuju, prema procjeni liječnika, moguće rizike. Mesalazin prelazi placentnu barijeru i njegova koncentracija u plazmi pupkovine je niža od one u majčinoj plazmi Metabolit acetil-mesalazina nađen je u sličnim koncentracijama u plazmi pupkovine i majčine vrpce. U nekoliko promatračkih studija nisu zabilježeni teratogeni učinci i nema dokaza o značajnom riziku u ljudskoj uporabi. Ispitivanja na životinjama s oralnim mesalazinom nisu pokazala izravne ili neizravne štetne učinke na trudnoću, razvoj embrija i fetusa, porođaj ili postnatalni razvoj. Krvni poremećaji (pancitopenija, leukopenija, trombocitopenija, anemija) prijavljeni su u novorođenčadi majki liječenih lijekom Pentasa.
Mesalamin se izlučuje u majčino mlijeko. Koncentracija mesalamina u majčinom mlijeku niža je nego u majčinoj krvi, dok je metabolit, acetil-mesalazin, u sličnim ili većim koncentracijama. Postoji "ograničeno iskustvo" oralne primjene mesalamina u žena koje doje. Nisu provedena kontrolirana ispitivanja s lijekom Pentasa tijekom dojenja. Reakcije preosjetljivosti, poput proljeva u novorođenčadi, ne mogu se isključiti. Ako dojenče doživi proljev, dojenje treba prekinuti.
Ispitivanja mesalamina na životinjama nisu pokazala utjecaj na plodnost muškaraca i žena.
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima -
Nije vjerojatno da će liječenje lijekom Pentasa utjecati na sposobnost upravljanja vozilima i / ili rada sa strojevima.
04.8 Nuspojave -
Nuspojave su navedene u nastavku prema organu, organu / sustavu i učestalosti MedDRA -e. Učestalosti su definirane kao: vrlo česte (1/10) uobičajene (≥ 1/100 a
Učestalost nuspojava na temelju kliničkih ispitivanja i izvješća o praćenju nakon stavljanja na tržište
(*) mehanizam kojim mesalazin izaziva mio- i perikarditis, pankreatitis, nefritis i hepatitis nije poznat, ali je vjerojatno alergijske prirode.
Važno je napomenuti da se mnoge nuspojave mogu pripisati i samom IBD -u.
Prijavljivanje sumnji na nuspojave.
Izvještavanje o sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijave sve sumnje na nuspojave putem nacionalnog sustava za prijavljivanje. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Predoziranje -
Akutno iskustvo kod životinja:
Oralne doze mesalamina do 5 g / kg u svinja ili pojedinačne intravenozne doze mesalazina do 920 mg / kg u štakora nisu bile smrtonosne.
Iskustvo kod čovjeka:
Ograničeno kliničko iskustvo s predoziranjem ne ukazuje na bubrežnu ili jetrenu toksičnost. Specifični protuotrov nije poznat, a liječenje je simptomatsko i podržava. Liječenje predoziranja kod ljudi:
Simptomatsko liječenje u bolničkom okruženju. Pažljivo praćenje bubrežne funkcije.
05.0 FARMAKOLOŠKA SVOJSTVA -
05.1 "Farmakodinamička svojstva -
Farmakoterapijska skupina: crijevna protuupalna sredstva, amino salicilna kiselina i analozi.
ATC: A07EC02.
Utvrđeno je da je mesalamin aktivni sastojak sulfasalazina koji se koristi za liječenje ulceroznog kolitisa, Crohnove bolesti i proktitisa.
Kliničke studije pokazuju da se čini da je terapijska vrijednost mesalazina, nakon oralne ili rektalne primjene, posljedica lokalnog učinka na upaljenu crijevnu sluznicu, a ne sustavnog.
Prisutni bolesnici s IBD -om: povećana migracija leukocita, abnormalna proizvodnja citokina, povećana proizvodnja metabolita arahidonske kiseline, osobito leukotriena B4, te povećano stvaranje slobodnih radikala u upaljenoj crijevnoj sluznici. učinak koji inhibira kemotaksiju leukocita, smanjuje proizvodnju citokina i leukotriena te neutralizira slobodne radikale.Trenutno nije poznato koji od ovih mehanizama ima dominantnu ulogu u kliničkoj učinkovitosti mesalazina.
05.2 "Farmakokinetička svojstva -
Lokalna dostupnost: terapijska aktivnost mesalazina najvjerojatnije ovisi o lokalnom kontaktu lijeka s oboljelim područjem sluznice crijeva.
Vrećice i tablete s modificiranim otpuštanjem Pentasa sastoje se od mikrogranula mezalamina obloženih etilcelulozom. Nakon primjene i raspadanja tableta, mesalazin se kontinuirano oslobađa iz pojedinih mikrogranula u cijelom gastrointestinalnom traktu pri različitim enteralnim pH uvjetima.
Mikrogranule stižu u duodenum unutar jednog sata nakon primjene, bez obzira na istovremeni unos hrane. Prosječna brzina tranzita u tankom crijevu je približno 3-4 sata kod zdravih dobrovoljaca.
Apsorpcija
Na temelju podataka o urinu zdravih dobrovoljaca, nakon oralne primjene apsorbira se 30-50% unesene doze, pretežno u tanko crijevo.
Mesalazin se može otkriti u plazmi već 15 minuta nakon primjene. Maksimalna koncentracija u plazmi postiže se nakon 1-4 sata. Nakon postupnog smanjenja, mesalamin se više neće moći otkriti 12 sati nakon primjene. Krivulja koncentracije u plazmi za acetil mesalazin slijedi isti obrazac, ali su koncentracije općenito veće i eliminacija je sporija.
Metabolički omjer acetil-mesalazina i mesalamina u plazmi nakon oralne primjene kreće se od 3,5 do 1,3 nakon dnevnih doza od 500 mg x3 odnosno 2 g x3, što implicira doziranje ovisnu acetilaciju koja može biti podložna zasićenju.
Stacionarne koncentracije mesalamina u plazmi su približno 2 μmol / L, 8 μmol / L i 12 μmol / L nakon dnevnih doza od 1,5 g, 4 g odnosno 6 g. Za acetil mesalazin odgovarajuće koncentracije su 6 mcmol / l, 13 mcmol / l i 16 mcmol / l.
Distribucija
Mesalazin se veže za proteine plazme za oko 50%, acetil-mesalazin za oko 80%. 5-ASA i Ac-5-ASA ne prelaze krvno-moždanu barijeru.
Biotransformacija
Mesalazin se presistemski crijevnom sluznicom i sistemski u jetri metabolizira u N-acetil-mesalazin (acetilmesalazin). Do dijela acetilacije dolazi i bakterijska flora debelog crijeva. Čini se da acetilacija nije ovisna o pacijentovom fenotipu acetilatora.
Smatra se da je acetil mesalazin klinički i toksikološki neaktivan, no to još nije potvrđeno.
Uklanjanje
Poluvrijeme eliminacije mesalamina u plazmi je oko 40 minuta, a acetil-mesalazina oko 70 minuta. Zbog kontinuiranog oslobađanja PENTASA-e u cijelom gastrointestinalnom traktu, poluvrijeme eliminacije mesalazina ne može se odrediti nakon oralne primjene, no ravnotežno stanje postiže se nakon razdoblja liječenja od 5 dana nakon oralne primjene.
Obje tvari izlučuju se urinom i stolicom.
Izlučivanje mokraćom uglavnom se sastoji od acetil mesalazina.
U bolesnika s oštećenom funkcijom jetre ili bubrega, smanjenje stope eliminacije i povećanje sistemske koncentracije mesalazina mogu predstavljati povećani rizik od štetnih nefrotoksičnih reakcija.
05.3 Pretklinički sigurnosni podaci -
Siguran otrovni učinak na bubreg dokazan je kod svih vrsta. Općenito, toksične doze premašuju one koje se koriste u ljudi 5-10 puta.
U životinja nije zabilježena značajna toksičnost povezana s gastrointestinalnim traktom, jetrom ili hematopoetskim sustavom.
Test in vitro i studija in-vivo nisu pokazali mutagene i klastogene učinke. Studije o kancerogenom potencijalu provedene na miševima i štakorima nisu pokazale povećanje učestalosti tumora povezanih sa supstancom.
Ispitivanja na životinjama s oralnim mesalazinom nisu pokazala izravne ili neizravne štetne učinke na plodnost, trudnoću, embrio-fetalni razvoj, porod ili postnatalni razvoj.
06.0 FARMACEUTSKE INFORMACIJE -
06.1 Pomoćne tvari -
Tablete: polivinilpirolidon, etilceluloza, magnezijev stearat, talk, mikrokristalna celuloza.
Vrećice: etil celuloza, mikrokristalna celuloza.
06.2 Inkompatibilnost "-
Nije bitno.
06.3 Rok valjanosti "-
Tablete s promijenjenim oslobađanjem: 3 godine.
Granule s produljenim oslobađanjem: 2 godine. Nakon otvaranja vrećica,
granulat je stabilan 24 sata.
06.4 Posebne mjere pri skladištenju -
Ovaj lijek ne zahtijeva nikakve posebne uvjete skladištenja.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja -
Tablete s promijenjenim otpuštanjem:
Pakiranje od 50 tableta (5 blistera aluminij / poliamid-aluminij-polivinil klorid).
Granule s produljenim otpuštanjem:
Pakiranje od 50 vrećica granula. Granule se nalaze u aluminijskim vrećicama.
06.6 Upute za uporabu i rukovanje -
Nema posebnih uputa.
Neiskorišteni lijekovi i otpad nastali iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 NOSITELJ "Odobrenja za stavljanje u promet" -
Ferring S.p.A. - Via Senigallia 18/2 - 20161 MILAN
08.0 BROJ DOZVOLE ZA PROMET -
500 mg tablete s modificiranim otpuštanjem, 50 tableta: 027130071
1 g granula s produljenim otpuštanjem, 50 vrećica: 027130083
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA -
Vrećice Pentasa 1 g:
Registracija 22. listopada 1998. - Obnova ovlaštenja Lipanj 2010