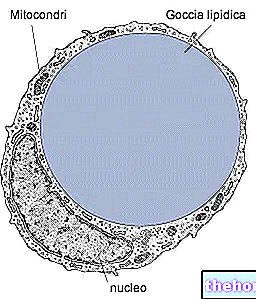
Definicija
Enzimi su proteini proizvedeni u biljnim i životinjskim stanicama, koji djeluju kao katalizatori koji ubrzavaju biološke reakcije bez promjene.
Enzimi djeluju kombinirajući se sa određenom tvari pretvarajući je u drugu tvar; klasični primjeri dati su probavnim enzimima prisutnim u slini, želucu, gušterači i tankom crijevu, koji obavljaju bitnu funkciju u probavi i pomažu razgradnju hrane na osnovne sastojke, koje tijelo zatim može apsorbirati i koristiti, obrađujući ih drugim enzimima ili izlučuju kao otpad.
Svaki enzim ima posebnu ulogu: onaj koji razgrađuje masti, na primjer, ne djeluje na proteine ili ugljikohidrate. Enzimi su bitni za dobrobit organizma. Nedostatak, čak i jednog enzima, može uzrokovati ozbiljne poremećaje. Poznati primjer je fenilketonurija (PKU), bolest koju karakterizira nemogućnost metabolizma esencijalne aminokiseline, fenilalanin čija akumulacija može uzrokovati tjelesne deformitete i duševne bolesti.
Biokemijska studija
Enzimi su posebni proteini koji imaju karakteristiku da su biološki katalizatori, odnosno imaju sposobnost razgradnje energije aktivacije (Eatt) reakcije, mijenjajući njezin put tako da je kinetički spor proces brži.
Enzimi povećavaju kinetiku termodinamički mogućih reakcija i, za razliku od katalizatora, manje -više su specifični: stoga posjeduju specifičnost supstrata.
Enzim nije uključen u stehiometriju reakcije: da bi se to dogodilo, konačno katalitičko mjesto mora biti identično početnom.
U katalitičkom djelovanju gotovo uvijek postoji spora faza koja određuje brzinu procesa.
Kada govorimo o enzimima nije ispravno govoriti o ravnotežnim reakcijama, umjesto toga govorimo o stacionarno stanje (stanje u kojem se određeni metabolit stvara i kontinuirano troši, održavajući njegovu koncentraciju gotovo konstantnom tijekom vremena). Produkt reakcije koju katalizira jedan enzim obično je sam po sebi reaktant za sljedeću reakciju, kataliziran drugim enzimom itd.
Procesi katalizirani enzimima obično se sastoje od niza reakcija.
Generička reakcija koju katalizira enzim (E) može se sažeti na sljedeći način:

E je enzim
S je podloga;
ES predstavlja adukt između enzima i supstrata;
P je proizvod;
K je konstanta brzine reakcije.
Generički enzim (E) u kombinaciji sa supstratom (S) tvori adukt (ES) s konstantom brzine K1; može se disocirati natrag u E + S, s konstantom brzine K2, ili, (ako "živi" dovoljno dugo ) može prijeći u oblik P s konstantom brzine K3.
Proizvod (P) se, pak, može rekombinirati s enzimom i reformirati adukt s konstantom brzine K4.
Kad se enzim i supstrat pomiješaju, postoji djelić vremena u kojem se susret između dvije vrste još nije dogodio: to jest, postoji izuzetno kratak vremenski interval (koji ovisi o reakciji) u kojem enzim i supstrat imaju još nije ispunjen; nakon tog razdoblja enzim i supstrat dolaze u kontakt u sve većim količinama i nastaje ES adukt. Nakon toga, enzim djeluje na supstrat i proizvod se oslobađa. Tada se može reći da je c "početni vremenski interval u kojem se koncentracija ES adukta ne može definirati; nakon tog razdoblja, pretpostavlja se da je stacionarno stanje je utvrđeno, odnosno, brzina procesa koji dovode do dobivanja adukta jednaka je brzini procesa koji dovode do uništenja adukta.
Michaelis-Mentenova konstanta (KM) je konstanta ravnoteže (upućuje na prvu gore opisanu ravnotežu); može se reći, s dobrom aproksimacijom (jer treba uzeti u obzir i K3), da je KM predstavljen omjerom između kinetičkih konstanti K2 i K1 (odnosi se na uništavanje i stvaranje ES adukta u prvoj gore opisanoj ravnoteži) .
Kroz Michaelis-Mentenovu konstantu imamo "naznaku afiniteta između enzima i supstrata: ako je KM mala c" je "visok afinitet između enzima i supstrata, tada je adukt ES stabilan.
Enzimi su podložni regulaciji (ili modulaciji).
U prošlosti se uglavnom govorilo o negativnoj modulaciji, odnosno inhibiciji katalitičkih sposobnosti enzima, ali može postojati i pozitivna modulacija, odnosno postoje vrste sposobne pojačati katalitičke sposobnosti enzima.
Postoje 4 vrste inhibicija (dobivene iz aproksimacija na modelu radi usklađivanja eksperimentalnih podataka s matematičkim jednadžbama):
- konkurentna inhibicija
- nekonkurentna inhibicija
- nekonkurentna inhibicija
- kompetitivna inhibicija
O konkurentnoj inhibiciji govorimo kada je molekula (inhibitor) sposobna natjecati se sa supstratom. Zbog strukturne sličnosti, inhibitor može reagirati umjesto supstrata, otuda i terminologija "kompetitivna inhibicija". Vjerojatnost da se enzim veže za inhibitor ili supstrat ovisi o koncentraciji oba i njihovom afinitetu s enzimom; brzina reakcije stoga ovisi o tim čimbenicima.
Za postizanje iste brzine reakcije kao i bez prisutnosti inhibitora, potrebno je imati veću koncentraciju supstrata.
Eksperimentalno je pokazano da se u prisutnosti inhibitora Michaelis-Mentenova konstanta povećava.
Umjesto toga, "nekonkurentna inhibicija, interakcija između molekule koja bi trebala djelovati kao modulator (pozitivni ili negativni inhibitor) i" enzima "odvija se na mjestu koje je različito od onog na kojem je interakcija javlja se između enzima i supstrata; stoga govorimo o alosteričnoj modulaciji (iz grč allosteros → drugo mjesto).
Ako se inhibitor veže za enzim, može izazvati promjenu strukture enzima i posljedično može smanjiti učinkovitost kojom se supstrat veže za enzim.
U ovoj vrsti procesa Michaelis-Mentenova konstanta ostaje konstantna jer ta vrijednost ovisi o ravnoteži između enzima i supstrata, pa se čak i u prisutnosti inhibitora te ravnoteže ne mijenjaju.
Pojava nekonkurentne inhibicije je rijetka; Tipičan nekompetitivan inhibitor je tvar koja se reverzibilno veže na ES adukt uzrokujući ESI:

Inhibicija viška supstrata ponekad može biti nekonkurentna, jer se to događa kada se druga molekula supstrata veže za ES kompleks, čime nastaje ESS kompleks.
S druge strane, akompeticijski inhibitor može se vezati samo za supstratski enzimski adukt kao u prethodnom slučaju: vezanje supstrata za slobodni enzim inducira konformacijsku modifikaciju koja čini mjesto dostupnim za inhibitor.
Michaelis Mentenova konstanta opada s povećanjem koncentracije inhibitora: očito se stoga povećava afinitet enzima za supstrat.
Serinska proteaza
Oni su obitelj enzima kojima pripadaju kimotripsin i tripsin.
Kimotripsin je proteolitički i hidrolitički enzim koji siječe desno od hidrofobnih i aromatskih aminokiselina.
Produkt gena koji kodira kimotripsin nije aktivan (aktivira se naredbom); neaktivni oblik kimotripsina predstavljen je polipeptidnim lancem od 245 aminokiselina. Kimotripsin ima kuglasti oblik zbog pet disulfidnih mostova i drugih manjih interakcija (elektrostatičke, Van der Waalsove sile, vodikove veze itd.).
Kimotripsin stvaraju kimozne stanice gušterače gdje se nalaze u posebnim membranama i izbacuju kroz kanal gušterače u crijeva, u vrijeme probave hrane: kimotripsin je zapravo probavni enzim. Proteini i hranjive tvari koje unosimo hranom podvrgavaju se probavi kako bi se reducirali na manje lance te apsorbirali i pretvorili u energiju (npr. Amilaze i proteaze razgrađuju hranjive tvari u glukozu i aminokiseline koje do krvnih žila dospijevaju u stanice dopiru do portalne vene i odatle se prenose u jetru gdje se podvrgavaju daljnjem liječenju).
Enzimi se proizvode u neaktivnom obliku i aktiviraju se tek kad dođu do "mjesta na kojem moraju djelovati"; nakon što njihova radnja završi, deaktiviraju se. Enzim, nakon što se deaktivira, ne može se reaktivirati: da bi imao "daljnje katalitičko djelovanje, mora se zamijeniti" drugom molekulom enzima. Kad bi se himitripsin već u gušterači proizvodio u aktivnom obliku, on bi napao potonji: pankreatitis su patologije uzrokovane probavnim enzimima koji su već aktivirani u gušterači (a ne na potrebnim mjestima); neki od njih ako se ne liječe na vrijeme, dovesti do smrti.
U kimotripsinu i u svim serinskim proteazama katalitičko djelovanje je posljedica postojanja alkoholnog aniona (-CH2O-) u bočnom lancu serina.
Serinske proteaze preuzimaju ovo ime upravo zato što je njihovo katalitičko djelovanje posljedica serina.
Nakon što je cijeli enzim izvršio svoje djelovanje, prije nego što može ponovno djelovati na podlozi, mora se obnoviti vodom; "oslobađanje" serina vodom je najsporija faza procesa, a to je ta faza koji određuje brzinu katalize.
Katalitičko djelovanje odvija se u dvije faze:
- stvaranje aniona s katalitičkim svojstvima (anionski alkohol) i naknadni nukleofilni napad na karbonilni ugljik (C = O) s cijepanjem peptidne veze i stvaranjem estera;
- vodeni napad s obnavljanjem katalizatora (sposoban ponovno pokazati svoje katalitičko djelovanje).
Različiti enzimi koji pripadaju obitelji serinskih proteaza mogu se sastojati od različitih aminokiselina, ali za sve njih katalitičko mjesto predstavlja alkoholni anion bočnog lanca serina.
Podporodica serinskih proteaza je ona enzima uključenih u koagulaciju (koja se sastoji u transformaciji proteina, iz njihovog neaktivnog oblika u "drugi oblik koji je aktivan"). Ovi enzimi osiguravaju da je koagulacija što učinkovitija i ograničena u prostor i vrijeme (koagulacija se mora dogoditi brzo i mora se dogoditi samo u blizini ozlijeđenog područja) .Enzimi uključeni u koagulaciju aktiviraju se kaskadno (aktivacijom jednog enzima dobivaju se milijarde enzima: svaki aktivirani enzim , zauzvrat aktivira mnoge druge enzime).
Tromboza je patologija uzrokovana neispravnim djelovanjem enzima koagulacije: uzrokovana je aktivacijom, bez potrebe (jer nema ozljeda), enzima koji se koriste u koagulaciji.
Postoje modulirajući (regulatorni) enzimi i inhibitorni enzimi za druge enzime: u interakciji s potonjima reguliraju ili inhibiraju njihovu aktivnost; čak i produkt enzima može biti inhibitor enzima.Ima i enzima koji djeluju što je supstrat veći.
Lizozim
Luigi Pasteur je kihanjem na petrijevu zdjelicu otkrio da u sluzi postoji enzim sposoban ubiti bakterije: lizocim; sa grčkog: liso = koje veličine; zimo = enzim.
Lizozim je sposoban razbiti staničnu stijenku bakterija. Bakterije i jednostanični organizmi općenito trebaju mehanički otporne strukture koje ograničavaju njihov oblik; unutar bakterija postoji vrlo visok osmotski tlak pa privlače vodu. Plazma membrana bi eksplodirala da nema stanične stijenke koja se protivi ulasku vode i ograničava volumen bakterije.
Stanična stijenka sastoji se od polisaharidnog lanca u kojem se izmjenjuju molekule N-acetil-glukozamina (NAG) i molekule N-acetil-muraminske kiseline (NAM); veza između NAG -a i NAM -a se prekida hidrolizom. Karboksilna skupina NAM -a, u staničnoj stijenci, uključena je u peptidnu vezu s aminokiselinom.
Između različitih lanaca stvaraju se mostovi koji se sastoje od pseudo-peptidnih veza: grananje je posljedica molekule lizina; struktura je u cjelini vrlo razgranata i to joj daje visoku stabilnost.
Lizozim je antibiotik (ubija bakterije): djeluje tako da napravi pukotinu u stijenci bakterije; kada se ova struktura (koja je mehanički otporna) slomi, bakterija izvlači vodu sve dok ne pukne. Lizozim uspijeva razbiti β-1,4 glukozidnu vezu između NAM i NAG.
Katalitičko mjesto lizozima predstavljeno je žlijebom koji prolazi duž enzima u koji je umetnut polisaharidni lanac: šest žlijezda glukozida lanca smješteno je u utor.
U položaju tri utora c "nalazi se prigušnica: u ovom položaju može se postaviti samo jedan NAG jer NAM, koji je većih dimenzija, ne može ući. Stvarno katalitičko mjesto nalazi se između položaja četiri i pet: budući da postoji NAG u položaju tri, rez će se odvijati između NAM -a i NAG -a (a ne obrnuto); rez je, prema tome, specifičan.
Optimalni pH za djelovanje lizozima je pet. Na katalitičkom mjestu enzima, tj. Između položaja četiri i pet, postoje bočni lanci asparaginske kiseline i glutaminske kiseline.
Stupanj homologije: mjeri srodstvo (tj. Sličnost) između proteinskih struktura.
Postoji snažna veza između lizozima i laktoza-sintaze.
Laktoza sintetaza sintetizira laktozu (koja je glavni mliječni šećer): laktoza je galaktozil glukozid u kojem je c "β-1,4 glukozidna veza između galaktoze i glukoze.
Stoga, laktoza sintetaza katalizira reakciju suprotnu onoj koju katalizira lizozim (koji umjesto toga cijepa β-1,4 glukozidnu vezu)
Laktoza sintetaza je dimer, odnosno sastoji se od dva proteinska lanca, od kojih jedan ima katalitička svojstva i usporediv je s lizozimom, a drugi je regulatorna podjedinica.
Tijekom trudnoće, stanice mliječne žlijezde sintetiziraju glikoproteine djelovanjem galatozil-transferaze (ima "homologiju sekvence od 40% s lizozimom): ovaj enzim je u stanju prenijeti galaktozil skupinu iz visokoenergetske strukture u struktura glikoproteina. Tijekom trudnoće inducira se ekspresija gena koji kodira galaktozil-transferazu (postoji i ekspresija drugih gena koji također daju druge proizvode): dolazi do povećanja veličine dojke jer se aktivira mliječna žlijezda (prethodno neaktivna) koja mora proizvoditi mlijeko. Tijekom poroda proizvodi se α-laktalbumin koji je regulatorni protein: u stanju je regulirati katalitički kapacitet galaktozil-transferaze (diskriminacijom supstrata). Galaktozil-transferaza modificirana α-laktalalbuminom može prenijeti galaktozil na molekulu glukoze: tvoreći β-1,4 glikozidnu vezu i dajući laktozu (laktoza sintetazu).
Dakle, galaktoza transferaza priprema mliječnu žlijezdu prije poroda i proizvodi mlijeko nakon poroda.
Za proizvodnju glikoproteina, galaktozil transferaza se veže za galaktozil i NAG; tijekom poroda laktalni albumin veže se za galaktoziltransferazu čineći da potonji prepozna glukozu i više ne NAG da daje laktozu.