Što je Telmisartan Teva Pharma?
Telmisartan Teva Pharma je lijek koji sadrži djelatnu tvar telmisartan. Dostupan je u obliku tableta (20 mg, 40 mg i 80 mg).
Telmisartan Teva Pharma je 'generički lijek'. To znači da je Telmisartan Teva Pharma sličan „referentnom lijeku“ koji je već odobren u Europskoj uniji (EU), a zove se Micardis.
Za što se koristi Telmisartan Teva Pharma?
Telmisartan Teva Pharma je indiciran za liječenje esencijalne hipertenzije (visokog krvnog tlaka) u odraslih.Izraz "esencijalno" znači da hipertenzija nema očitog uzroka.
Lijek se može nabaviti samo na recept.
Kako se koristi Telmisartan Teva Pharma?
Preporučena doza lijeka Telmisartan Teva Pharma je 40 mg jednom dnevno, no nekim pacijentima može koristiti i doza od 20 mg. Ako željeni krvni tlak nije postignut, doza se može povećati na 80 mg ili se može dodati drugi lijek za hipertenziju.
Kako djeluje Telmisartan Teva Pharma?
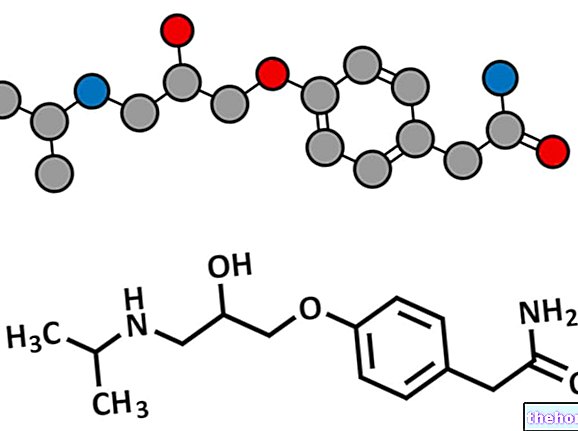
Djelatna tvar u lijeku Telmisartan Teva Pharma, telmisartan, "antagonist je receptora angiotenzina II", što znači da blokira djelovanje hormona u tijelu koji se naziva angiotenzin II. Angiotenzin II je snažan vazokonstriktor (tvar koja sužava krvne žile) . Blokirajući receptore na koje se angiotenzin II normalno veže, telmisartan sprječava rad hormona dopuštajući proširenje krvnih žila, što rezultira padom krvnog tlaka i smanjuje rizik povezan s visokim krvnim tlakom.
Kako je ispitivano Telmisartan Teva Pharma?
Budući da je Telmisartan Teva Pharma generički lijek, studije kod pacijenata bile su ograničene na testove za utvrđivanje njegove bioekvivalencije s referentnim lijekom Micardis. Dva lijeka su bioekvivalentna kada proizvode istu razinu aktivne tvari u tijelu.
Koje su prednosti i rizici Telmisartan Teve?
Budući da je Telmisartan Teva Pharma generički lijek i da je bioekvivalentan referentnom lijeku, smatra se da su njegove koristi i rizici isti kao i kod referentnog lijeka.
Zašto je Telmisartan Teva Pharma odobren?
CHMP je zaključio da se, u skladu sa zahtjevima EU, pokazalo da Telmisartan Teva Pharma ima usporedivu kvalitetu i da je bioekvivalentna Micardisu. Stoga je CHMP smatrao da, kao u slučaju Micardisa, koristi nadmašuju identificirane rizike. I preporučio izdavanje odobrenja za stavljanje u promet lijeka Telmisartan Teva Pharma.
Više informacija o Telmisartan Teva Pharma
Dana 3. listopada 2011. Europska komisija izdala je „Odobrenje za stavljanje lijeka u promet“ za Telmisartan Teva Pharma, važeće na području cijele Europske unije.
Za više informacija o terapiji lijekom Telmisartan Teva Pharma pročitajte upute za uporabu (uključene u EPAR) ili se obratite svom liječniku ili ljekarniku.
Puna verzija EPAR -a referentnog lijeka također se može pronaći na web stranici Agencije.
Posljednje ažuriranje ovog sažetka: 08-2011.
Podaci o lijeku Telmisartan Teva Pharma objavljeni na ovoj stranici mogu biti zastarjeli ili nepotpuni. Za ispravnu uporabu ovih informacija pogledajte stranicu Odricanje od odgovornosti i korisne informacije.