Aktivni sastojci: Golimumab
Simponi 50 mg otopina za injekciju u napunjenoj olovci
Ulošci za paket Simponi dostupni su za veličine pakiranja:- Simponi 50 mg otopina za injekciju u napunjenoj olovci
- Simponi 100 mg otopina za injekciju u napunjenoj olovci
Indikacije Zašto se koristi Simponi? Čemu služi?
Simponi sadrži djelatnu tvar zvanu golimumab.
Simponi pripada skupini lijekova koji se nazivaju „TNF blokatori“. Koristi se kod odraslih za liječenje sljedećih upalnih bolesti:
- Reumatoidni artritis
- Psorijatični artritis
- Aksijalni spondiloartritis, uključujući ankilozirajući spondilitis i neradiografski aksijalni spondiloartritis
- Ulcerozni kolitis
U djece tjelesne težine najmanje 40 kg, Simponi se koristi za liječenje poliartikularnog juvenilnog idiopatskog artritisa.
Simponi djeluje tako što blokira djelovanje proteina koji se naziva "faktor tumorske nekroze alfa" (TNF-α). Ovaj protein je uključen u upalne procese u tijelu i blokirajući ga, moguće je smanjiti upalu u tijelu.
Reumatoidni artritis
Reumatoidni artritis je upalna bolest zglobova. Ako imate aktivni reumatoidni artritis, u početku ćete se liječiti drugim lijekovima. Ako ne reagirate adekvatno na ove lijekove, liječit ćete se Simponijem u kombinaciji s drugim lijekom koji se naziva metotreksat:
- Smanjite znakove i simptome bolesti.
- Usporite oštećenja kostiju i zglobova.
- Poboljšajte tjelesne funkcije.
Psorijatični artritis
Psoriatični artritis je upalna bolest zglobova, obično praćena psorijazom, upalnom kožnom bolesti. Ako imate aktivan psorijatični artritis, prvo ćete se liječiti drugim lijekovima. Ako ne reagirate adekvatno na ove lijekove, bit ćete liječeni lijekom Simponi za:
- Smanjite znakove i simptome bolesti.
- Usporite oštećenja kostiju i zglobova.
- Poboljšajte tjelesne funkcije.
Ankilozirajući spondilitis i neradiografski aksijalni spondiloartritis
Ankilozirajući spondilitis i neradiografski aksijalni spondiloartritis upalne su bolesti kralježnice. Ako imate ankilozirajući spondilitis ili neradiografski aksijalni spondiloartritis, prvo ćete se liječiti drugim lijekovima. Ako ne reagirate adekvatno na ove lijekove, liječit ćete se Simponijem za:
- Smanjite znakove i simptome bolesti.
- Poboljšajte tjelesne funkcije.
Ulcerozni kolitis
Ulcerozni kolitis je upalna bolest crijeva. Ako imate ulcerozni kolitis, prvo ćete dobiti druge lijekove. Ako ne reagirate adekvatno na ove lijekove, dobit ćete Simponi za liječenje vaše bolesti.
Poliartikularni juvenilni idiopatski artritis
Poliartikularni juvenilni idiopatski artritis upalna je bolest koja uzrokuje bolove i otekline u zglobovima kod djece. Ako vaše dijete ima poliartikularni juvenilni idiopatski artritis, vašem djetetu će se prvo dati drugi lijekovi. Ako vaše dijete ne reagira adekvatno na ove lijekove, vaše će dijete dobiti Simponi u kombinaciji s metotreksatom za liječenje bolesti.
Kontraindikacije Kada se Simponi ne smije koristiti
Nemojte koristiti Simponi:
- Ako ste alergični (preosjetljivi) na golimumab ili neki drugi sastojak ovog lijeka (naveden u dijelu 6).
- Ako imate tuberkulozu (TBC) ili neku drugu ozbiljnu infekciju.
- Ako imate umjereno ili teško zatajenje srca.
Ako niste sigurni odnosi li se bilo koji od gore navedenih uvjeta na vas, razgovarajte sa svojim liječnikom, ljekarnikom ili medicinskom sestrom prije nego počnete primjenjivati Simponi.
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Simponi
Prije upotrebe Simponija razgovarajte sa svojim liječnikom, ljekarnikom ili medicinskom sestrom.
Infekcije
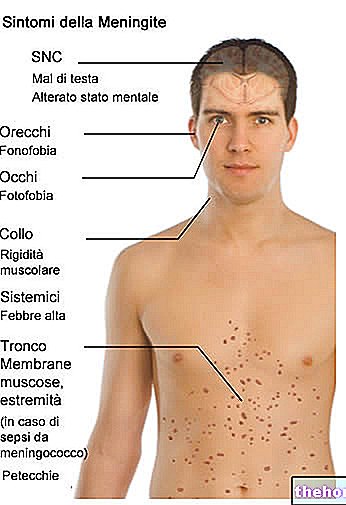
Odmah obavijestite svog liječnika ako ste već imali ili imate simptome infekcije tijekom ili nakon liječenja lijekom Simponi. Simptomi infekcije uključuju groznicu, kašalj, otežano disanje, simptome slične gripi, proljev, rane, zubne probleme ili peckanje pri mokrenju.
- Uz pomoć Simponija možete lakše dobiti infekcije.
- Infekcije mogu napredovati brže i biti teže. Također, infekcije iz prošlosti se mogu vratiti.
Tuberkuloza (TB)
Odmah obavijestite svog liječnika ako primijetite simptome tuberkuloze tijekom liječenja. Simptomi tuberkuloze uključuju uporni kašalj, gubitak tjelesne težine, osjećaj umora, groznicu ili noćno znojenje.
- Nekoliko slučajeva tuberkuloze zabilježeno je kod pacijenata liječenih lijekom Simponi, u rijetkim slučajevima čak i kod pacijenata koji su bili liječeni lijekovima za tuberkulozu. Vaš liječnik će napraviti pretrage kako bi provjerio imate li tuberkulozu. Liječnik će zabilježiti te testove u karticu upozorenja za pacijenta.
- Vrlo je važno da obavijestite svog liječnika ako ste ranije imali tuberkulozu ili ste bili u bliskom kontaktu s nekim tko ima ili je imao tuberkulozu.
- Ako vaš liječnik misli da ste u opasnosti od tuberkuloze, možda ćete se liječiti lijekovima protiv tuberkuloze prije nego što primite Simponi.
Virus hepatitisa B (HBV)
- Prije nego što primijenite Simponi, obavijestite svog liječnika ako ste nositelj ili ste imali hepatitis B
- Obavijestite svog liječnika ako mislite da ste u opasnosti od zaraze hepatitisom B
- Vaš liječnik bi trebao procijeniti imate li hepatitis B
- Liječenje blokatorima TNF -a, poput Simponija, može uzrokovati reaktiviranje virusa hepatitisa B u pacijenata koji nose ovaj virus, što u nekim slučajevima može uzrokovati smrt.
Invazivne gljivične infekcije
Odmah obavijestite svog liječnika ako ste živjeli ili putovali u "područje gdje su česte infekcije uzrokovane specifičnim vrstama gljivica koje mogu zahvatiti pluća ili druge dijelove tijela (tzv. Histoplazmoza, kokcidioidomikoza ili blastomikoza). Pitajte svog liječnika ako ne znate.da li su ove gljivične infekcije česte na području gdje ste živjeli ili putovali.
Rak i limfom
Recite svom liječniku ako imate ili ste ikada imali limfom (vrstu raka krvi) ili neku drugu vrstu raka prije nego što primite Simponi.
- Ako koristite Simponi ili druge blokatore TNF -a, možete povećati rizik od razvoja limfoma ili druge vrste raka.
- Pacijenti s teškim reumatoidnim artritisom ili drugim upalnim stanjima koji su dugo patili od ove bolesti mogu imati veći rizik od razvoja limfoma od prosjeka.
- Rak, uključujući neobične, ponekad smrtonosne karcinome, zabilježen je u djece i adolescenata koji su uzimali lijekove koji blokiraju TNF.
- U rijetkim slučajevima, kod pacijenata koji su uzimali druge blokatore TNF-a primijećen je specifičan i težak tip limfoma koji se naziva hepatosplenični limfom T-stanica. Većina tih pacijenata bili su adolescenti ili mladi muškarci. Ovaj oblik raka obično je rezultirao smrću. Gotovo svi ovi pacijenti također su primali lijekove poznate kao azatioprin ili 6-merkaptopurin. Obavijestite svog liječnika ako uzimate azatioprin ili 6-merkaptopurin sa Simponijem.
- Bolesnici s teškom perzistentnom astmom, kroničnom opstruktivnom plućnom bolešću (KOPB) ili teškim pušačima mogu imati povećan rizik od raka tijekom liječenja Simponijem. Ako imate tešku perzistentnu astmu, KOPB ili ste teški pušač, trebate razgovarati sa svojim liječnikom je li liječenje blokatorom TNF -a prikladno.
- Neki pacijenti liječeni golimumabom razvili su određene vrste raka kože. Ako primijetite bilo kakvu promjenu izgleda kože ili izrasline na koži tijekom ili nakon terapije, obavijestite svog liječnika.
Zastoj srca
Odmah obavijestite svog liječnika ako primijetite nove ili pogoršavajuće simptome zatajenja srca. Simptomi zatajenja srca uključuju nedostatak daha ili oticanje stopala.
- S blokatorima TNF -a, uključujući Simponi, zabilježeni su slučajevi novog ili pogoršanja zastoja srca. Neki od ovih pacijenata su umrli.
- Ako imate blago zatajenje srca i liječite se lijekom Simponi, liječnik će vas pomno pratiti.
Bolest živčanog sustava
Odmah obavijestite svog liječnika ako vam je ikada dijagnosticirana ili razvijete simptome demijelinizirajuće bolesti, poput multiple skleroze. Simptomi mogu uključivati promjene vida, slabost u rukama i nogama, utrnulost ili trnce u bilo kojem dijelu tijela. Vaš liječnik će odlučiti trebate li uzimati Simponi.
Stomatološke operacije ili zahvati
- Recite svom liječniku ako ćete imati bilo kakve stomatološke operacije ili zahvate.
- Recite kirurgu ili stomatologu koji izvodi zahvat da se liječite lijekom Simponi pokazujući karticu upozorenja za pacijenta.
Autoimune bolesti
Obavijestite svog liječnika ako razvijete simptome bolesti koja se naziva lupus. Simptomi uključuju uporni osip, groznicu, bolove u zglobovima i umor.
- U rijetkim slučajevima, ljudi liječeni blokatorima TNF -a razvili su lupus.
Bolesti krvi
Kod nekih pacijenata tijelo možda ne proizvodi dovoljno krvnih stanica koje pomažu tijelu u borbi protiv infekcija ili zaustavljanju krvarenja. Ako imate upornu temperaturu koju ne razumijete, imate modrice ili krvarite ili izgledate blijedo, odmah se obratite svom liječniku. Vaš liječnik može odlučiti prekinuti liječenje.
Ako niste sigurni odnosi li se bilo koji od gore navedenih uvjeta na vas, obratite se svom liječniku ili ljekarniku prije nego počnete primjenjivati Simponi.
Cijepljenja
Recite svom liječniku ako ste nedavno bili cijepljeni ili se planirate cijepiti.
- Ne smijete primati određena (živa) cjepiva tijekom liječenja Simponijem.
- Neka cijepljenja mogu uzrokovati infekcije. Ako ste primali Simponi tijekom trudnoće, vaša beba može imati povećan rizik od dobivanja ove infekcije otprilike šest mjeseci nakon posljednje doze primljene tijekom trudnoće. Važno je obavijestiti svog pedijatra i druge zdravstvene radnike o uporabi Simponija. može odlučiti kada bi dijete trebalo primiti cjepivo.
Razgovarajte s liječnikom svog djeteta o cijepljenju za vaše dijete. Ako je moguće, vaše dijete mora biti upoznato sa svim cijepljenjima prije upotrebe Simponija.
Infektivni terapijski agensi
Posavjetujte se sa svojim liječnikom ako ste nedavno uzimali ili namjeravate započeti liječenje infektivnim terapijskim sredstvom (poput ukapavanja BCG -a za liječenje raka).
Alergijske reakcije
Odmah obavijestite svog liječnika ako se nakon liječenja Simponijem razviju simptomi alergijske reakcije. Simptomi alergijske reakcije mogu uključivati oticanje lica, usana, usta ili grla koje može uzrokovati poteškoće pri gutanju ili disanju, osip na koži, osip, oticanje šaka, stopala i gležnjeva.
- Neke od ovih reakcija mogu biti ozbiljne ili, rijetko, opasne po život.
- Neke od ovih reakcija javljaju se nakon prve primjene Simponija.
Djeca i adolescenti
Simponi se ne preporučuje za djecu manju od 40 kg s poliartikularnim juvenilnim idiopatskim artritisom ili za djecu i adolescente mlađe od 18 godina za bilo koje drugo stanje.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak lijeka Simponi
- Obavijestite svog liječnika ili ljekarnika ako uzimate, nedavno ste uzimali ili biste mogli uzeti bilo koje druge lijekove, uključujući bilo koje druge lijekove za liječenje reumatoidnog artritisa, poliartikularnog juvenilnog idiopatskog artritisa, psorijatičnog artritisa, ankilozirajućeg spondilitisa, aksijalnog spondiloartritisa, neradiografskog ili ulceroznog kolitisa.
- Ne biste trebali uzimati Simponi s lijekovima koji sadrže djelatnu tvar anakinru ili abatacept. Ovi lijekovi se koriste za liječenje reumatskih bolesti.
- Obavijestite svog liječnika ili ljekarnika ako uzimate bilo koje druge lijekove koji utječu na imunološki sustav.
- Ne može se liječiti određenim (živim) cjepivima dok se koristi Simponi.
Ako niste sigurni odnosi li se bilo koji od gore navedenih uvjeta na vas, obratite se svom liječniku ili ljekarniku prije nego počnete primjenjivati Simponi.
Upozorenja Važno je znati da:
Trudnoća i dojenje
Prije upotrebe Simponija razgovarajte sa svojim liječnikom ako:
- Trudni ste ili planirate trudnoću dok koristite Simponi. Učinci ovog lijeka na trudnice nisu poznati. Ne preporučuje se uporaba lijeka Simponi u trudnica. Ako ćete se liječiti lijekom Simponi, trebali biste izbjeći trudnoću primjenom odgovarajuće kontracepcije tijekom liječenja i najmanje 6 mjeseci nakon posljednje injekcije Simponija.
- Prije dojenja posljednji tretman Simponijem mora biti najmanje 6 mjeseci ranije. Morate prestati dojiti ako vam se daje Simponi.
- Ako ste primali Simponi tijekom trudnoće, vaša beba može imati povećan rizik od infekcije. Važno je obavijestiti svog pedijatra i druge zdravstvene radnike o vašoj uporabi Simponija prije nego što vaša beba primi cjepivo (za više informacija pogledajte odlomak o cijepljenja).
Ako ste trudni ili dojite, mislite da ste trudni ili planirate trudnoću, obratite se svom liječniku ili ljekarniku za savjet prije nego uzmete ovaj lijek.
Upravljanje vozilima i strojevima
Simponi može neznatno umanjiti vašu sposobnost upravljanja vozilima i rada s alatima ili strojevima. Nakon uporabe Simponija možete osjetiti omaglicu. U tom slučaju nemojte voziti niti rukovati alatima ili strojevima.
Simponi sadrži lateks i sorbitol
Osjetljivost na lateks
Osjetljivost na lateks Jedan dio napunjene brizgalice, poklopac koji prekriva iglu, sadrži lateks. Budući da lateks može izazvati ozbiljne alergijske reakcije, obavijestite svog liječnika prije uporabe Simponija ako ste vi ili njegovateljica alergični na lateks.
Netolerancija na sorbitol
Simponi sadrži sorbitol (E420). Ako vam je liječnik rekao da ne podnosite neke šećere, obratite se svom liječniku prije uzimanja ovog lijeka.
Doziranje i način uporabe Kako koristiti Simponi: Doziranje
Uvijek koristite ovaj lijek točno onako kako vam je rekao vaš liječnik ili ljekarnik. Ako ste u nedoumici, trebate se posavjetovati sa svojim liječnikom ili ljekarnikom.
Koliko se Simponija daje
Reumatoidni artritis, psorijatični artritis i aksijalni spondiloartritis, uključujući ankilozirajući spondilitis i neradiografski aksijalni spondiloartritis:
- Preporučena doza je 50 mg (sadržaj 1 napunjene olovke) koja se daje jednom mjesečno, na isti dan svakog mjeseca.
- Prije uzimanja četvrte doze razgovarajte sa svojim liječnikom. Vaš liječnik će odlučiti trebate li nastaviti liječenje Simponijem.
- Ako imate više od 100 kg, doza se može povećati na 100 mg (sadržaj 2 napunjene olovke), jednom mjesečno, uvijek na isti dan svakog mjeseca.
Poliartikularni juvenilni idiopatski artritis:
- Preporučena doza je 50 mg koja se daje jednom mjesečno, na isti dan svakog mjeseca.
- Prije nego dijete uzme četvrtu dozu, razgovarajte s liječnikom svog djeteta. Liječnik vašeg djeteta odlučit će trebate li nastaviti liječenje Simponijem.
Ulcerozni kolitis
- Donja tablica prikazuje kako ćete općenito koristiti ovaj lijek.
- U pacijenata s tjelesnom težinom manjom od 80 kg, 50 mg (sadržaj 1 napunjene olovke) 4 tjedna nakon zadnjeg liječenja, a zatim svaka 4 tjedna.
- U pacijenata s tjelesnom težinom od 80 kg ili više, 100 mg (sadržaj 2 napunjene olovke) 4 tjedna nakon zadnjeg liječenja, a zatim svaka 4 tjedna.
Kako se daje Simponi
- Simponi se daje injekcijom pod kožu (potkožno).
- U početku će vaš liječnik ili medicinsko osoblje ubrizgati Simponi, no vi i vaš liječnik možete odlučiti da možete sami ubrizgati Simponi. U tom slučaju bit ćete upućeni kako sami ubrizgati Simponi.
Posavjetujte se sa svojim liječnikom ako imate pitanja u vezi samostalne primjene injekcije. Na kraju ove upute pronaći ćete detaljne "Upute za primjenu".
Ako ste zaboravili upotrijebiti Simponi
Ako ste zaboravili upotrijebiti Simponi na zakazani dan, ubrizgajte propuštenu dozu čim se sjetite.
Nemojte upotrijebiti dvostruku dozu kako biste nadoknadili zaboravljenu dozu.
Kada ubrizgati sljedeću dozu:
- Ako kasnite manje od 2 tjedna, ubrizgajte propuštenu dozu čim se sjetite i nastavite slijediti svoj izvorni raspored.
- Ako kasnite više od 2 tjedna, ubrizgajte zaboravljenu dozu čim se sjetite i obavijestite svog liječnika ili ljekarnika i pitajte kada biste trebali uzeti sljedeću dozu.
Ako niste sigurni što učiniti, pitajte svog liječnika, ljekarnika ili medicinsku sestru.
Ako prestanete koristiti Simponi
Ako razmišljate o prestanku primjene Simponija, prvo se obratite svom liječniku ili ljekarniku.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku ili ljekarniku.
Predoziranje Što učiniti ako ste uzeli previše Simponija
Ako ste uzeli ili dali previše lijeka Simponi (ubrizgali ste ga previše u jednoj dozi ili ste ga koristili prečesto), odmah obavijestite svog liječnika ili ljekarnika. Uvijek uzmite vanjsko pakiranje i ovo uputstvo, čak i ako je prazno.
Nuspojave Koje su nuspojave Simponija
Kao i svi drugi lijekovi, i ovaj lijek može izazvati nuspojave, iako se one neće pojaviti kod svih. Neki pacijenti mogu osjetiti ozbiljne nuspojave koje mogu zahtijevati medicinski tretman. Rizik od nekih nuspojava veći je pri dozi od 100 mg u usporedbi s dozom od 50 mg. Nuspojave se također mogu pojaviti nekoliko mjeseci nakon posljednje injekcije.
Odmah obavijestite svog liječnika ako primijetite bilo koju od sljedećih ozbiljnih nuspojava Simponija koje uključuju:
- alergijske reakcije koje mogu biti teške ili rijetko opasne po život (rijetko).Simptomi alergijske reakcije mogu uključivati oticanje lica, usana, usta ili grla koje može uzrokovati poteškoće pri gutanju ili disanju, osip na koži, osip, oticanje šaka, stopala ili gležnjeva. Neke od ovih reakcija dogodile su se nakon prve primjene Simponija.
- teške infekcije (uključujući tuberkulozu, bakterijske infekcije uključujući teške infekcije krvi i upale pluća, teške gljivične infekcije i druge oportunističke infekcije) (česte). Simptomi infekcije mogu uključivati groznicu, umor, (uporni) kašalj, otežano disanje, simptome slične gripi, gubitak težine, noćno znojenje, proljev, rane, zubne probleme i osjećaj peckanja pri mokrenju.
- reaktivacija virusa hepatitisa B ako ste nositelj ili ste ranije imali hepatitis B (rijetko). Simptomi mogu uključivati žutilo kože i očiju, tamnosmeđi urin, bol u desnoj strani trbuha, groznicu, loš osjećaj, slabost i osjećaj umora.
- bolesti živčanog sustava poput multiple skleroze (rijetko). Simptomi bolesti živčanog sustava mogu uključivati promjene vida, slabost u rukama ili nogama, utrnulost ili trnce u bilo kojem dijelu tijela.
- rak limfnih čvorova (limfom) (rijetko). Simptomi limfoma mogu uključivati natečene limfne čvorove, gubitak tjelesne težine ili groznicu.
- zatajenje srca (rijetko). Simptomi zatajenja srca mogu uključivati nedostatak daha ili oticanje stopala.
- znakovi poremećaja imunološkog sustava koji se nazivaju: - lupus (rijetko). Simptomi mogu uključivati bolove u zglobovima ili osip na obrazima ili rukama osjetljiv na sunce. - sarkoidoza (rijetko). Simptomi mogu uključivati ustrajan kašalj, otežano disanje, bol u prsima, groznicu, natečene limfne čvorove, gubitak težine, osip na koži i zamagljen vid.
- oticanje malih krvnih žila (vaskulitis) (rijetko). Simptomi mogu uključivati groznicu, glavobolju, gubitak tjelesne težine, noćno znojenje, osip i probleme s živcima kao što su utrnulost i trnci.
- rak kože (rijetko). Simptomi raka kože mogu uključivati promjene u izgledu kože ili izrasline na koži.
- bolesti krvi (uobičajeno). Simptomi bolesti krvi mogu uključivati groznicu koja ne prolazi, snažnu sklonost modricama ili krvarenjima ili vrlo blijed izgled.
- rak krvi (leukemija) (rijetko). Simptomi leukemije mogu uključivati groznicu, osjećaj umora, česte infekcije, modrice i noćno znojenje.
Odmah obavijestite svog liječnika ako primijetite bilo koji od gore navedenih simptoma.
Sljedeće dodatne nuspojave primijećene su kod lijeka Simponi:
Vrlo česte nuspojave (mogu se javiti u više od 1 na 10 osoba):
- Infekcije gornjih dišnih putova, grlobolja ili promuklost, prehlada
Česte nuspojave (mogu se javiti u do 1 na 10 osoba):
- Abnormalni testovi jetre (povećani jetreni enzimi), utvrđeni tijekom krvnih pretraga koje je obavio vaš liječnik
- Vrtoglavica
- Glavobolja
- Osjećaj utrnulosti ili trnci
- Površinske gljivične infekcije
- Apsces
- Bakterijske infekcije (poput celulitisa)
- Smanjenje crvenih krvnih stanica
- Pozitivan nalaz krvi za lupus
- Alergijske reakcije
- Probavne smetnje
- Bol u želucu
- Mučnina (mučnina)
- Utjecaj
- Bronhitis
- Infekcija sinusa
- Herpes na licu
- Visoki krvni tlak
- Groznica
- Astma, otežano disanje, teško disanje
- Poremećaji želuca i crijeva koji uključuju upalu unutrašnjosti želuca i debelog crijeva koja može uzrokovati groznicu
- Bol i čirevi u ustima
- Reakcije na mjestu ubrizgavanja (uključujući crvenilo, tvrdoću, bol, modrice, svrbež, trnce i iritaciju)
- Gubitak kose
- Osip i svrbež kože
- Poteškoće sa spavanjem
- Depresija
- Osjećaj slabosti
- Prijelomi kostiju
- Bol u prsima
Manje česte nuspojave (mogu se javiti u do 1 na 100 osoba):
- Upala bubrega
- Rak, uključujući rak kože i nekancerozne kvržice ili male mase, uključujući madeže
- Mjehurići na koži
- Psorijaza (uključujući onu dlanova i / ili tabana i / ili u obliku kožnih pustula)
- Smanjenje trombocita
- Smanjenje bijelih krvnih stanica
- Kombinirano smanjenje trombocita, crvenih krvnih stanica i bijelih krvnih stanica
- Poremećaji štitnjače
- Povećanje razine šećera u krvi
- Povećanje razine kolesterola u krvi
- Poremećaji ravnoteže
- Vizualni poremećaji
- Osjećaj nepravilnog rada srca
- Sužavanje krvnih žila u srcu
- Krvni ugrušci
- Crvenilo
- Zatvor
- Kronična upala pluća
- Kiselinski refluks
- Kamenje u žuči
- Problemi s jetrom
- Poremećaji dojki
- Menstrualni poremećaji
Rijetke nuspojave (mogu se javiti u do 1 na 1.000 osoba):
- Nemogućnost koštane srži da proizvodi krvne stanice
- Infekcija zglobova ili okolnih tkiva
- Teško ozdravljenje
- Upala krvnih žila unutarnjih organa
- Leukemija
- Melanom (vrsta raka kože)
- Ljuštenje kože
- Imunološki poremećaji koji mogu zahvatiti pluća, kožu i limfne čvorove (vrlo često prisutni kao sarkoidoza)
- Bol i promjena boje u prstima ruku ili nogu
- Poremećaji okusa
- Poremećaji mjehura
- Problemi s bubrezima
- Upala krvnih žila u koži uzrokuje osip
Nuspojave s učestalošću nisu poznate:
- Karcinom stanica Merkel (vrsta raka kože)
- Rijetki rak krvi koji pogađa uglavnom mlade ljude (hepatosplenični limfom T-stanica)
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Nuspojave možete prijaviti i izravno putem nacionalnog sustava za prijavu navedenih u Dodatku V. Nuspojave koje možete pomoći pružiti više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
- Čuvajte ovaj lijek izvan pogleda i dohvata djece.
- Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na naljepnici i kutiji iza "EXP". Rok valjanosti odnosi se na zadnji dan tog mjeseca.
- Čuvati u hladnjaku (2 ° C-8 ° C). Nemojte zamrzavati.
- Napunjenu brizgalicu čuvajte u vanjskom pakiranju radi zaštite lijeka od svjetlosti.
- Nemojte koristiti ovaj lijek ako primijetite da tekućina nije svijetle do svijetložute boje, zamućena je ili sadrži strane čestice.
- Ne bacajte lijekove u otpadne vode ili kućni otpad. Pitajte svog liječnika ili ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Druge podatke
Što Simponi sadrži
Aktivni sastojak je golimumab. Jedna napunjena olovka od 0,5 ml sadrži 50 mg golimumaba.
Pomoćni sastojci su sorbitol (E420), L-histidin, L-histidin monohidroklorid monohidrat, polisorbat 80 i voda za injekcije.
Izgled Simponija i sadržaj pakiranja
Simponi se isporučuje kao otopina za injekcije u napunjenoj olovci za jednokratnu uporabu. Simponi je dostupan u pakiranjima koja sadrže 1 napunjenu olovku i višestrukim pakiranjima koja sadrže 3 (3 pakiranja od 1) napunjene olovke. Ne mogu se na tržište staviti sve veličine pakiranja.
Otopina je bistra do blago opalescentna (sjajna poput bisera), bezbojna do svijetložuta i može sadržavati neke male prozirne ili bijele proteinske čestice. Nemojte koristiti Simponi ako je otopina promijenila boju, zamućena je ili sadrži vidljive strane čestice.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
SIMPONI 50 MG INJEKTIVNA OTOPINA
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Simponi 50 mg otopina za injekciju u napunjenoj olovci
Jedna napunjena olovka od 0,5 ml sadrži 50 mg golimumaba *.
Simponi 50 mg otopina za injekciju u napunjenoj štrcaljki
Jedna napunjena štrcaljka od 0,5 ml sadrži 50 mg golimumaba *.
* IgG1 humano monoklonsko antitijelo? proizvedeno iz stanične linije mišjeg hibridoma s tehnologijom rekombinantne DNA.
Pomoćna tvar s poznatim učinkom:
Svaka napunjena brizgalica sadrži: 20,5 mg sorbitola za dozu od 50 mg.
Svaka napunjena štrcaljka sadrži: 20,5 mg sorbitola za dozu od 50 mg.
Za potpuni popis pomoćnih tvari pogledajte odjeljak 6.1.
03.0 FARMACEUTSKI OBLIK
Otopina za injekcije u napunjenoj olovci (injekcija), SmartJect
Otopina za injekciju u napunjenoj štrcaljki (injekcija)
Otopina je bistra do blago opalescentna, bezbojna do blijedožuta.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Reumatoidni artritis (RA)
Simponi, u kombinaciji s metotreksatom (MTX), indiciran je za:
• liječenje umjerenog do teškog aktivnog reumatoidnog artritisa u odraslih pacijenata kada je odgovor na antireumatske lijekove koji mijenjaju bolest (DMARD), uključujući MTX, bio neodgovarajući.
• liječenje teškog, aktivnog i progresivnog reumatoidnog artritisa u odraslih osoba koje prethodno nisu liječene MTX -om.
Pokazalo se da Simponi, u suradnji s MTX-om, smanjuje brzinu progresije oštećenja zglobova izmjerenu rendgenskim zrakama i poboljšava fizičku funkciju.
Juvenilni idiopatski artritis
Poliartikularni juvenilni idiopatski artritis (PIA)
Simponi u kombinaciji s MTX -om indiciran je za liječenje poliartikularnog juvenilnog idiopatskog artritisa u djece tjelesne težine najmanje 40 kg koja su neadekvatno reagirala na prethodnu terapiju MTX -om.
Psorijatični artritis (AP)
Simponi, sam ili u kombinaciji s metotreksatom (MTX), indiciran je za liječenje aktivnog i progresivnog psorijatičnog artritisa u odraslih osoba kada je odgovor na prethodnu DMARD terapiju bio nedovoljan. Pokazalo se da Simponi smanjuje brzinu progresije lijeka. oštećenje perifernog zgloba, mjereno rendgenskim snimkama u bolesnika sa simetričnim podtipovima poliartikularne bolesti (vidjeti dio 5.1) i radi poboljšanja tjelesne funkcije.
Aksijalni spondiloartritis
Ankilozirajući spondilitis (AS)
Simponi je indiciran za liječenje teškog, aktivnog ankilozirajućeg spondilitisa kod odraslih osoba koje nisu adekvatno reagirale na konvencionalne terapije.
Neradiografski aksijalni spondiloartritis (aksijalni SpA br.)
Simponi je indiciran za liječenje odraslih pacijenata s teškim aktivnim neradiografskim aksijalnim spondiloartritisom s objektivnim znakovima upale na što ukazuju dokazi povišenog C-reaktivnog proteina (CRP) i / ili magnetske rezonancije (MRI) koji su imali neodgovarajući odgovor ili ne podnose nesteroidne protuupalne lijekove (NSAID).
Ulcerozni kolitis (CU)
Simponi je indiciran za liječenje umjerenog do teškog aktivnog ulceroznog kolitisa u odraslih pacijenata koji nisu adekvatno odgovorili na konvencionalnu terapiju, uključujući kortikosteroide i 6-merkaptopurin (6-MP) ili azatioprin (AZA), ili koji ne podnose ili za koje postoji medicinska kontraindikacija za ove terapije.
04.2 Doziranje i način primjene
Liječenje Simponijem trebali bi započeti i nadzirati liječnici specijalisti s iskustvom u dijagnostici i liječenju reumatoidnog artritisa, poliartikularnog juvenilnog idiopatskog artritisa, psorijatičnog artritisa, ankilozirajućeg spondilitisa, neradiografskog aksijalnog spondiloartritisa ili ulceroznog kolitisa. Pacijente liječene Simponijem treba upozoriti na pacijenta Kartica.
Doziranje
Reumatoidni artritis
Simponi 50 mg daje se jednom mjesečno, na isti dan svakog mjeseca.
Simponi se mora primjenjivati istodobno s MTX -om.
Psorijatični artritis, ankilozirajući spondilitis ili neradiografski aksijalni spondiloartritis
Simponi 50 mg daje se jednom mjesečno, na isti dan svakog mjeseca.
Za sve gore navedene indikacije dostupni podaci ukazuju na to da se klinički odgovor obično postiže unutar 12-14 tjedana od početka liječenja (nakon 3-4 doze). Treba razmotriti nastavak terapije u pacijenata koji ne pokazuju dokaze o terapijskoj koristi unutar ovog vremenskog okvira.
Pacijenti s tjelesnom težinom većom od 100 kg
Za sve gore navedene indikacije, u bolesnika s RA, AP, SA ili aksijalnom SpA nr težinom većom od 100 kg, koji ne postignu odgovarajući klinički odgovor nakon 3 ili 4 doze, povećanje doze golimumaba do 100 mg jednom mjesečno, uzimajući u obzir povećani rizik od nekih ozbiljnih nuspojava pri primjeni doze od 100 mg u usporedbi s dozom od 50 mg (vidjeti dio 4.8). Treba razmotriti nastavak terapije u bolesnika koji ne pokazuju dokaze o terapijskoj koristi nakon što su primili 3- 4 dodatne doze od 100 mg.
Ulcerozni kolitis
Pacijenti s tjelesnom težinom manjom od 80 kg
Simponi se daje kao početna doza od 200 mg, nakon čega slijedi 100 mg u 2. tjednu, zatim 50 mg svaka 4 tjedna nakon toga (vidjeti dio 5.1).
Pacijenti s tjelesnom težinom većom ili jednakom 80 kg
Simponi se daje kao početna doza od 200 mg, nakon čega slijedi 100 mg u 2. tjednu, zatim 100 mg svaka 4 tjedna nakon toga (vidjeti dio 5.1).
Tijekom održavanja, kortikosteroidi se mogu postupno smanjivati u skladu sa smjernicama kliničke prakse.
Dostupni podaci ukazuju na to da se klinički odgovor općenito postiže unutar 12-14 tjedana liječenja (nakon 4 doze). Treba razmotriti nastavak terapije kod pacijenata koji u tom vremenskom razdoblju ne pokažu dokaze o terapijskoj koristi.
Propuštena doza
Ako pacijent zaboravi ubrizgati Simponi na zakazani dan, propuštenu dozu treba ubrizgati čim se pacijent sjeti. Pacijente treba uputiti da ne ubrizgavaju dvostruku dozu kako bi nadoknadili zaboravljenu dozu.
Sljedeću dozu treba primijeniti prema sljedećim uputama:
• Ako je odgođena doza manja od 2 tjedna, pacijent bi trebao ubrizgati propuštenu dozu i nastaviti slijediti svoj izvorni raspored.
• Ako je kašnjenje u doziranju duže od 2 tjedna, pacijent bi trebao ubrizgati propuštenu dozu i morat će se odrediti novi raspored doziranja od datuma ove injekcije.
Posebne populacije
Starije osobe (≥ 65 godina)
U starijih osoba nije potrebno prilagođavanje doze.
Oštećenje bubrega i jetre
Simponi nije ispitivan u ovih populacija pacijenata. Ne mogu se dati preporuke o dozama.
Pedijatrijska populacija
Sigurnost i djelotvornost lijeka Simponi u pacijenata mlađih od 18 godina za indikacije koje nisu pIA nisu utvrđene.
Poliartikularni juvenilni idiopatski artritis
Simponi 50 mg daje se jednom mjesečno, na isti dan svakog mjeseca, za djecu s tjelesnom težinom od najmanje 40 kg.
Dostupni podaci ukazuju na to da se klinički odgovor obično postiže unutar 12-14 tjedana liječenja (nakon 3-4 doze). Nastavak terapije treba preispitati u djece koja u tom vremenskom razdoblju ne pokazuju nikakve terapijske koristi.
Način primjene
Simponi je za potkožnu primjenu. Nakon odgovarajuće obuke u tehnici potkožne injekcije, pacijenti će moći sami ubrizgati Simponi ako njihov liječnik utvrdi da su sposobni, uz odgovarajući medicinski nadzor ako je potrebno. Pacijente treba uputiti da ubrizgaju punu količinu lijeka Simponi u skladu s cjelovitim uputama za primjenu navedenim u uputama za uporabu.Ako je potrebno više injekcija, injekcije se trebaju primijeniti na različitim mjestima tijela.
Za upute o primjeni, vidjeti dio 6.6.
04.3 Kontraindikacije
Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari navedenih u dijelu 6.1.
Aktivna tuberkuloza (TB) ili druge ozbiljne infekcije poput sepse i oportunističkih infekcija (vidjeti dio 4.4).
Bolesnici s umjerenim do teškim zatajenjem srca (NYHA klasa III / IV - New York Heart Association) (vidjeti dio 4.4).
04.4 Posebna upozorenja i mjere opreza pri uporabi
Infekcije
Prije, tijekom i nakon liječenja lijekom Simponi, bolesnike treba pomno nadzirati zbog infekcija uključujući tuberkulozu. Budući da eliminacija golimumaba može potrajati do 5 mjeseci, u tom se razdoblju treba nastaviti s praćenjem. Daljnje liječenje lijekom Simponi ne smije se provoditi ako pacijent razvije teške infekcije ili sepsu (vidjeti dio 4.3).
Simponi se ne smije koristiti u bolesnika s klinički značajnom, aktivnom infekcijom. Potreban je oprez pri razmatranju uporabe Simponija u bolesnika s kroničnom infekcijom ili u povijesti bolesti koje se ponavljaju. Pacijente je potrebno na odgovarajući način obavijestiti o potrebi izbjegavanja izloženosti potencijalnim čimbenicima rizika od infekcija.
Pacijenti koji uzimaju lijekove koji blokiraju TNF skloniji su teškim infekcijama.
U pacijenata liječenih lijekom Simponi zabilježene su bakterijske infekcije (uključujući sepsu i upalu pluća), mikobakterijske (uključujući TBC), invazivne gljivične infekcije i oportunističke infekcije, uključujući one sa smrtnim ishodom. Neke od ovih ozbiljnih infekcija razvile su se u bolesnika na istodobnoj imunosupresivnoj terapiji koja ih, osim u osnovi bolesti, može predisponirati na infekcije. Bolesnike koji razviju novu infekciju tijekom liječenja lijekom Simponi treba pažljivo pratiti i podvrgnuti "pažljivoj dijagnostičkoj procjeni. Primjenu lijeka Simponi treba prekinuti ako se u bolesnika razvije nova teška infekcija ili sepsa i odgovarajuće" započinjanje. Antimikrobna ili antifungalna terapija sve dok infekcija nije Za pacijente koji su živjeli ili putovali u regije u kojima su invazivne gljivične infekcije poput histoplazmoze, kokcidioidomikoze ili blastomikoze endemične, treba pažljivo razmotriti dobrobiti i rizike liječenja lijekom Simponi prije početka terapije Simponijem. U visokorizičnih pacijenata liječenih Simponi, invazivnu gljivičnu infekciju, treba posumnjati ako razviju tešku sustavnu bolest. Ako je moguće, dijagnozu i primjenu empirijske antifungalne terapije u ovih bolesnika treba postaviti u dogovoru s liječnikom s iskustvom u skrbi za bolesnike s invazivnim gljivičnim infekcijama.
Tuberkuloza
U bolesnika liječenih Simponijem zabilježeni su slučajevi tuberkuloze. Valja napomenuti da se u većini ovih slučajeva radilo o izvanplućnoj tuberkulozi, lokaliziranoj i difuznoj.
Prije početka liječenja lijekom Simponi, sve bolesnike treba pregledati na aktivnu i neaktivnu ("latentnu") tuberkulozu. Ova procjena treba uključivati detaljnu medicinsku povijest, uključujući osobnu povijest tuberkuloze ili mogući prethodni kontakt s izvorom TBC infekcije te prethodnu i / ili istodobnu imunosupresivnu terapiju. U svih se bolesnika trebaju provesti odgovarajući dijagnostički testovi, poput tuberkulinskih kožnih ili krvnih pretraga te rendgenskih snimaka prsnog koša (mogu se primijeniti lokalne smjernice). Preporučuje se da se ti testovi zabilježe na kartici s upozorenjima pacijenata. Prepisitelje se podsjeća na rizik od lažno negativnih rezultata kožnih testova na tuberkulinu, osobito u teško bolesnih ili imunološki oslabljenih pacijenata.
Ako se dijagnosticira aktivna tuberkuloza, ne smije se započeti terapija Simponijem (vidjeti dio 4.3).
Ako se sumnja na latentnu tuberkulozu, potrebno je konzultirati liječnika s iskustvom u liječenju tuberkuloze. U svim dolje opisanim situacijama potrebno je pažljivo razmotriti omjer koristi i rizika terapije Simponijem.
Ako se dijagnosticira neaktivna ("latentna") tuberkuloza, potrebno je započeti antituberkuloznu terapiju za latentnu tuberkulozu prije početka liječenja lijekom Simponi, prema lokalnim smjernicama.
U pacijenata koji imaju mnogo ili značajne čimbenike rizika za tuberkulozu i imaju negativan test na latentnu tuberkulozu, potrebno je razmotriti antituberkuloznu terapiju prije početka primjene Simponija. Prije početka liječenja Simponijem treba razmotriti i primjenu antituberkulotičke terapije bolesnici s prethodnom anamnezom latentne ili aktivne tuberkuloze za koje se ne može potvrditi odgovarajući tijek liječenja.
Slučajevi aktivne tuberkuloze dogodili su se u bolesnika liječenih lijekom Simponi tijekom i nakon liječenja latentne tuberkuloze. Bolesnike liječene lijekom Simponi treba pomno pratiti zbog znakova i simptoma aktivne tuberkuloze, uključujući pacijente koji su negativno testirani na latentnu tuberkulozu, pacijente koji se liječe od latentne tuberkuloze ili pacijente koji su prethodno bili liječeni od latentne tuberkuloze. "Infekcija tuberkulozom.
Svim pacijentima treba savjetovati da potraže liječnički savjet ako se tijekom ili nakon liječenja Simponijem pojave znakovi / simptomi koji ukazuju na tuberkulozu (npr. Uporni kašalj, mršavljenje / gubitak tjelesne težine, niska temperatura).
Reaktivacija virusa hepatitisa B
Reaktivacija hepatitisa B opažena je kod pacijenata liječenih antagonistima TNF-a, uključujući Simponi, i koji su bili kronični nositelji ovog virusa (tj. Pozitivni na površinski antigen). U nekim slučajevima došlo je do fatalnih ishoda.
Prije početka liječenja lijekom Simponi pacijente treba pregledati na HBV infekciju. Za bolesnike koji su pozitivni na HBV infekciju, preporučuje se konzultacija s liječnikom s iskustvom u liječenju hepatitisa B.
Nositelje virusa hepatitisa B za koje je potrebno liječenje lijekom Simponi potrebno je pomno pratiti zbog znakova i simptoma aktivne infekcije virusom hepatitisa B tijekom trajanja terapije i nekoliko mjeseci nakon završetka terapije. Dovoljno je podataka o bolesnicima s virusom hepatitisa B koji se liječe antivirusnim lijekovima terapiju u kombinaciji s terapijom antagonistima TNF-a kako bi se spriječila reaktivacija virusa hepatitisa B. U bolesnika kod kojih se razvije reaktivacija virusa hepatitisa B, liječenje Simponijem mora se prekinuti i započeti učinkovita antivirusna terapija s odgovarajućim potpornim liječenjem.
Maligne neoplazme i limfoproliferativne bolesti
Potencijalna uloga terapije inhibitorom TNF -a u razvoju zloćudnih bolesti nije poznata. Na temelju dosadašnjih saznanja, ne može se isključiti mogući rizik od razvoja limfoma, leukemije ili drugih zloćudnih bolesti kod pacijenata liječenih antagonistima TNF -a. Treba biti oprezan pri razmatranju terapije inhibitorom TNF -a u bolesnika s malignom bolešću u anamnezi ili prilikom razmatranja nastavka liječenja u pacijenata u kojih se razvije zloćudni tumor.
Dječje maligne neoplazme
U razdoblju nakon stavljanja lijeka u promet, zloćudni tumori, neki smrtonosni, zabilježeni su među djecom, adolescentima i mladim odraslim osobama (do 22 godine starosti) liječenima lijekovima koji blokiraju TNF (početak terapije ≤ 18 godina. Približno polovica slučajeva bila je Ostali slučajevi bili su predstavljeni različitim malignitetima i uključivali su rijetke maligne bolesti obično povezane s imunosupresijom. Ne može se isključiti rizik od razvoja malignih neoplazmi u djece i adolescenata liječenih inhibitorima TNF -a.
Limfom i leukemija
U kontroliranim fazama kliničkih ispitivanja sa svim lijekovima inhibitorima TNF-a, uključujući Simponi, primijećeno je više slučajeva limfoma među pacijentima koji su primali liječenje protiv TNF-a u usporedbi s kontrolnim pacijentima. Tijekom kliničkih ispitivanja Simonija IIb i III faze u RA, AP i SA, učestalost limfoma u pacijenata liječenih Simponijem bila je veća nego što se očekivalo u općoj populaciji. U bolesnika liječenih Simponijem zabilježeni su slučajevi leukemije. povećan pozadinski rizik od limfoma i leukemije u pacijenata s reumatoidnim artritisom s dugotrajnom, visoko aktivnom upalnom bolešću, što komplicira procjenu rizika.
Rijetki slučajevi hepatospleničnog limfoma T-stanica (HSTCL) prijavljeni su nakon stavljanja lijeka u promet kod pacijenata liječenih drugim lijekovima koji blokiraju TNF (vidjeti dio 4.8). Ovaj rijetki oblik limfoma T-stanica ima izrazito agresivan tijek i obično smrtonosni ishod Većina slučajeva dogodila se kod adolescenata i mladih odraslih muškaraca, gotovo svi koji su istodobno primali azatioprin (AZA) ili 6-merkaptopurin (6-MP) za upalnu bolest crijeva. Potencijalni rizik kombinacije AZA ili 6-MP i Simponija mora se pažljivo razmotriti. Ne može se isključiti rizik od razvoja hepatospleničnog limfoma T-stanica u bolesnika liječenih lijekovima koji blokiraju TNF.
Maligne neoplazme osim limfoma
U kontroliranim fazama kliničkih ispitivanja faze IIb i III provedenih sa Simponijem u RA, AP, SA i CU, incidencija malignih tumora osim limfoma (isključujući nemelanomski rak kože) bila je slična u skupini liječenoj Simponijem i u kontrolnoj skupini .
Displazija debelog crijeva / karcinom
Nije poznato utječe li liječenje golimumabom na rizik od razvoja displazije ili raka debelog crijeva. Svi bolesnici s ulceroznim kolitisom koji imaju povećan rizik od razvoja displazije ili karcinoma debelog crijeva (na primjer, bolesnici s dugotrajnim ulceroznim kolitisom ili primarnim sklerozirajućim kolangitisom) ili koji u anamnezi imaju displaziju ili rak debelog crijeva trebaju se ispitati na ovu displaziju u redovitim intervalima prije početka terapije i tijekom tijeka bolesti. Ova procjena treba uključivati kolonoskopiju i biopsiju u skladu s lokalnim preporukama. U bolesnika s nedavno dijagnosticiranom displazijom koji se liječe lijekom Simponi, potrebno je pažljivo razmotriti omjer koristi i rizika kod pojedinog bolesnika te treba li nastaviti s terapijom.
U istraživačkom kliničkom ispitivanju koje je procjenjivalo uporabu lijeka Simponi u bolesnika s teškom perzistentnom astmom, zabilježeno je više slučajeva malignosti u pacijenata liječenih Simponijem nego u kontrolnih bolesnika (vidjeti dio 4.8). Značaj ovih nalaza nije poznat.
U istraživačkoj kliničkoj studiji koja je procjenjivala uporabu drugog lijeka protiv TNF-a, infliksimaba, u bolesnika s umjerenom do teškom kroničnom opstruktivnom plućnom bolešću (KOPB), zabilježeno je više slučajeva malignih bolesti, uglavnom zahvaćenih pluća ili glave i vrata, u infliksimabu -liječeni bolesnici u odnosu na bolesnike u kontrolnoj skupini.Svi su bolesnici dugo pušili. Stoga je potreban oprez pri procjeni uporabe antagonista TNF -a u bolesnika s KOPB -om, kao i u bolesnika s većim rizikom od malignosti kao teški pušači.
Tumori kože
Melanom i karcinom stanica Merkel zabilježeni su u bolesnika liječenih lijekovima koji inhibiraju TNF, uključujući Simponi (vidjeti dio 4.8). Preporučuju se povremeni pregledi kože, osobito kod pacijenata s čimbenicima rizika za nastanak raka kože.
Kongestivno zatajenje srca (CHF)
Bilo je izvješća o pogoršanju kongestivnog zatajenja srca (CHF) i novim slučajevima CHF -a s antagonistima TNF -a, uključujući Simponi. Neki su slučajevi imali smrtonosni ishod. U kliničkom ispitivanju s drugim antagonistom TNF -a uočeno je pogoršanje kongestivnog zatajenja srca i povećan mortalitet zbog koronarne srčane insuficijencije. Simponi nije ispitivan u bolesnika s CHF -om. Simponi se mora koristiti s oprezom u bolesnika s insuficijencijom. / II) Bolesnike treba pomno pratiti i prekinuti liječenje Simponijem u pacijenata koji imaju nove ili pogoršavajuće simptome zatajenja srca (vidjeti dio 4.3).
Učinci na živčani sustav
Upotreba lijekova koji blokiraju TNF, uključujući Simponi, povezana je s novim pojavama ili pogoršanim slučajevima kliničkih simptoma i / ili radiografskih dokaza o demijelinizirajućim poremećajima središnjeg živčanog sustava, uključujući multiplu sklerozu i periferne demijelinizirajuće poremećaje. poremećaja, dobrobiti i rizike liječenja anti-TNF-om treba pažljivo razmotriti prije početka terapije Simponijem.
U slučaju razvoja ovih stanja treba razmotriti prekid terapije lijekom Simponi (vidjeti dio 4.8).
Kirurške intervencije
Iskustvo sa sigurnošću liječenja Simponijem u pacijenata koji su podvrgnuti operaciji, uključujući artroplastiku, je ograničeno. Prilikom planiranja operacije treba uzeti u obzir dugo poluvrijeme eliminacije. Pacijenta koji treba kirurški zahvat tijekom liječenja lijekom Simponi potrebno je pomno pratiti radi povećanog rizika od infekcija i potrebno je razmotriti odgovarajuće mjere.
Imunosupresija
Postoji mogućnost da lijekovi protiv TNF-a, uključujući Simponi, utječu na obranu domaćina od infekcija i zloćudnih bolesti, jer TNF posreduje upalu i modulira stanične imunološke odgovore.
Autoimune reakcije
Relativni nedostatak TNF -a? uzrokovane anti-TNF terapijom, mogu dovesti do pokretanja autoimunog procesa. Ako pacijent nakon liječenja Simponijem pokaže simptome koji predviđaju sindrom sličan lupusu i pozitivan je na dvolančana DNA antitijela, liječenje Simponijem mora se prekinuti ( vidjeti dio 4.8).
Hematološke reakcije
Postmarketinški slučajevi pancitopenije, leukopenije, neutropenije, aplastične anemije i trombocitopenije zabilježeni su u pacijenata liječenih anti-TNF lijekovima. Citopenije, uključujući pancitopeniju, nisu bile često zabilježene u kliničkim ispitivanjima sa Simponijem. Svim pacijentima treba savjetovati da odmah potraže liječničku pomoć ako razviju kompatibilne znakove ili simptome krvnih diskrazija (npr. Trajna groznica, modrice, krvarenje i blijedilo). U bolesnika s potvrđenim značajnim hematološkim abnormalnostima treba razmotriti prekid terapije Simponijem.
Istodobna primjena antagonista TNF -a i anakinre
Ozbiljne infekcije i neutropenija dogodile su se u kombiniranim kliničkim ispitivanjima anakinre i drugog inhibitora TNF -a, etanercepta, bez dodatne kliničke koristi. S obzirom na prirodu nuspojava uočenih ovom kombiniranom terapijom, slične toksičnosti mogu se pojaviti kod kombinacije anakinre i drugih inhibitora TNF -a. Kombinacija Simponija i anakinre se ne preporučuje.
Istodobna primjena antagonista TNF -a i abatacepta
U kliničkim studijama, kombinirana uporaba TNF-antagonista i abatacepta bila je povezana s povećanim rizikom od infekcija, uključujući ozbiljne infekcije, u usporedbi s antagonistima TNF-a koji su se koristili sami, bez povećanja kliničke koristi. Simponi i abatacept se ne preporučuju.
Istodobna primjena s drugim biološkim terapijama
Nema dovoljno informacija o istodobnoj primjeni Simponija s drugim biološkim terapijama koje se koriste za liječenje istih stanja kao i Simponi. Istodobna uporaba Simponija s ovim biološkim lijekovima ne preporučuje se zbog mogućnosti povećanog rizika od infekcije i drugih potencijalnih interakcija s lijekovima.
Zamjena između bioloških DMARD -ova
Potreban je oprez, a pacijente treba i dalje nadzirati pri promjeni s jednog biološkog na drugi, jer preklapanje biološke aktivnosti može dodatno povećati rizik od nuspojava, uključujući infekciju.
Cijepljenja / infektivna terapijska sredstva
Pacijenti liječeni Simponijem mogu primiti istodobna cijepljenja, isključujući živa cjepiva (vidjeti dijelove 4.5 i 4.6). U pacijenata liječenih anti-TNF terapijom dostupni su ograničeni podaci o odgovoru na cijepljenje, živim cjepivima ili o sekundarnom prijenosu infekcije uz primjenu živih cjepiva. Korištenje živih cjepiva moglo bi dovesti do kliničkih infekcija, uključujući i širenje infekcija .
Druge uporabe zaraznih terapijskih sredstava, poput živih oslabljenih bakterija (na primjer, intravezikalne instilacije s BCG -om za liječenje raka) mogle bi rezultirati kliničkim infekcijama, uključujući diseminirane infekcije. Preporuča se da se terapijski zarazni agensi ne daju istodobno sa Simponijem.
Alergijske reakcije
U razdoblju nakon stavljanja lijeka u promet, nakon primjene Simponija zabilježene su teške reakcije sustavne preosjetljivosti (uključujući anafilaktičku reakciju). Neke od tih reakcija dogodile su se nakon prve primjene Simponija. U slučaju anafilaktičkih ili drugih reakcija alergičnih na teške, primjenu Simponija treba odmah prekinuti i započeti odgovarajuća terapija.
Osjetljivost na lateks
Poklopac igle na napunjenoj olovci ili napunjenoj štrcaljki izrađen je od osušenog prirodnog kaučuka koji sadrži lateks i može izazvati alergijske reakcije kod osoba osjetljivih na lateks.
Posebne populacije
Starije osobe (≥ 65 godina)
U fazama III RA, AP, SA i CU studija nisu primijećene sveukupne razlike u nuspojavama (AE), ozbiljnim nuspojavama (EAG) i ozbiljnim infekcijama u pacijenata starijih od 65 godina koji su primali terapiju. U usporedbi sa Simponijem mlađim pacijentima. Međutim, treba biti oprezan u liječenju starijih osoba, a posebnu pozornost treba posvetiti pojavi infekcija. U aksijalnoj SpA studiji nije bilo pacijenata u dobi od 45 godina ili starijih.
Oštećenje bubrega i jetre
Nisu provedena posebna istraživanja sa lijekom Simponi u bolesnika s oštećenjem bubrega ili jetre. Simponi se mora koristiti s oprezom u osoba s oštećenom funkcijom jetre (vidjeti dio 4.2).
Pedijatrijska populacija
Cijepljenja
Ako je moguće, preporučuje se da pedijatrijski pacijenti prije početka terapije Simponijem budu u dobrom stanju sa svim imunizacijama u skladu s važećim smjernicama za imunizaciju.
Pomoćne tvari
Simponi sadrži sorbitol (E420). Pacijenti s rijetkim nasljednim problemima intolerancije na fruktozu ne smiju uzimati Simponi.
Mogućnost pogrešaka u liječenju
Simponi je registriran u jačini od 50 mg i 100 mg za potkožnu primjenu. Važno je da se za primjenu ispravne doze koristi točna doza kako je navedeno u doziranju (vidjeti dio 4.2). Treba paziti na osiguravanje odgovarajuće doze kako bi se osiguralo da pacijenti nisu predozirani ili predozirani.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Nisu provedena ispitivanja interakcija.
Istodobna primjena s drugim biološkim terapijama
Ne preporučuje se kombinacija Simponija s drugim biološkim terapijama za liječenje istih stanja kao i Simponi, uključujući anakinru i abatacept (vidjeti dio 4.4).
Živa cjepiva / infektivna terapijska sredstva
Živa cjepiva ne smiju se primjenjivati istodobno sa Simponijem (vidjeti dijelove 4.4 i 4.6).
Zarazni terapijski agensi ne smiju se primjenjivati istodobno sa Simponijem (vidjeti dio 4.4).
Metotreksat
Iako istodobna primjena metotreksata (MTX) dovodi do povećanja najnižih koncentracija simponija u ravnotežnom stanju u bolesnika s RA, AP ili AS, podaci ne ukazuju na potrebu prilagođavanja doze Simponija ili MTX -a (vidjeti dio 5.2).
04.6 Trudnoća i dojenje
Žene u reproduktivnoj dobi
Žene u reproduktivnoj dobi moraju koristiti odgovarajuću kontracepciju kako bi spriječile trudnoću i nastaviti je primjenjivati najmanje 6 mjeseci nakon posljednje primjene golimumaba.
Trudnoća
Nema odgovarajućih podataka o uporabi golimumaba u trudnica. Zbog inhibicije TNF -a, primjena golimumaba tijekom trudnoće može utjecati na normalne imunološke reakcije novorođenčeta. Studije na životinjama ne ukazuju na izravne ili štetne učinke. Neizravni učinci na trudnoću embrionalni / fetalni razvoj, porod ili postnatalni razvoj (vidjeti dio 5.3.) Primjena golimumaba se ne preporučuje u trudnica; golimumab se smije davati trudnicama samo kad je to izrazito potrebno.
Golimumab prelazi placentu. Nakon liječenja monoklonskim antitijelima koja inhibiraju TNF tijekom trudnoće, antitijela su pronađena do 6 mjeseci u serumu dojenčadi rođene liječenim ženama, pa stoga ta djeca mogu imati povećan rizik od infekcije.
Primjena živih cjepiva u izložene dojenčadi u maternici golimumab se ne preporučuje 6 mjeseci nakon majčine posljednje injekcije golimumaba tijekom trudnoće (vidjeti dijelove 4.4 i 4.5).
Dojenje
Nije poznato izlučuje li se golimumab u majčino mlijeko ili se sistemski apsorbira nakon gutanja. Pokazano je da golimumab izlučuje u mlijeko majmuna, a budući da se humani imunoglobulini izlučuju u mlijeko, žene ne bi trebale dojiti tijekom liječenja i najmanje 6 mjeseci nakon liječenja golimumabom.
Plodnost
Studije plodnosti s golimumabom nisu provedene na životinjama. Studija plodnosti na miševima koja je koristila slično antitijelo koje selektivno inhibira funkcionalnu aktivnost mišjeg TNF -a nije pokazala relevantne učinke na plodnost (vidjeti dio 5.3).
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Simponi može neznatno umanjiti sposobnost upravljanja vozilima i rada sa strojevima. Nakon primjene Simponija može se pojaviti vrtoglavica (vidjeti dio 4.8).
04.8 Nuspojave
Sažetak sigurnosnog profila
U kontrolnom razdoblju ključnih studija RA, AP, SA, Axial SpA nr i CU, infekcija gornjih dišnih putova bila je najčešća nuspojava (ADR) prijavljena u 12,6% pacijenata liječenih golimumabom. U usporedbi s 11,0% kontrolirati pacijente. Najozbiljniji nuspojave prijavljene za golimumab uključuju teške infekcije (uključujući sepsu, upalu pluća, tuberkulozu, invazivne gljivične infekcije i oportunističke infekcije), demijelinizirajuće bolesti, reaktivaciju HBV-a, CHF, autoimune procese (sindrom sličan lupusu), hematološke reakcije, tešku sistemsku preosjetljivost ( uključujući anafilaktičku reakciju), vaskulitis, limfom i leukemiju (vidjeti dio 4.4).
Tablica s popisom nuspojava
Nuspojave zabilježene u kliničkim ispitivanjima i prijavljene nakon postmarketinške uporabe golimumaba u cijelom svijetu navedene su u Tablici 1. Unutar organskih sustava nuspojave su po učestalosti navedene u sljedećim kategorijama: vrlo česte (≥ 1/10); česte (≥ 1/100,
stol 1
Tablica sa popisom ADR -ova
*: Promatrano s drugim sredstvima za blokiranje TNF -a.
U ovom odjeljku je prosječno trajanje praćenja (približno 4 godine) općenito prikazano za sve primjene golimumaba. Tamo gdje je upotreba golimumaba opisana dozom, srednje trajanje praćenja varira (približno 2 godine za dozu od 50 mg, približno 3 godine za dozu od 100 mg) jer se pacijenti mogu prebacivati između doza.
Opis odabranih nuspojava na lijekove
Infekcije
U kontrolnom razdoblju ključnih studija infekcija gornjih dišnih putova bila je najčešća nuspojava prijavljena u 12,6% pacijenata liječenih golimumabom (incidencija na 100 ispitanika-godina: 60,8; 95% CI: 55,0, 67,1) u usporedbi s 11,0% kontrolnih pacijenata (incidencija na 100 ispitanika godišnje: 54,5; 95% CI: 46,1, 64,0). U kontroliranim i nekontroliranim fazama studija sa medijanom praćenja od približno 4 godine, učestalost infekcija gornjih dišnih putova na 100 subjekt-godina bila je 34,9 događaja; 95% CI: 33,8, 36,0 za bolesnike liječene golimumabom.
U kontrolnom razdoblju ključnih studija infekcije su uočene u 23,0% pacijenata liječenih golimumabom (incidencija na 100 ispitanika: 132,0; 95% CI: 123,3, 141,1) u usporedbi s 20,2% kontrolnih pacijenata (incidencija po 100 predmetnih godina: 122,3; 95% CI: 109,5, 136,2). U kontroliranim i nekontroliranim fazama studija sa medijanom praćenja od približno 4 godine, incidencija na 100 subjekto-godina infekcija bila je 81,1 događaj; 95% CI: 79,5, 82,8 za bolesnike liječene golimumabom.
U kontrolnom razdoblju RA, AP, SA i Axial SpA nr studija, ozbiljne infekcije primijećene su u 1,2% pacijenata liječenih golimumabom i 1,2% kontrolnih pacijenata. Učestalost ozbiljnih infekcija na 100 ispitanih godina tijekom praćenja u kontrolnom razdoblju studija RA, AP, SA i nr-aksijalnog SpA bila je 7,3; 95% CI: 4,6, 11, 1 za skupinu od 100 mg golimumaba, od 2,9; 95% CI: 1,2, 6,0 za skupinu s 50 mg golimumaba i 3,6; 95% CI: 1, 5, 7,0 za skupinu koja je primala placebo. U kontrolnom razdoblju UC ispitivanja indukcije golimumaba uočene su ozbiljne infekcije u 0,8 % pacijenata liječenih golimumabom u odnosu na 1,5% kontrolnih pacijenata. Ozbiljne infekcije zabilježene u pacijenata liječenih golimumabom uključivale su tuberkulozu, bakterijske infekcije uključujući sepsu i upalu pluća, invazivne gljivične infekcije i druge oportunističke infekcije. Neke od ovih infekcija bile su fatalne. U kontroliranim i nekontroliranim dijelovima ključnih studija sa medijanom praćenja do 3 godine, zabilježena je veća učestalost ozbiljnih infekcija, uključujući oportunističke infekcije i tuberkulozu u bolesnika liječenih golimumabom u dozi od 100 mg u odnosu na liječene bolesnike. 50 mg. Učestalost svih teških infekcija na 100 ispitanika bila je 4,1; 95% CI: 3,6, 4,5, za bolesnike liječene golimumabom 100 mg i 2,5; 95% CI: 2,0, 3,1, za bolesnike liječene golimumabom 50 mg.
Maligne neoplazme
Limfom
Učestalost limfoma u pacijenata liječenih golimumabom tijekom ključnih studija bila je veća od očekivane u općoj populaciji. U kontroliranim i nekontroliranim dijelovima ovih studija s medijanom praćenja do 3 godine primijećena je veća učestalost limfoma u bolesnika liječenih golimumabom 100 mg u usporedbi s bolesnicima liječenima golimumabom 50 mg.Limfom je dijagnosticiran u 11 ispitanika (1 u skupinama liječenih golimumabom u dozi od 50 mg i 10 u skupinama liječenih golimumabom u dozi od 100 mg) s incidencijom (95% CI) po 100 predmetnih godina praćenja 0,03 odnosno 0,13 događaja za golimumab 50 mg i golimumab 100 mg, odnosno 0,00 događaja za placebo. Većina limfoma dogodila se u studiji GO-AFTER u koju su uključeni pacijenti koji su prethodno bili izloženi lijekovima protiv TNF-a i s duljim i refraktornijim trajanjem bolesti (vidjeti dio 4.4).
Maligne neoplazme osim limfoma
U kontrolnim razdobljima ključnih studija i otprilike 4 godine praćenja, incidencija malignih bolesti osim limfoma (isključujući nemelanomski rak kože) bila je slična između golimumaba i kontrolnih skupina. Približno 4 godine praćenja, incidencija malignih tumora bez limfoma (isključujući nemelanomski rak kože) bila je slična onoj u općoj populaciji.
U kontroliranim i nekontroliranim razdobljima ključnih studija sa medijanom praćenja do 3 godine, nemelanomski karcinom kože dijagnosticiran je u 5 ispitanika liječenih placebom, 10 liječenih golimumabom 50 mg i 31 lijekom golimumabom 100 mg s incidencija (95% CI) na 100 godina praćenja od 0,36 za kombinirani golimumab i 0,87 za placebo.
U kontroliranim i nekontroliranim razdobljima ključnih studija sa medijanom praćenja do 3 godine, maligni tumori uz melanom, nemelanomski rak kože i limfom dijagnosticirani su u 5 ispitanika liječenih placebom, u 21 liječenih golimumabom 50 mg i u 34 liječenih golimumabom 100 mg s incidencijom (95% CI) na 100 godina praćenja od 0,48 za kombinirani golimumab i 0,87 za placebo (vidjeti dio 4.4).
Slučajevi prijavljeni u kliničkim ispitivanjima u prisutnosti astme
U istraživačkoj kliničkoj studiji, pacijenti s teškom perzistentnom astmom primali su punu dozu golimumaba (150% dodijeljene doze lijeka) potkožno u 0 tjednu, nakon čega je slijedilo 200 mg golimumaba, 100 mg golimumaba ili 50 mg golimumaba. 4 tjedna subkutano tjedan 52. Prijavljeno je osam zloćudnih bolesti u skupini koja je primala kombiniranu terapiju golimumabom (n = 230), a nijedan u skupini koja je primala placebo (n = 79). Limfom je prijavljen u 1 bolesnika, nemelanomski rak kože u 2 bolesnika, a drugi zloćudni tumori u 5 bolesnika. Nije bilo specifičnog spajanja bilo koje vrste malignosti.
U fazi ispitivanja kontroliranom placebom, incidencija (95% CI) svih zloćudnih bolesti na 100 godina praćenja bila je 3,19 u skupini liječenoj golimumabom. Učestalost (95% CI) na 100 ispitanika u godinama praćenja -up je u bolesnika liječenih golimumabom iznosio 0,40 za limfom, 0,79 za nemelanomski rak kože i 1,99 za ostale zloćudne bolesti. Za ispitanike liječene placebom, incidencija (95% CI) ovih zloćudnih bolesti na 100 ispitanika / godina praćenja bila je 0,00. Značaj ovih nalaza nije poznat.
Neurološki događaji
U kontroliranim i nekontroliranim razdobljima ključnih studija sa medijanom praćenja do 3 godine, primijećena je veća učestalost demijelinizacije u bolesnika liječenih golimumabom 100 mg u usporedbi s bolesnicima liječenima golimumabom 50 mg (vidjeti dio 4.4). .
Povećanje jetrenih enzima
U kontrolnim razdobljima ključnih studija RA i AP, blago povišenje ALT (> 1 i 1 i
U kontrolnom razdoblju ključnih studija RA i AS, povišenje ALT-a ≥ 5 puta GGN bilo je rijetko i opaženo je u većem broju pacijenata liječenih golimumabom (0,4%do 0,9%) u usporedbi s kontrolnim bolesnicima (0,0%). Ovaj trend nije primijećen u populaciji AP. U kontroliranim i nekontroliranim razdobljima ključnih studija RA, AP i SA sa medijanom praćenja od 5 godina, incidencija povišenja ALT ≥ 5 puta iznad gornje granice gornje granice bila je slična i za golimumab i za kontrolne bolesnike. Općenito, ta su povišenja bila asimptomatska, a abnormalnosti su se smanjile ili riješile nastavkom ili prekidom uzimanja golimumaba ili promjenom istodobnih lijekova. Nisu zabilježeni slučajevi u kontroliranim i nekontroliranim razdobljima studije Axial SpA. (Do 1 godine) U kontrolnim razdobljima ključnih studija indukcije CU-a s golimumabom, povišene vrijednosti ALT ≥ 5 x GNN uočene su u sličnim stopama u bolesnika liječenih golimumabom i placebom (0,3% do 1,0%).U kontroliranim i nekontroliranim razdobljima ključnih studija UC-a sa medijanom praćenja od približno 2 godine, udio pacijenata s povišenim ALT-om ≥ 5 x GGN bio je 0,8% u bolesnika koji su primali golimumab tijekom održavanja UC studije.
U ključnim studijama RA, AP, SA i Axial SpA, pacijent u studiji RA s već postojećim abnormalnostima jetre i lijekovima zbunjujućeg faktora liječenim golimumabom razvio je smrtonosni neinfektivni hepatitis s žuticom. Ne može se isključiti uloga golimumaba kao čimbenika koji doprinosi ili otežava.
Reakcije na mjestu ubrizgavanja
U kontrolnim razdobljima ključnih studija reakcije na mjestu ubrizgavanja opažene su u 5,4% pacijenata liječenih golimumabom, u usporedbi s 2,0% kontrolnih pacijenata. Prisutnost protutijela na golimumab može povećati rizik od reakcija na mjestu ubrizgavanja. Većina reakcija na mjestu ubrizgavanja bile su blage i umjerene, a najčešće manifestacije su eritem na mjestu ubrizgavanja. Reakcije na mjestu ubrizgavanja općenito ne zahtijevaju prekid liječenja lijekom.
U kontroliranim studijama faze IIb i / ili III u RA, AP, SA, Axial nr SpA, teškoj perzistentnoj astmi iu studijama UC faze II / III, nijedan bolesnik liječen golimumabom nije razvio anafilaktičke reakcije.
Autoimuna antitijela
U kontroliranim i nekontroliranim razdobljima ključnih studija s godinu dana praćenja, 3,5% pacijenata liječenih golimumabom i 2,3% kontrolnih pacijenata imalo je nedavno pozitivnu ANA (titracije 1: 160 ili više). Učestalost anti-dsDNA antitijela nakon jedne godine praćenja u anti-dsDNA negativnih pacijenata na početku je bila 1,1%.
Pedijatrijska populacija
Poliartikularni juvenilni idiopatski artritis
Sigurnost golimumaba proučavana je u studiji III faze na 173 bolesnika s pJIA u dobi od 2 do 17 godina. Prosječno praćenje bilo je približno dvije godine. U ovoj studiji, vrsta i učestalost prijavljenih nuspojava općenito su bili slični onima koji su viđeni u studijama na odraslima s RA.
Prijavljivanje sumnji na nuspojave
Prijavljivanje sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika traži se da prijave svaku sumnju na nuspojavu putem web stranice Talijanske agencije za lijekove: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Predoziranje
U kliničkoj studiji primijenjene su pojedinačne doze do 10 mg / kg intravenozno bez toksičnosti koja ograničava dozu. U slučaju predoziranja, preporuča se da se pacijent prati zbog znakova i simptoma nuspojava i odmah započne odgovarajuće simptomatsko liječenje.
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: imunosupresivi, inhibitori faktora tumorske nekroze (TNF-?), ATC oznaka: L04AB06
Mehanizam djelovanja
Golimumab je ljudsko monoklonsko protutijelo koje tvori stabilne komplekse s visokim afinitetom i za topljive i za bioaktivne transmembranske oblike TNF-? humani, sprječavajući vezivanje TNF-? svojim receptorima.
Farmakodinamički učinci
Pokazalo se da vezanje golimumaba na humani TNF inhibira ljudsku endotelijalnu stanicu induciranu ekspresiju stanične površine induciranom TNF-a staničnom površinom, molekulu adhezije vaskularnih stanica tipa 1 (VCAM) i unutarstaničnu adhezijsku molekulu tipa 1 (ICAM). In vitro, Golimumab je također inhibirao TNF-induciranu sekreciju interleukin (IL) -6, IL-8 i faktor stimulacije kolonije granulocita i makrofaga (GM-CSF).
Uočeno je poboljšanje razine C-reaktivnog proteina (CRP) u usporedbi s placebo skupinama, a liječenje Simponijem rezultiralo je značajnim smanjenjem razine u serumu u odnosu na početnu vrijednost IL-6, ICAM-1, matriks metaloproteinaze.3 (MMP) i vaskularnog endotela faktor rasta (VEGF), u usporedbi s kontrolnim tretmanom. Nadalje, u pacijenata s RA i AS razine TNF-? smanjena, a razina IL-8 smanjena u bolesnika s AP. Te su promjene uočene u prvoj procjeni (4. tjedan) nakon početne primjene Simponija i općenito su trajale do 24. tjedna.
Klinička učinkovitost
Reumatoidni artritis
Učinkovitost lijeka Simponi dokazana je u tri multicentrična, randomizirana, dvostruko slijepa, placebom kontrolirana klinička ispitivanja provedena na više od 1500 pacijenata u dobi od ≥ 18 godina s umjereno do teškim aktivnim RA dijagnosticiranim prema kriterijima American College of Rheumatology (ACR) najmanje 3 mjeseca prije pregleda. Pacijenti su morali imati najmanje 4 otečena i 4 bolna zgloba. Simponi ili placebo davali su se potkožno svaka 4 tjedna.
GO-FORWARD je ocijenio 444 bolesnika s aktivnim RA-om unatoč stabilnoj dozi od najmanje 15 mg / tjedan MTX-a i koji prethodno nisu bili liječeni nikakvim lijekovima protiv TNF-a. Bolesnici su randomizirani na placebo + MTX, Simponi 50 mg + MTX, Simponi 100 mg + MTX ili Simponi 100 mg + placebo. Pacijenti koji su primali placebo + MTX, nakon 24. tjedna, dobili su Simponi 50 mg + MTX. U 52. tjednu pacijenti su ušli u otvorenu dugotrajnu produženu studiju.
GO-AFTER je procijenio 445 pacijenata koji su prethodno bili liječeni jednim ili više lijekova protiv TNF-a, adalimumabom, etanerceptom ili infliksimabom. Bolesnici su randomizirani u placebo, Simponi 50 mg ili Simponi 100 mg. Tijekom ispitivanja, pacijenti su mogli nastaviti istodobnu DMARD terapiju s MTX -om, sulfasalazinom (SSZ) i / ili hidroksiklorokinom (HCQ). Razlozi za prekid prethodne terapije protiv TNF-a bili su nedostatak učinkovitosti (58%), netolerancija (13%) i / ili drugi razlozi osim sigurnosti ili djelotvornosti (29%, uglavnom iz financijskih razloga).
GO-BEFORE je procijenio 637 pacijenata s aktivnom RA, bez MTX-a koji nisu prethodno liječeni anti-TNF lijekovima. Pacijenti su randomizirani da primaju placebo + MTX, Simponi 50 mg + MTX, Simponi 100 mg + MTX ili Simponi 100 mg + placebo. U 52. tjednu pacijenti su ušli u otvorenu dugotrajnu produženu studiju u kojoj su pacijenti koji su primali placebo + MTX i imali najmanje 1 bolan ili natečen zglob premješteni na liječenje Simponijem od 50 mg + MTX.
U GO-FORWARD-u (ko) primarni krajnji rezultati bili su udio pacijenata koji su postigli odgovor na ACR 20 u 14. tjednu i poboljšanje Upitnika za procjenu zdravlja (HAQ) u 24. tjednu od početne vrijednosti. Bio je udio pacijenata koji su postigli odgovor na ACR 20 u 14. tjednu. U GO-BEFORE-u, ko-primarne krajnje točke bile su udio pacijenata koji su postigli odgovor ACR 50 u 24. tjednu i promjenu od početne vrijednosti u modificiranom Sharpovom rezultatu prema van der Heijdeu (vdH-S) u 52. tjednu. Osim primarnih krajnjih točaka, provedene su i dodatne procjene utjecaja liječenja lijekom Simponi na znakove i simptome artritisa, radiografski odgovor, tjelesnu funkciju i kvalitetu života povezanu sa statusom.
Općenito, nisu primijećene klinički značajne razlike u procjenama učinkovitosti između Simponija od 50 mg i 100 mg u kombinaciji s režimima doziranja MTX-a do 104 tjedna u GO-FORWARD i GO-BEFORE i do 24 tjedna u GO-AFTER. u svakoj od studija RA prema dizajnu studije, pacijenti u dugotrajnom produljenju mogli su se prebacivati između doza Simponija od 50 mg i 100 mg prema nahođenju liječnika.
znaci i simptomi
Rezultati ključnih ACR kriterija za dozu Simponija od 50 mg u 14., 24. i 52. tjednu za GO-FORWARD, GO-AFTER i GO-BEF prikazani su u tablici 2 i opisani su u nastavku. Odgovori su viđeni u prvoj procjeni (4. tjedan) nakon početne primjene Simponija.
U GO-FORWARD studiji, od 89 ispitanika randomiziranih na Simponi 50 mg + MTX, 48 je još bilo na liječenju u 104. tjednu. Među njima je 40, 33 i 24 pacijenta imalo odgovor ACR 20/50/70 u 104. tjednu, Među pacijentima koji su ostali u studiji i liječili se Simponijem, slične stope odgovora ACR -a 20/50/70 opažene su od 104. do 256.
U studiji GO-AFTER postotak pacijenata koji su postigli odgovor na ACR 20 bio je veći kod pacijenata liječenih lijekom Simponi u usporedbi s pacijentima koji su primali placebo, bez obzira na prijavljeni razlog za prekid jedne ili više protuupalnih terapija. -TNF.
Tablica 2
Ključni rezultati učinkovitosti iz kontroliranih dijelova studija GO-FORWARD, GO-AFTER i GO-BEFORE
a n odgovara randomiziranim pacijentima; stvarni broj pacijenata koji se mogu ocijeniti za svaku krajnju točku može varirati ovisno o vremenskoj točki.
* p ≤ 0,001
NA: Nije primjenjivo
U studiji GO-BEFORE primarna analiza u pacijenata s umjerenim do teškim reumatoidnim artritisom (kombinacije skupina Simponi 50 i 100 mg + MTX u odnosu na sam MTX za ACR 50) nije bila statistički značajna u 24. tjednu (p = 0.053 U 52. tjednu kroz u populaciji, udio pacijenata u skupini Simponi 50 mg + MTX koji su postigli ACR odgovor općenito je bio veći, ali se nije značajno razlikovao u usporedbi s samim MTX -om (vidjeti tablicu 2.) Dodatne analize podskupina reprezentativne za navedenu populaciju pacijenata s teškim , aktivni i progresivni RA. Općenito superiorni učinak je dokazan sa Simponijem 50 mg + MTX u odnosu na sam MTX u navedenoj populaciji u odnosu na ukupnu populaciju.
U studijama GO-FORWARD i GO-AFTER statistički i klinički značajni odgovori na ljestvici aktivnosti bolesti (DAS28) primijećeni su u svakoj unaprijed određenoj fazi, u 14. i 24. tjednu (p ≤ 0,001). Među pacijentima koji su ostali na liječenju lijekom Simponi, randomiziranim na početku studije, odgovori na DAS28 zadržali su se do 104. tjedna. Među pacijentima koji su ostali u studiji i liječili se lijekom Simponi, odgovori na DAS28 bili su slični od 104. do 256 tjedna.
U studiji GO-BEFORE procijenjen je glavni klinički odgovor definiran kao održavanje odgovora ACR 70 u kontinuiranom razdoblju od 6 mjeseci. U 52. tjednu 15% pacijenata u skupini koja je uzimala Simponi 50 mg + MTX postiglo je vrhunski klinički odgovor u usporedbi sa 7% pacijenata u skupini koja je primala placebo + MTX (p = 0,018). Od 159 ispitanika randomiziranih na Simponi 50 mg + MTX, 96 je još bilo na liječenju u 104. tjednu. Među tih 85, 66 i 53 pacijenata imalo je ACR odgovor 20/50/70 u 104. tjednu, respektivno. I liječeni Simponijem, slično Stope odgovora ACR -a 20/50/70 promatrane su od 104. do 256.
Radiografski odgovor:
U studiji GO-BEFORE za procjenu su korištene promjene u odnosu na početnu vrijednost ocjene vdH-S, kompozitne ocjene strukturnih oštećenja koja radiografski mjeri broj i veličinu zajedničkih erozija i stupanj smanjenja zglobnog prostora u šakama / zapešćima i stopalima stupanj oštećenja konstrukcije. Ključni rezultati za Simponi u dozi od 50 mg u 52. tjednu prikazani su u tablici 3.
Broj pacijenata bez nove erozije ili promjene u odnosu na početnu vrijednost ukupnog vdH-S skora ≤ 0 bio je značajno veći u skupini Simponi nego u kontrolnoj skupini (p = 0,003). Radiografski učinci uočeni u 52. tjednu održavali su se do 104. tjedna. Među pacijentima koji su ostali u studiji i liječeni Simponijem, radiografski učinci bili su slični od 104. do 256.
Tablica 3
Prosječna (SD) radiografska promjena od početne vrijednosti do 52. tjedna u ukupnom rezultatu vdH-S u populaciji ispitanika GO-BEFORE
a n odgovara randomiziranim pacijentima
* p = 0,015
** p = 0,044
Tjelesna funkcija i kvaliteta života povezana sa zdravljem
Tjelesna funkcija i invaliditet ocijenjeni su kao zasebne krajnje točke u studijama GO-FORWARD i GO-AFTER, koristeći HAQ DI indeks invaliditeta. U tim studijama, u 24. tjednu, Simponi je pokazao klinički i statistički značajno poboljšanje HAQ DI u odnosu na početnu vrijednost u usporedbi s kontrolnom skupinom. Među pacijentima koji su ostali na liječenju Simponijem, randomiziranim na početku studije, poboljšanje HAQ DI održavalo se do 104. tjedna Među pacijentima koji su ostali u studiji i liječili se Simponijem, poboljšanje HAQ DI bilo je slično od 104. do 256 tjedna.
Studija GO-FORWARD pokazala je klinički i statistički značajna poboljšanja kvalitete života povezana sa zdravljem, mjerena rezultatom tjelesne komponente SF-36 u bolesnika liječenih lijekom Simponi u odnosu na placebo u 24. tjednu. Među pacijentima koji su ostali na liječenju lijekom Simponi, randomizirani su Pokretanje studije poboljšalo je SF-36 održano do 104. tjedna. Među pacijentima koji su ostali u studiji i liječili se Simponijem, poboljšanje fizičke komponente SF-36 bilo je slično od 104. do 256. tjedna. -NAPRIJED i GO-AFTER studije uočena su statistički značajna poboljšanja umora, prema ljestvici Funkcionalna procjena terapije kroničnih bolesti-umor (FACIT-F).
Psorijatični artritis
Učinkovitost i sigurnost lijeka Simponi ocijenjeni su u multicentričnoj, randomiziranoj, dvostruko slijepoj, placebom kontroliranoj kliničkoj studiji (GO-REVEAL) provedenoj na 405 odraslih pacijenata s aktivnom PA (≥ 3 otečena zgloba i ≥ 3 zgloba bolna), unatoč terapiji s nesteroidnim protuupalnim lijekovima (NSAID) ili DMARD-ovima. Pacijenti u ovoj studiji imali su dijagnozu AP najmanje 6 mjeseci i najmanje blagu psorijazu. Pacijenti sa svakom podvrstom psorijatičnog artritisa, uključujući artritis, bili su upisani poliartikularno bez reumatoida kvržice (43%), asimetrični periferni artritis (30%), distalni artritis interfalangealnog zgloba (DIP) (15%), spondilitis s perifernim artritisom (11%) i sakatni artritis (1%). nema prethodnog liječenja anti-TNF-om Simponi ili placebo davali su se potkožno svaka 4 tjedna. Pacijenti su randomizirani na placebo, Simponi 50 mg ili na S nametnuti 100 mg. Pacijenti koji su primali placebo, nakon 24. tjedna, dobili su Simponi u dozi od 50 mg. U 52. tjednu pacijenti su ušli u dugoročnu otvorenu produženu studiju.
Približno 48% pacijenata nastavilo je sa stabilnim dozama metotreksata (≤ 25 mg / tjedan). Ko-primarne krajnje točke bile su udio pacijenata koji su postigli odgovor na ACR 20 u 14. tjednu i promjena u odnosu na početnu vrijednost u modificiranom ukupnom skoru AP vdH-S u 24. tjednu.
Općenito, nisu primijećene klinički značajne razlike u mjerama učinkovitosti između režima doziranja Simponija od 50 mg i 100 mg do 104. tjedna. Prema dizajnu studije, pacijenti u dugotrajnom produljenju mogli bi proći prijelaz između Simponija od 50 mg i 100 mg doze prema nahođenju liječnika ispitivača.
znaci i simptomi
Ključni rezultati za dozu od 50 mg u 14. i 24. tjednu prikazani su u tablici 4. i opisani su u nastavku.
Tablica 4
Ključni rezultati učinkovitosti iz studije GO-REVEAL
* str
a n odgovara randomiziranim pacijentima; stvarni broj pacijenata koji se mogu ocijeniti za svaku krajnju točku može varirati ovisno o vremenskoj točki
b Indeks područja i težine psorijaze
c Na temelju podskupine pacijenata s uključenom tjelesnom površinom (BSA) ≥ 3%na početku, 79 pacijenata (69,9%) u skupini koja je primala placebo i 109 (74,3%) u lijeku Simponi 50 mg.
Odgovori su uočeni pri prvoj procjeni (4. tjedan) nakon početne primjene Simponija. Slični odgovori ACR 20 viđeni su u 14. tjednu u bolesnika s poliartikularnim artritisom u odsutnosti reumatoidnih čvorića i podtipova AP, asimetričnog perifernog artritisa. Broj pacijenata s drugim podtipovima PA bio je premali da bi se omogućila smislena procjena.Odgovori primijećeni u skupinama liječenih lijekom Simponi bili su slični u bolesnika liječenih ili ne s istodobnim MTX -om. Od 146 pacijenata randomiziranih na 50 mg lijeka Simponi, 70 ih je još bilo na liječenju u 104. tjednu. Među tih 70 pacijenata, 64, 46 i 31 pacijent imali su ACR odgovor 20/50/70. Među pacijentima koji su ostali u studiji i liječili se Simponijem, slične stope odgovora ACR 20/50/70 opažene su od 104. do 256 tjedna.
Statistički značajni odgovori primijećeni su i u DAS28 u 14. i 24. tjednu (str
U 24. tjednu primijećeno je poboljšanje parametara periferne aktivnosti tipično za psorijatični artritis (npr. Broj natečenih zglobova, broj osjetljivih zglobova, daktilitis i entezitis) u bolesnika liječenih lijekom Simponi. Liječenje Simponijem rezultiralo je značajnim poboljšanjem tjelesne funkcije prema procjeni HAQ DI-a i značajnim poboljšanjem kvalitete života povezanog sa zdravljem na temelju sažetih rezultata fizičkih i mentalnih komponenti SF-36 na liječenju Simponijem, u koje su randomizirani na početku studije, odgovori DAS28 i HAQ DI održavali su se kroz 104. tjedan. Među pacijentima koji su ostali u studiji i liječeni Simponijem, odgovori DAS28 i HAQ DI bili su slični. od 104. do 256 tjedna.
Radiografski odgovor:
Strukturna oštećenja šaka i stopala radiološki su procijenjena promjenom vdH-S skoka u odnosu na početnu vrijednost, modificiranom za AP uz dodatak distalnih interfalangealnih zglobova (DIP) šake.
Liječenje Simponijem u dozi od 50 mg smanjuje brzinu progresije oštećenja perifernih zglobova u usporedbi s liječenjem placebom u 24. tjednu, mjereno kao promjena u odnosu na početnu vrijednost u izmijenjenom ukupnom rezultatu vdH -S (srednja vrijednost ± SD bila je 0,27 ± 1,3 u skupini koja je primala placebo u usporedbi s - 0,16 ± 1,3 u skupini Simponi; p = 0,011). Od 146 pacijenata koji su randomizirani na Simponi u dozi od 50 mg, rentgenski podaci u 52. tjednu bili su dostupni za 126 pacijenata, od kojih 77% nije pokazalo napredovanje od početne vrijednosti. U 104. tjednu rentgenski podaci bili su dostupni za 114 pacijenata, a 77% nije pokazalo napredovanje od početne vrijednosti. Među pacijentima koji su ostali u studiji i liječili se Simponijem, sličan udio pacijenata nije pokazao napredovanje od početne vrijednosti od 104. do 256 tjedna.
Aksijalni spondiloartritis
Ankilozantni spondilitis
Učinkovitost i sigurnost lijeka Simponi procijenjeni su u multicentričnoj, dvostruko slijepoj, randomiziranoj, placebom kontroliranoj kliničkoj studiji (GO-RAISE) provedenoj na 356 odraslih pacijenata s aktivnim ankilozirajućim spondilitisom (definiranim kao patološka aktivnost ankilozirajućeg spondilitisa prema Indeksu Bath (BASDAI) ) ≥ 4 i VAS za ukupne bolove u leđima ≥ 4 na skali od 0 do 10 cm). Pacijenti uključeni u ovo ispitivanje imali su bolest u aktivnoj fazi, unatoč trenutnoj ili prethodnoj terapiji NSAID-ima ili DMARD-ima, a prethodno nisu bili liječeni nikakvim anti-TNF lijekovima. Simponi ili placebo davali su se potkožno svaka 4 tjedna. Bolesnici su randomizirani na placebo, Simponi 50 mg ili Simponi 100 mg te su mogli nastaviti istodobnu DMARD terapiju (MTX, SSZ i / ili HCQ). Primarni krajnji cilj bio je postotak pacijenata s odgovorom Studijske skupine za procjenu ankilozirajućeg spondilitisa (ASAS 20) u 14. tjednu. Podaci o učinkovitosti kontrolirani placebom prikupljani su i analizirani do 24. tjedna.
Ključni rezultati za dozu od 50 mg prikazani su u tablici 5. i opisani su u nastavku. Općenito, nisu uočene klinički značajne razlike u mjerama učinkovitosti između režima doziranja Simponija od 50 mg i 100 mg do 24. tjedna. Prema dizajnu studije, pacijenti u dugotrajnom produljenju mogli bi se podvrgnuti prelasku sa Simponija u dozi od 50 mg i 100 mg doze prema nahođenju liječnika ispitivača.
Tablica 5
Ključni rezultati učinkovitosti iz studije GO-RAISE
* p ≤ 0,001 za sve usporedbe
a n odgovara randomiziranim pacijentima; stvarni broj pacijenata koji se mogu ocijeniti za svaku krajnju točku može varirati ovisno o vremenskoj točki
Među pacijentima koji su ostali u studiji i liječili se Simponijem, udio pacijenata s odgovorom na ASAS 20 i ASAS 40 bio je sličan od 24. do 256 tjedna.
Statistički značajni odgovori primijećeni su i u BASDAI 50, 70 i 90 (p ≤ 0,017) u 14. i 24. tjednu. Poboljšanja u mjerenjima aktivnosti ključnih bolesti nađena su pri prvoj procjeni (4. tjedan) nakon početne primjene Simponija, koja su se održavala kroz tjedan 24. Među pacijentima koji su ostali u studiji i liječili se lijekom Simponi, slične stope promjena u odnosu na početnu vrijednost primijećene su u BASDAI -u od 24. do 25. tjedna. Dosljedna učinkovitost primijećena je kod pacijenata bez obzira na upotrebu DMARD -a (MTX, sulfasalazin i / ili hidroksiklorokin), prisutnost antigena HLA-B27 ili početne razine CRP-a na temelju procjene odgovora ASAS 20 u 14. tjednu.
Liječenje Simponijem dovelo je do značajnih poboljšanja fizičke funkcije, što je procijenjeno promjenama u odnosu na početne vrijednosti funkcionalnog indeksa ankilozirajućeg spondilitisa u kupelji (BASFI) u 14. i 24. tjednu. Kvaliteta života povezana sa zdravljem, mjerena rezultatom komponente. poboljšalo se u 14. i 24. tjednu. Među pacijentima koji su ostali u studiji i liječili se Simponijem, poboljšanja fizičke funkcije i kvalitete života povezana sa zdravljem bila su slična od 24. do 256 tjedna.
Neradiografski aksijalni spondiloartritis
Sigurnost i djelotvornost lijeka Simponi ocijenjeni su u multicentričnoj, randomiziranoj, dvostruko slijepoj, placebom kontroliranoj studiji (GO-AHEAD) provedenoj na 197 odraslih pacijenata s teškim aksijalnim SpA nr u aktivnoj fazi (definirano kao oni pacijenti koji su zadovoljili ASAS klasifikaciju kriteriji za dijagnozu aksijalnog spondiloartritisa, ali nisu zadovoljili modificirane newyorške kriterije za dijagnozu AS.) Pacijenti uključeni u ovu studiju imali su aktivnu bolest (definiranu BASDAI ≥ 4 i vizualnom analognom ljestvicom (VAS) za ukupnu bol u leđima ≥ 4, svaki na ljestvici od 0 do 10 cm) unatoč tekućoj ili prethodnoj terapiji nesteroidnim protuupalnim lijekovima i prethodno nisu bili liječeni bilo kojim biološkim sredstvom, uključujući anti TNF. Pacijenti su randomizirani na placebo ili Simponi u dozi od 50 mg koja se primjenjuje potkožno svaka 4 tjedna. U tjednu 16, ušli su pacijenti otvoreno razdoblje liječenja u kojem su svi primili Simponi 50 mg primijenjeno potkožno svaka 4 tjedna do 48. tjedna s procjenama učinkovitosti provedenim do 52. tjedna i praćenjem sigurnosti do 60. tjedna. Približno 93% pacijenata koji su primali Simponi na početku otvoreni nastavak (16. tjedan) ostao je na liječenju do kraja studije (52. tjedan). Analize su provedene i na cijeloj tretiranoj populaciji (AT, N = 197) i na populaciji s objektivnim znakovima upale (OSI, N = 158, na što ukazuju visoke razine CRP -a i / ili "dokazi o sakroileitisu na magnetskoj rezonanciji" Podaci o učinkovitosti kontrolirani placebom prikupljeni su i analizirani do 16. tjedna. Primarna krajnja točka bila je udio pacijenata koji su postigli odgovor na ASAS 20 u 16. tjednu. Ključni rezultati prikazani su u tablici 6. i opisani su u nastavku.
Tablica 6
Ključni rezultati učinkovitosti iz GO-AHEAD studije u 16. tjednu
a n odgovara randomiziranim i liječenim pacijentima
b Ankilozirajući spondilitis Ocjena aktivnosti bolesti C-reaktivnog proteina (AT-Placebo, N = 90; AT-Simponi 50 mg, N = 88; OSI-Placebo, N = 71; OSI-Simponi 50 mg, N = 71)
c n odgovara broju pacijenata s početnim i 16. tjednim podacima magnetske rezonancije
d SPARCC (Kanadski konzorcij za istraživanje spondiloartritisa)
** p u odnosu na placebo
* p vs placebo
Statistički značajno poboljšanje znakova i simptoma teške aktivne faze nr aksijalnog SpA pokazano je u bolesnika liječenih Simponijem u dozi od 50 mg u usporedbi s placebom u 16. tjednu (Tablica 6). Poboljšanja su vidljiva pri prvoj procjeni (4. tjedan) nakon početne primjene Simponija. SPARCC MRI rezultat pokazao je statistički značajno smanjenje upale u SI zglobu u 16. tjednu u bolesnika liječenih Simponijem u dozi od 50 mg u usporedbi s placebom (Tablica 6). Bol procijenjen prema VAS-ovoj ukupnoj boli u leđima i noćnim bolovima u leđima te aktivnosti bolesti izmjerene ASDAS-C također su pokazale statistički značajno poboljšanje od početne do 16. tjedna u bolesnika liječenih Simponijem u dozi od 50 mg u usporedbi s placebom (str.
Statistički značajna poboljšanja u pokretljivosti kralježnice prema BASMI -u (Metrološki indeks ankilozirajućeg spondilitisa u kadi) i u tjelesnoj funkciji prema BASFI -u pokazala su se u bolesnika liječenih Simponijem u dozi od 50 mg u usporedbi s bolesnicima liječenima placebom (str.
Za sve gore opisane krajnje točke, statistički značajni rezultati također su pokazani u populaciji OSI u 16. tjednu.
I u populaciji AT i OSI poboljšanja u znakovima i simptomima, pokretljivosti kralježnice, tjelesnoj funkciji, kvaliteti života i produktivnosti uočena u 16. tjednu kod pacijenata liječenih Simponijem u dozi od 50 mg zadržala su se u onih pacijenata koji su ostali u studiji u 52. tjednu.
Ulcerozni kolitis
Učinkovitost lijeka Simponi ocijenjena je u dva randomizirana, dvostruko slijepa, placebom kontrolirana klinička ispitivanja na odraslim pacijentima.
U indukcijskom ispitivanju (PURSUIT-Induction) ocjenjivani su pacijenti s umjerenim do teškim aktivnim ulceroznim kolitisom (Mayo skor 6 do 12; endoskopski pod-skor ≥ 2) koji su imali neadekvatan odgovor ili koji nisu podnosili konvencionalne terapije ili su ovisni o kortikosteroidima. U dijelu ispitivanja potvrde doze 761 je bolesnik randomiziran za primanje Simponija SC 400 mg u tjednu 0 i 200 mg u tjednu 2, Simponija SC 200 mg u tjednu 0 i 100 mg u tjednu 2 ili placebo SC u tjednu 0 i 2. Dopuštena je istodobna primjena stabilnih doza oralnih aminosalicilata, kortikosteroida i / ili imunomodulacijskih sredstava. U ovoj je studiji ocijenjena učinkovitost Simponija do 6. tjedna.
Rezultati studije održavanja (PURSUIT-Maintenance) temeljili su se na procjeni 456 pacijenata koji su postigli klinički odgovor u prethodnoj indukciji Simponija. Pacijenti su randomizirani da primaju Simponi 50 mg, Simponi 100 mg ili placebo primijenjen potkožno svaka 4 tjedna. Dopuštena je istodobna primjena stabilnih doza oralnih aminosalicilata i / ili imunomodulacijskih sredstava. Kortikosteroide je trebalo postupno smanjivati na početku studije održavanja.Učinkovitost lijeka Simponi u ovoj je studiji procjenjivana do 54. tjedna. Pacijenti koji su završili studiju održavanja do 54. tjedna nastavili su liječenje u jednoj studiji. Produženje, s ocjenom učinkovitosti do 216. tjedna. Procjena učinkovitosti u produženoj studiji temeljila se na promjenama u upotrebi kortikosteroida, liječničkoj globalnoj procjeni (PGA) aktivnosti bolesti i poboljšanju kvalitete života mjerenom Upitnikom o upalnoj bolesti crijeva (IBDQ).
Tablica 7
Ključni rezultati učinkovitosti iz studija PURSUIT - Induction and PURSUIT - Maintenance
N = broj pacijenata
** p ≤ 0,001
* p ≤ 0,01
a Definirano kao smanjenje u odnosu na početnu vrijednost Mayo ocjene za ≥ 30% i ≥ 3 boda, popraćeno smanjenjem podrekordalnog krvarenja rektalnog krvarenja ≥ 1 ili podrekordera rektalnog krvarenja od 0 ili 1.
b Definirano kao Mayo rezultat ≤ 2 boda, bez pojedinačnih pod bodova> 1
c Definirano kao 0 ili 1 u endoskopskom pod-skoru Mayo partiture.
d Indukcija samo sa Simponijem.
e Pacijente su procjenjivali na aktivnost CU -a s djelomičnim rezultatom Mayo svaka 4 tjedna (gubitak odgovora potvrđen je endoskopijom). Stoga je jedan pacijent koji je održavao odgovor bio u stanju kontinuiranog kliničkog odgovora pri svakoj kliničkoj procjeni do 54. tjedna.
f Pacijent je morao biti u remisiji u 30. i 54. tjednu (bez gubitka odgovora u bilo kojem trenutku do 54. tjedna) da bi postigao trajnu remisiju.
g U pacijenata s tjelesnom težinom manjom od 80 kg, veći udio pacijenata koji su primali terapiju održavanja od 50 mg pokazao je trajnu kliničku remisiju od onih koji su primali placebo.
Više pacijenata liječenih Simponijem pokazalo je trajno zacjeljivanje sluznice (pacijenti sa zacjeljivanjem sluznice u 30. i 54. tjednu) u skupini od 50 mg (42%, nominalno p
Među 54% pacijenata (247/456) koji su primali istodobnu terapiju kortikosteroidima na početku PURSUIT-održavanja, udio pacijenata koji su zadržali klinički odgovor do 54. tjedna i nisu primali istodobnu terapiju kortikosteroidima na početku PURSUIT-održavanja 54. tjedan bio je veći u skupini od 50 mg (38%, 30/78) i u skupini od 100 mg (30%, 25/82) u usporedbi s placebom (21%, 18/87). Udio pacijenata koji su eliminirali kortikosteroide do 54. tjedna bili su veći u skupini koja je uzimala 50 mg (41%, 32/78) i u skupini od 100 mg (33%, 27/82) u usporedbi s placebom (22%, 19/87). nakon produžene studije, udio ispitanika koji su ostali bez kortikosteroida općenito se održavao do 216. tjedna.
U 6. tjednu Simponi je značajno poboljšao kvalitetu života mjerenu promjenom u odnosu na početnu vrijednost u mjeri za bolest specifičnoj, IBDQ (Upalni upitnik o bolesti crijeva). Među pacijentima koji su primali terapiju održavanja sa Simponijem, poboljšanje kvalitete života mjereno pomoću IBDQ-a održavao se do 54. tjedna.
Približno 63% pacijenata koji su primali lijek Simponi na početku produljene studije (56. tjedan) ostalo je na liječenju do kraja studije (posljednja primjena golimumaba u 212. tjednu).
Imunogenost
U fazama III RA, AP i SA studija do 52. tjedna, antitijela na golimumab otkrivena su imunološkim testom enzima (EIA) u 5% (105/2062) pacijenata liječenih golimumabom, a gdje su testirana, gotovo su sva antitijela neutralizirana in vitro. Slični postoci istaknuti su u reumatološkim indikacijama. Istodobna primjena MTX-a rezultirala je manjim postotkom pacijenata s antitijelima na golimumab od pacijenata koji su primali golimumab bez MTX-a (približno 3% [41/1235] naspram 8% [64/827], respektivno).
U aksijalnom SpA nr, antitijela na golimumab otkrivena su u 7% (14/193) pacijenata liječenih golimumabom do 52. tjedna pomoću EIA testa.
U UC studijama II i III faze do 54. tjedna, antitijela na golimumab otkrivena su EIA testom u 3% (26/946) pacijenata liječenih golimumabom. Šezdeset osam posto (21/31) pacijenata pozitivnih na antitijela imalo je neutralizirajuća antitijela in vitro. Istodobno liječenje imunomodulatorima (azatioprin, 6-merkaptopurin i MTX) rezultiralo je manjim postotkom pacijenata s antitijelima na golimumab nego u bolesnika koji su primali golimumab bez imunomodulatora (1% (4/308) naspram 3% (22)). 638)). Među pacijentima koji su nastavili produljeno ispitivanje i imali uzorke koji su se mogli ocijeniti do 228. tjedna, antitijela na golimumab otkrivena su u 4% (23/604) pacijenata liječenih golimumabom. Osamdeset dva posto (18/22) pacijenata pozitivnih na antitijela imalo je neutralizirajuća antitijela in vitro.
EIA test tolerantan na lijekove korišten je u pJIA studiji za otkrivanje antitijela protiv golimumaba.S obzirom na povećanu osjetljivost i poboljšanu toleranciju na lijekove, očekivalo se da će se s EIA testom tolerantnom na lijekove otkriti veća incidencija antitijela protiv golimumaba u usporedbi s EIA testom. U ispitivanju pIA III faze do 48. tjedna, antitijela na golimumab otkrivena su EIA testom tolerantnim na lijekove u 40% (69/172) djece liječene golimumabom, od kojih je većina imala titar manji od 1: 1.000. Učinak na koncentraciju golimumaba u serumu viđen je pri titrima> 1: 100, dok se nije vidio učinak na učinkovitost do titra> 1: 1.000, iako je broj djece s titrima> 1: 1.000 bio nizak (N = 8). djeca koja su bila pozitivna na antitijela protiv golimumaba, 39% (25/65) imalo je neutralizirajuća antitijela. Veća incidencija antitijela s EIA testom tolerantnom na lijekove, s obzirom na to da su uglavnom bila protutijela na niske titre, nije imala očit utjecaj na razinu lijeka, učinkovitosti i sigurnosti te stoga ne predstavlja nikakve nove sigurnosne signale.
Prisutnost protutijela na golimumab može povećati rizik od reakcija na mjestu ubrizgavanja (vidjeti dio 4.4). Mali broj pacijenata pozitivnih na protutijela na golimumab ograničava sposobnost donošenja čvrstih zaključaka o odnosu između protutijela protiv golimumaba i kliničke učinkovitosti ili sigurnosnih mjera.
Budući da su ispitivanja imunogenosti specifična za proizvod i test, usporedba postotaka antitijela s onima drugih proizvoda nije prikladna.
Pedijatrijska populacija
Poliartikularni juvenilni idiopatski artritis
Sigurnost i djelotvornost lijeka Simponi procijenjeni su u randomiziranoj, dvostruko slijepoj, placebom kontroliranoj studiji suspenzije (GO-KIDS) na 173 djece (od 2 do 17 godina) s aktivnom pJIA s najmanje 5 aktivnih zglobova i neodgovarajućom. odgovor na MTX. U studiju su bila uključena djeca s poliartikularnim tijekom JIA -e (pozitivan ili negativan poliartritis s reumatoidnim faktorom, ekstenzivni oligoartritis, juvenilni psorijatični artritis ili sustavna JIA bez stalnih sistemskih simptoma). Srednji broj aktivnih zglobova na početku bio je 12 a medijan CRP -a bio je 0,17 mg / dL.
Dio 1 studije uključivao je otvorenu fazu od 16 tjedana u kojoj je 173 upisane djece primalo Simponi 30 mg / m2 (maksimalno 50 mg) potkožno svaka 4 tjedna i MTX. 154 djece koja su postigla odgovor na ACR Ped 30 u 16. tjednu ušla su u dio 2 studije, randomiziranu fazu odvikavanja, i primala su Simponi 30 mg / m2 (maksimalno 50 mg) + MTX ili placebo + MTX svaki. 4 tjedna. Nakon izbijanja bolesti, djeca su primala Simponi 30 mg / m2 (maksimalno 50 mg) + MTX. U 48. tjednu bebe su ušle u fazu dugotrajnog produženja.
Djeca u ovoj studiji pokazala su ACR Ped 30, 50, 70 i 90 odgovore već u 4. tjednu.
U 16. tjednu 87% djece je odgovaralo na ACR Ped 30, a 79%, 66%, a 36% djece na ACR Ped 50, ACR Ped 70, odnosno ACR Ped 90. U 16. tjednu 34 % djece imalo je neaktivnu bolest definiranu prisutnošću svega od navedenog: odsutnost zglobova s aktivnim artritisom; odsutnost vrućice, osip, serositis, splenomegalija, hepatomegalija ili generalizirana limfadenopatija koja se može pripisati JIA; odsutnost aktivnog uveitisa; Normalni ESR (
U 16. tjednu sve komponente ACR Ped pokazale su klinički značajno poboljšanje u odnosu na početnu vrijednost (vidi tablicu 8).
Tablica 8
Poboljšanja u odnosu na početnu vrijednost u ACR Ped komponentama u 16. tjednu
na početku = tjedan 0
b "n" odražava upisane pacijente
c VAS: Vizualna analogna ljestvica
d CHAQ: Upitnik za procjenu zdravstvenog stanja djeteta
i ESR (mm / h): brzina sedimentacije eritrocita (milimetri na sat)
Primarni krajnji cilj studije, postotak djece koja su bila odgovor na ACR Ped 30 u 16. tjednu i koja nisu doživjela egzacerbaciju između 16. i 48. tjedna, nije ispunjena. Većina djece nije imala pogoršanje. 16. i 48. tjedan (59% u skupini Simponi + MTX, odnosno 53% u skupini koja je primala placebo + MTX; p = 0,41).
Unaprijed specificirana analiza podgrupe primarne krajnje točke na temelju osnovnih vrijednosti CRP-a (≥ 1 mg / dL vs
U 48. tjednu 53%, odnosno 55% djece u skupini koja je primala Simponi + MTX, odnosno placebo + MTX skupini, bili su odgovori na ACR Ped 30, a 40% i 28% djece u skupini Simponi + MTX i placebo + MTX je postigao neaktivnu bolest.
Europska agencija za lijekove odgodila je obvezu podnošenja rezultata studija sa lijekom Simponi u pedijatrijskoj populaciji s ulceroznim kolitisom (za informacije o pedijatrijskoj uporabi vidjeti dio 4.2).
05.2 Farmakokinetička svojstva
Apsorpcija
Nakon jednokratne "potkožne primjene golimumaba zdravim subjektima ili bolesnicima s RA, prosječno vrijeme za postizanje maksimalnih serumskih koncentracija (Tmax) kretalo se od 2 do 6 dana. Injekcija od 50 mg potkožnog golimumaba u zdravih ispitanika rezultirala je srednjom maksimalnom koncentracijom u serumu (Cmax) ± standardna devijacija od 3,1 ± 1,4 mcg / mL.
Nakon jedne potkožne injekcije od 100 mg, apsorpcija golimumaba bila je slična u ruci, trbuhu i bedru, sa prosječnom apsolutnom bioraspoloživošću od 51%. Potkožno se očekuje da će apsolutna bioraspoloživost doze od 50 mg ili 200 mg golimumaba biti slična.
Distribucija
Nakon jednokratne IV primjene, srednji volumen distribucije bio je 115 ± 19 mL / kg.
Uklanjanje
Sistemski klirens golimumaba procijenjen je na 6,9 ± 2,0 ml / dan / kg. Procjenjuje se da je terminalno poluvrijeme bilo oko 12 ± 3 dana u zdravih ispitanika, a imalo je slične vrijednosti u bolesnika s RA, AP, SA ili CU.
Kad se doza od 50 mg golimumaba primjenjivala potkožno bolesnicima s RA, AP ili AS svaka 4 tjedna, serumske koncentracije dosegle su stanje ravnoteže do 12. tjedna. Uz istodobnu primjenu MTX -a, liječenje golimumabom 50 mg potkožno svaka 4 tjedna proizvelo je prosjek (± standardna devijacija) najniža serumska koncentracija u stanju ravnoteže od približno 0,6 ± 0,4 μg / mL u bolesnika s aktivnim RA unatoč terapiji MTX -om, približno 0,5 ± 0,4 μg / mL u bolesnika s aktivnim AP -om i približno 0,8 ± 0,4 μg / mL u bolesnici s AS. Prosječne najniže koncentracije Golimumaba u serumu u bolesnika s aksijalnom SpA nr bile su slične onima koje su primijećene u AS pacijenata nakon potkožne primjene 50 mg golimumaba svaka 4 tjedna.
Bolesnici s RA, AP ili SA koji nisu primali istodobno primijenjeni MTX imali su najniže koncentracije golimumaba u stanju ravnoteže približno 30% niže od onih u pacijenata koji su primali golimumab s MTX-om. U ograničenom broju pacijenata s RA koji su liječeni golimumabom potkožno dulje od 6 mjeseci, istodobna primjena MTX-a smanjila je prividni klirens golimumaba za približno 36%. Međutim, populacijske farmakokinetičke analize ukazuju da istodobna primjena NSAID -a, oralnih kortikosteroida ili sulfasalazina nije utjecala na prividni klirens golimumaba.
Nakon indukcijskih doza od 200 mg i 100 mg golimumaba u 0, odnosno 2. tjednu, te nakon toga doze održavanja od 50 mg ili 100 mg golimumaba potkožno svaka 4 tjedna u pacijenata s UK, koncentracije golimumaba u serumu dosegle su stanje ravnoteže približno 14 tjedana nakon početka Liječenje golimumabom od 50 mg ili 100 mg potkožno svaka 4 tjedna tijekom održavanja rezultiralo je srednjom najnižom koncentracijom u serumu u ravnotežnom stanju od približno 0, 9 ± 0,5 mcg / mL odnosno 1,8 ± 1,1 mcg / mL.
U UC bolesnika liječenih golimumabom 50 mg ili 100 mg potkožno svaka 4 tjedna, istodobna primjena imunomodulatora nije imala značajan učinak na najniže razine golimumaba u stanju dinamičke ravnoteže.
Pacijenti koji su razvili protutijela protiv golimumaba imali su uglavnom niske najniže koncentracije golimumaba u serumu u ravnotežnom stanju (vidjeti dio 5.1).
Linearnost
Golimumab je u bolesnika s RA pokazao približno proporcionalne dozi farmakokinetičke parametre u rasponu doza od 0,1 - 10,0 mg / kg nakon pojedinačne intravenske doze. Nakon jedne doze SC u zdravih ispitanika Približno su proporcionalni farmakokinetički parametri primijećeni i u rasponu doza od 50 mg do 400 mg.
Učinak težine na farmakokinetiku
Postoji trend povećanja očitog klirensa golimumaba s povećanjem tjelesne težine (vidjeti dio 4.2).
Pedijatrijska populacija
Farmakokinetika golimumaba utvrđena je u 173 djece s pJIA u dobi od 2 do 17 godina. U studiji pJIA, djeca koja su liječena golimumabom 30 mg / m2 (maksimalno 50 mg) potkožno svaka 4 tjedna imala su medijane najnižih koncentracija golimumaba u stanju dinamičke ravnoteže koje su bile slične u dobnim skupinama i koje su također bile slične ili malo veće od onih zabilježenih u odraslih RA bolesnici liječeni golimumabom 50 mg svaka 4 tjedna.
Populacijski farmakokinetički / farmakodinamički modeli i simulacije u djece s pJIA potvrdili su vezu između izloženosti golimumabu u serumu i kliničke učinkovitosti te potvrđuju da golimumab u dozi od 50 mg svaka 4 tjedna u djece s pJIA -om težine najmanje 40 kg omogućuje postizanje izloženosti sličnih onima koje pokazali su se učinkovitima kod odraslih.
05.3 Pretklinički podaci o sigurnosti
Neklinički podaci ne otkrivaju nikakvu posebnu opasnost za ljude na temelju konvencionalnih studija farmakološke sigurnosti, toksičnosti pri ponovljenim dozama, reproduktivne i razvojne toksičnosti.
Studije mutagenosti, plodnosti životinja ili dugotrajne karcinogenosti nisu provedene s golimumabom.
U studiji plodnosti miša i opće reproduktivne funkcije koja je koristila slično antitijelo koje selektivno inhibira funkcionalnu aktivnost mišjeg TNFa, broj trudnih miševa je smanjen. Nije poznato jesu li ti rezultati posljedica učinaka na mužjake i / ili U evolucijskoj studiji toksičnosti provedenoj na miševima nakon primjene istog analognog antitijela i na majmunima cynomolgus koji su koristili golimumab, nije bilo naznaka toksičnosti za majku, embriotoksičnosti ili teratogenosti.
06.0 FARMACEUTSKI PODACI
06.1 Pomoćne tvari
Sorbitol (E420)
L-histidin
L-histidin monohidroklorid monohidrat
Polisorbat 80
Voda za injekcije.
06.2 Nekompatibilnost
U nedostatku studija kompatibilnosti, ovaj lijek se ne smije miješati s drugim proizvodima.
06.3 Razdoblje valjanosti
22 mjeseca
06.4 Posebne mjere pri skladištenju
Čuvati u hladnjaku (2 ° C - 8 ° C).
Nemojte zamrzavati.
Napunjenu olovku ili napunjenu štrcaljku čuvajte u vanjskom pakiranju radi zaštite od svjetlosti.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
Simponi 50 mg otopina za injekciju u napunjenoj olovci
0,5 mL otopine u napunjenoj štrcaljki (staklo tipa 1) s fiksnom iglom (nehrđajući čelik) i poklopcem igle (guma koja sadrži lateks), u napunjenoj olovci. Simponi je dostupan u pakiranjima koja sadrže 1 napunjenu injekciju olovka i više pakiranja koja sadrže 3 (3 pakiranja od 1) napunjene olovke.
Simponi 50 mg otopina za injekciju u napunjenoj štrcaljki
0,5 ml otopine u napunjenoj štrcaljki (staklo tipa 1) s fiksnom iglom (nehrđajući čelik) i zatvaračem za iglu (guma koja sadrži lateks). Simponi je dostupan u pakiranjima koja sadrže 1 napunjenu štrcaljku i više pakiranja koja sadrže 3 (3 pakiranja od 1) napunjene štrcaljke.
Ne mogu se na tržište staviti sve veličine pakiranja.
06.6 Upute za uporabu i rukovanje
Simponi se isporučuje u napunjenoj jednokratnoj olovci pod nazivom SmartJect ili u napunjenoj štrcaljki za jednokratnu uporabu. Svako pakiranje Simponija dolazi s uputama za uporabu koje u potpunosti opisuju kako koristiti olovku ili štrcaljku. Nakon što se napunjena brizgalica ili napunjena štrcaljka izvade iz hladnjaka, treba je ostaviti da dosegne sobnu temperaturu čekajući 30 minuta prije ubrizgavanja Simponija. Olovku ili štrcaljku ne smijete tresti.
Otopina je bistra do blago opalescentna, bezbojna do blijedožuta i može sadržavati neke male prozirne ili bijele proteinske čestice. To nije neobično za otopine koje sadrže proteine.
Simponi se ne smije koristiti ako je otopina promijenila boju, zamućena je ili sadrži vidljive strane čestice.
Cjelovite upute za pripremu i primjenu Simponija u napunjenoj olovci ili napunjenoj štrcaljki nalaze se u uputama za uporabu.
Neiskorišteni lijek i otpad dobiven iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
07.0 Nositelj odobrenja za stavljanje u promet
Janssen Biologics B.V.
Einsteinweg 101
2333 CB Leiden
Nizozemska
08.0 BROJ DOZVOLE ZA PROMET
EU/1/09/546/001 1 napunjena olovka
EU/1/09/546/002 3 napunjene olovke
EU/1/09/546/003 1 napunjena štrcaljka
EU/1/09/546/004 3 napunjene štrcaljke
039541014
039541026
039541038
039541040
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Datum prve autorizacije: 1. listopada 2009
Datum posljednje obnove: 19. lipnja 2014
10.0 DATUM REVIZIJE TEKSTA
02. veljače 2017
11.0 ZA RADIO -LIJEKOVE POTPUNI PODACI O DOSIMETRIJI UNUTARNJEG ZRAČENJA
12.0 ZA RADIO -LIJEKOVE, DODATNE DETALJNE UPUTE O IZVRŠNOJ PRIPREMI I KONTROLI KVALITETE