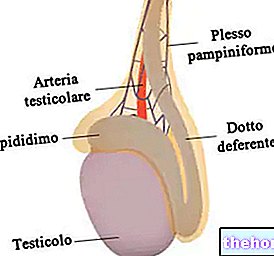
Aminokiseline i proteini posrednici su prijelaza iz svijeta minerala u živu materiju.
Kao što im naziv govori, aminokiseline su bifunkcionalne organske tvari: sastoje se od amino funkcije (-NH2) i karboksilne funkcije (-COOH); mogu biti α, β, γ itd., ovisno o položaju koji zauzima amino skupina u odnosu na karboksi skupinu:



Biološki važne aminokiseline su sve α-aminokiseline.
Proteinske strukture sastoje se od dvadeset aminokiselina.
Kao što se može vidjeti iz gore prikazanih generičkih struktura, sve aminokiseline imaju zajednički dio i drugačiji dio koji ih karakterizira (općenito predstavljene s R).
Od dvadeset aminokiselina, devetnaest je optički aktivnih (odbijaju ravninu polarizirane svjetlosti).
Većina aminokiselina ima samo jednu amino skupinu i jedan karboksil pa se zato i zovu neutralne aminokiseline; zovu se oni koji imaju dodatni karboksil kisele aminokiseline dok su oni s dodatnom amino grupom bazične aminokiseline.
Aminokiseline su kristalne krutine i imaju dobru topljivost u vodi.
Nedostatak nekih aminokiselina u prehrani uzrokuje ozbiljne promjene u razvoju; zapravo, ljudski organizam nije u stanju sintetizirati neke aminokiseline koje se točno nazivaju esencijalnima (moraju se unijeti hranom), dok može sam proizvesti samo neke aminokiseline (one koje nisu esencijalne).
Jedna od bolesti zbog nedostatka esencijalnih aminokiselina je ona poznata pod imenom kwashiorkor (riječ koja potječe iz afričkog narječja što u prijevodu znači "prva i druga"); ova bolest pogađa prvorođenče, ali nakon rođenja drugog djeteta jer prvom djetetu nedostaje majčino mlijeko koje sadrži ispravnu opskrbu bjelančevinama. Ova je bolest, dakle, široko rasprostranjena među pothranjenom populacijom i uključuje proljev, nedostatak apetita koji dovodi do progresivnog slabljenja organizma.
Kao što je već spomenuto, prirodne aminokiseline, s izuzetkom glicina (to je a-aminokiselina s vodikom umjesto R skupine i najmanja je od dvadeset), posjeduju optičku aktivnost zbog prisutnosti barem jedne asimetrične ugljika. U prirodnim aminokiselinama apsolutna konfiguracija asimetričnog ugljika na koji su vezane samo amino i karboksi skupine pripada L seriji;
D-aminokiseline nikada ne postaju dio strukture proteina.
Sjećamo se toga:
DNA ---- transkripcija → m-RNA ---- translacija → protein
Transkripcija se može kodirati kao L-aminokiseline; D-aminokiseline mogu biti sadržane u ne-proteinskim strukturama (npr. U stijenci bakterija: u bakterijama ne postoje "genetske informacije o tome da D-aminokiseline imaju zaštitnu ulogu, međutim, postoje" genetske informacije za enzime koji se bave stijenkom bakterijske sluznice).
Vratimo se aminokiselinama: različita struktura R skupine definira pojedinačne karakteristike svake aminokiseline i daje poseban doprinos karakteristikama proteina.
Stoga se smatralo da se aminokiseline dijele na temelju prirode R skupine:
Polarne, ali nenabijene aminokiseline:
Glicin (R = H-)
Serin (R = HO-CH2-)
Treoninbitan
Treonin ima dva centra simetrije: samo 2S, 3R treonin postoji u prirodi.
Treonin je esencijalna aminokiselina (ne treba je miješati s nezamjenjivom: sve aminokiseline su esencijalne) pa se mora uzimati s prehranom, tj. Jedući hranu koja ga sadrži jer, kao što je već spomenuto, genetsko naslijeđe nije prisutno u stanice ljudskih bića. sposobne proizvesti ovu aminokiselinu (ovo naslijeđe prisutno je u mnogim biljkama i boljima).
Hidroksilna skupina serina i treonina može se esterificirati s fosforilnom skupinom (dobivanjem fosfoserina i fosfotreonina), ovaj proces se naziva fosforilacija; fosforilacija se u prirodi koristi za prijevod signala između unutarnje i vanjske strane stanice.
Cistein (R = HS-CH2-)
Sulfhidril cisteina lakše se može protonirati od hidroksila serina: sumpor i kisik su šeste skupine, ali se sumpor lakše oksidira jer ima veće dimenzije.
Tirozin [R = HO- (C6H4) -CH2-]
N.B.
(C6H4) = di-supstituirani benzenski prsten
Kao i kod serina i treonina, hidroksil se može esterificirati (fosforilirati).Asparagin (R = NH2-CO-CH2-)
Glutamin (R = NH2-CO-CH2-CH2-)
Nepolarne aminokiseline
imaju hidrofobne bočne skupine; unutar ove klase razlikujemo:
Alifatika:
Alanin (R = CH3-)
Valin (R = (CH3) 2-CH-) bitan
Leucin (R = (CH3) 2-CH-CH2-) bitan
Izoleucin (R =
) bitno
Metionin (R = CH3-S-CH2-CH2-) bitan
Stanične membrane se sastoje od lipidnog dvosloja s proteinima usidrenim zahvaljujući njihovom hidrofobnom karakteru, stoga sadrže alanin, valin, izoleucin i leucin. S druge strane, metionin je aminokiselina koja je gotovo uvijek prisutna u malim količinama (oko 1%).
Prolin
Aromatično:
Fenilalanin (R = Ph-CH2-) Ph = fenil: esencijalni monosupstituirani benzen
Triptofan (R =
bitan
Ove dvije aminokiseline, budući da su aromatične, apsorbiraju blizu ultraljubičastog zračenja (oko 300 nm); stoga je moguće iskoristiti tehniku UV spektrofotometrije za određivanje koncentracije poznatog proteina koji sadrži te aminokiseline.
Napunjene aminokiseline
Zauzvrat se dijele na:
Kisele aminokiseline (koje imaju polarne ostatke s negativnim nabojem pri pH 7) takve su jer mogu dati pozitivan naboj H +:
Asparaginska kiselina
Glutaminska kiselina (R =
)
Ove aminokiseline potječu iz asparagina i glutamina; sva četiri postoje u prirodi i to znači da je c "specifična informacija za svakog od njih, to jest c" je bazna trojka u DNK koja kodira svaku od njih.
Bazne aminokiseline (koje imaju polarne ostatke s pozitivnim nabojem pri pH 7) takve su jer mogu prihvatiti pozitivan naboj H +:
Lizin (R =
) bitno
Arginin (R =
)
Histidin (R =
)
Postoje proteini u kojima u bočnim lancima postoje derivati aminokiselina: na primjer, može biti prisutan fosfoserin (ne postoje genetske informacije koje kodiraju fosfoserin, samo one za serin); fosfoserin je modifikacija posttranslacijski: nakon što je došlo do sinteze proteina
DNA ---- transkripcija → m-RNA ---- translacija → protein
takve post-translacijske modifikacije mogu se pojaviti na bočnim lancima proteina.
Vidi također: Proteini, pogled na kemiju