Struktura i funkcije
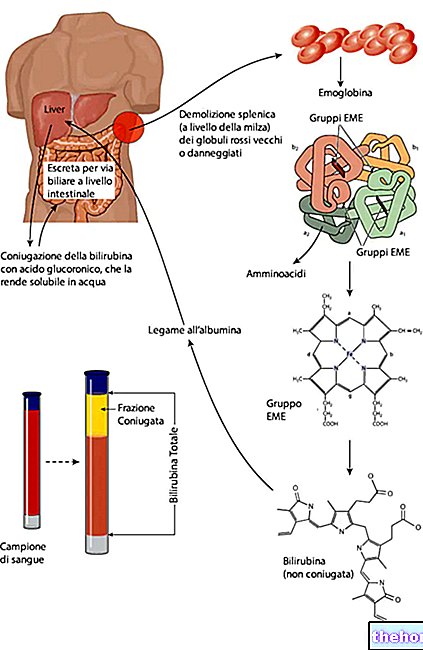
Hemoglobin je metaloprotein sadržan u crvenim krvnim zrncima, odgovoran za transport kisika u krvotok. Zapravo, kisik je samo umjereno topiv u vodi; stoga količine otopljene u krvi (manje od 2% ukupne količine) nisu dovoljne da zadovolje metaboličke zahtjeve tkiva. Stoga je evidentna potreba za posebnim prijevoznikom.
U krvotoku se kisik ne može izravno i reverzibilno vezati za proteine, što se događa umjesto metala poput bakra i željeza. Ne iznenađuje što u središtu svake proteinske podjedinice hemoglobina, omotane proteinskom ljuskom, nalazimo tzv. skupina EME, s metalnim srcem predstavljenim atomom željeza u oksidacijskom stanju Fe2 + (reducirano stanje), koje veže kisik na reverzibilan način.
Analiza krvi
- Normalne vrijednosti hemoglobina u krvi: 13-17 g / 100 ml
U žena su vrijednosti u prosjeku 5-10% niže nego u muškaraca.
Mogući uzroci visokog hemoglobina
- Policitemije
- Produženi boravak na uzvisini
- Kronične plućne bolesti
- Srčana bolest
- Doping krvi (upotreba eritropoetina i derivata ili tvari koje oponašaju njihovo djelovanje)
Mogući uzroci niskog hemoglobina
- Anemije
- Nedostatak željeza (nedostatak željeza)
- Obilno krvarenje
- Karcinomi
- Trudnoća
- Thalassemias
- Opekline
Sadržaj kisika u krvi stoga se daje zbrajanjem male količine otopljene u plazmi s udjelom vezanim za željezo hemoglobin.
Više od 98% kisika prisutnog u krvi vezano je za hemoglobin, koji pak cirkulira u krvotoku raspoređenom unutar crvenih krvnih zrnaca. Bez hemoglobina, dakle, eritrociti ne bi mogli obavljati svoju zadaću kao prijenosnici kisika u krvi.
S obzirom na središnju ulogu ovog metala, sinteza hemoglobina zahtijeva odgovarajući unos željeza u prehranu. Oko 70% željeza prisutnog u tijelu zapravo je sadržano u hem grupama hemoglobina.
Hemoglobin se sastoji od 4 podjedinice koje su strukturno vrlo slične mioglobinu *.
* Dok hemoglobin prenosi kisik iz pluća u tkiva, mioglobin prenosi kisik koji oslobađa hemoglobin u različite stanične organele koje ga koriste (npr. Mitohondrije).

Hemoglobin je veliki i složeni metaloprotein, karakteriziran s četiri kuglasta proteinska lanca omotana oko skupine hema koja sadrži Fe2 +.
Za svaku molekulu hemoglobina stoga nalazimo četiri skupine hema omotane u relativni globularni proteinski lanac. Budući da u svakoj molekuli hemoglobina postoje četiri atoma željeza, svaka molekula hemoglobina može vezati četiri atoma kisika za sebe, u skladu s reverzibilnom reakcijom:
Hb + 4O2 ← → Hb (O2) 4
Kao što je većini poznato, zadatak hemoglobina je uzeti kisik u plućima, osloboditi ga stanicama kojima je to potrebno, uzeti iz njih ugljični dioksid i otpustiti ga u pluća gdje ponovno počinje chilo.
Tijekom prolaska krvi u kapilarama plućnih alveola, hemoglobin veže kisik za sebe, koji se kasnije oslobađa u tkiva u perifernoj cirkulaciji. Do ove izmjene dolazi jer su veze kisika s željezom iz skupine EME labilne i osjetljive na mnoge čimbenike, od kojih je najvažniji napetost ili parcijalni tlak kisika.
Vezivanje kisika za hemoglobin i Bohrov učinak
U plućima se napetost kisika u plazmi povećava zbog difuzije plina iz alveola u krv (↑ PO2); ovo povećanje uzrokuje da se hemoglobin žustro veže za kisik; suprotno se događa u perifernim tkivima, gdje se koncentracija otopljenog kisika u krvi smanjuje (↓ PO2), a parcijalni tlak ugljičnog dioksida raste (↑ CO2); to potiče hemoglobin da oslobodi kisik i napuni se CO2. Pojednostavljujući koncept što je više moguće, što je više ugljičnog dioksida prisutno u krvi, manje kisika ostaje vezano za hemoglobin.
Iako je količina fizički otopljenog kisika u krvi vrlo niska, ona stoga igra temeljnu ulogu. Zapravo, ova količina uvelike utječe na čvrstoću veze između kisika i hemoglobina (kao i predstavlja "važnu referentnu vrijednost u regulaciji plućne ventilacije").
Sumirajući sve grafikonom, količina kisika vezanog za hemoglobin raste u odnosu na pO2 slijedeći sigmoidnu krivulju:

Činjenica da je regija plateu tako velika postavlja važnu sigurnosnu granicu pri maksimalnom zasićenju hemoglobina tijekom prolaska u pluća. Iako je pO2 na alveolarnoj razini normalno jednak 100 mm Hg, promatrajući brojku koju zapravo primjećujemo kako čak i parcijalni tlak kisika jednak 70 mmHg (tipična pojava nekih bolesti ili boravak na velikim nadmorskim visinama), postoci zasićenog hemoglobina ostaju blizu 100%.
U području najvećeg nagiba, kada parcijalna napetost kisika padne ispod 40 mmHg, sposobnost hemoglobina da veže kisik naglo opada.
U uvjetima mirovanja, PO2 u unutarstaničnim tekućinama iznosi približno 40 mmHg; na ovom mjestu, zbog zakona plinova, kisik otopljen u plazmi difundira prema siromašnijim tkivima O2, prelazeći kapilarnu membranu, pa posljedično, napetost O2 u plazmi dodatno pada i to pogoduje oslobađanju kisika iz hemoglobina. . S druge strane, tijekom intenzivnog fizičkog napora, napetost kisika u tkivima pada na 15 mmHg ili manje, zbog čega se krv uvelike osiromaši kisikom.
Kao što je već rečeno, u uvjetima mirovanja važna količina oksigeniranog hemoglobina napušta tkiva, koja ostaje dostupna u slučaju potrebe (na primjer radi rješavanja naglog povećanja metabolizma u nekim stanicama).
Puna linija prikazana na gornjoj slici naziva se krivulja disocijacije hemoglobina; tipično se određuje in vitro pri pH 7,4 i na temperaturi od 37 ° C.
Bohrov učinak ima posljedice i na unos O2 na razini pluća i na njegovo oslobađanje na razini tkiva.
Tamo gdje ima više otopljenog ugljičnog dioksida u obliku bikarbonata, hemoglobin lakše oslobađa kisik i postaje nabijen ugljikovim dioksidom (u obliku bikarbonata).

Isti učinak postiže se zakiseljavanjem krvi: što se više smanjuje pH krvi i manje kisika ostaje vezano za hemoglobin; nije iznenađujuće da se ugljični dioksid u krvi otapa uglavnom u obliku ugljične kiseline koja disocira.



U čast svog otkrivača, učinak pH ili ugljičnog dioksida na disocijaciju kisika poznat je kao Bohrov učinak.
Kao što se očekivalo, u kiselom okruženju hemoglobin lakše oslobađa kisik, dok je u baznom okruženju veza s kisikom jača.

Drugi čimbenici koji mogu promijeniti afinitet hemoglobina prema kisiku uključuju temperaturu. Konkretno, afinitet hemoglobina prema kisiku opada s povećanjem tjelesne temperature. To je osobito povoljno tijekom zimskih i proljetnih mjeseci, budući da je temperatura plućne krvi (u dodiru s zrak vanjskog okruženja) niži je od onog koji se doseže u tkivima, gdje se stoga olakšava oslobađanje kisika.

2.3 difosfoglicerat je međuprodukt u glikolizi koji utječe na afinitet hemoglobina prema kisiku. Ako se njegove koncentracije unutar crvenih krvnih zrnaca povećaju, smanjuje se afinitet hemoglobina prema kisiku, olakšavajući tako oslobađanje kisika u tkiva. Nije iznenađujuće da koncentracije eritrocita 2,3 difosfoglicerata povećava se, na primjer, kod anemije, kardio-plućne insuficijencije i tijekom boravka na velikoj nadmorskoj visini.
Općenito, učinak 2,3 bisfosfoglicerata relativno je spor, osobito u usporedbi s brzim odgovorom na promjene pH, temperature i parcijalnog tlaka ugljičnog dioksida.

Bohrov učinak vrlo je važan tijekom intenzivnog mišićnog rada; u takvim uvjetima, zapravo, u tkivima najizloženijim stresu dolazi do lokalnog povećanja temperature i tlaka ugljičnog dioksida, dakle i kiselosti krvi. Kao što je gore objašnjeno, sve to pogoduje oslobađanju kisika u tkiva, pomičući krivulju disocijacije hemoglobina udesno.