Aktivni sastojci: Trastuzumab
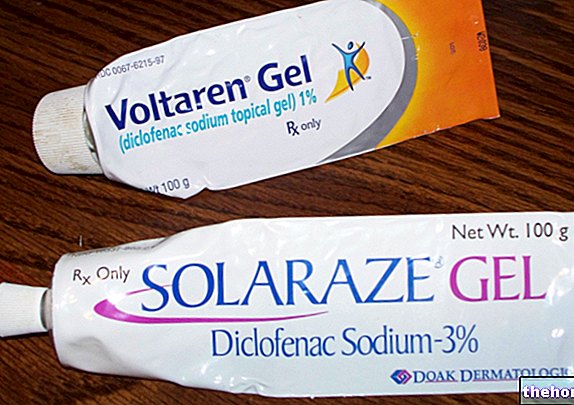
Herceptin 150 mg prašak za koncentrat za otopinu za infuziju
Herceptin umetci u pakiranju dostupni su za veličine pakiranja:- Herceptin 150 mg prašak za koncentrat za otopinu za infuziju
- Herceptin 600 mg otopina za injekciju u bočici
- Herceptin 600 mg otopina za injekciju putem uređaja za primjenu
Zašto se koristi Herceptin? Čemu služi?
Herceptin sadrži djelatnu tvar trastuzumab, koja je monoklonsko protutijelo. Monoklonska protutijela vežu se na specifične proteine ili antigene. Trastuzumab je dizajniran za selektivno vezanje na antigen nazvan receptor 2 humanog epidermalnog faktora rasta (HER2). HER2 je prisutan u velikim količinama na površini nekih stanica raka, potičući njihov rast. Kada se Herceptin veže za HER2, on zaustavlja rast ovih stanica i uzrokuje njihovu smrt.
Vaš liječnik može propisati Herceptin za liječenje raka dojke i želuca ako:
- Imate rani stadij raka dojke s visokom razinom proteina zvanog HER2.
- Imate metastatski rak dojke (rak dojke koji se proširio daleko od primarnog tumora) s visokom razinom HER2. Herceptin se može propisati u kombinaciji s kemoterapijskim lijekovima paklitakselom ili docetakselom kao prvi tretman za metastatski rak dojke ili se može propisati sam ako su se drugi tretmani pokazali neučinkovitima. Također se koristi u kombinaciji s lijekovima koji se zovu inhibitori aromataze za liječenje pacijenata s visokom razinom HER2 i metastatskim rakom dojke pozitivnim na hormonske receptore (rak osjetljiv na prisutnost ženskih spolnih hormona).
- Imate metastatski rak želuca s visokom razinom HER2, u kombinaciji s drugim lijekovima protiv raka, kapecitabinom ili 5-fluorouracilom i cisplatinom.
Kontraindikacije Kada se Herceptin ne smije koristiti
Nemojte koristiti Herceptin ako:
- ako ste alergični na trastuzumab, mišje (mišje) proteine ili na bilo koji drugi sastojak.
- imate teške probleme s disanjem u mirovanju zbog raka ili ako vam je potrebno liječenje kisikom.
Mjere opreza pri uporabi Što morate znati prije nego počnete uzimati Herceptin
Vaš će liječnik pomno nadzirati vašu terapiju.
Srčani pregled
Liječenje Herceptinom samostalno ili s taksanom može utjecati na vaše srce, osobito ako ste već uzimali "antraciklin (taksani i antraciklini su dvije druge vrste lijekova koji se koriste za liječenje raka). Stoga će se vaša funkcija srca prvo provjeriti., Tijekom (svaka tri mjeseca) i nakon (do dvije do pet godina) liječenja Herceptinom Ako osjetite znakove zatajenja srca (tj. srce ne pumpa krv pravilno), možda ćete morati prestati uzimati Herceptin.
Obratite se svom liječniku, ljekarniku ili medicinskoj sestri prije nego počnete uzimati Herceptin ako:
- ste imali zatajenje srca, koronarnu arterijsku bolest, bolest srčanih zalistaka (srčani šumovi), visoki krvni tlak, uzimali ste ili trenutno uzimate bilo koje lijekove za liječenje visokog krvnog tlaka.
- ste uzimali ili trenutno uzimate lijekove koji se zovu doksorubicin ili epirubicin (lijekovi za liječenje raka). Ovi lijekovi (ili bilo koji drugi antraciklin) mogu oštetiti srčani mišić i povećati rizik od srčanih problema tijekom uzimanja Herceptina.
- patite od nedostatka daha, osobito ako trenutno uzimate taksan. Herceptin može uzrokovati otežano disanje, osobito prvi put kada se daje. Ovo može biti ozbiljnije ako već patite od nedostatka zraka. Vrlo rijetko su pacijenti s teškim poteškoćama s disanjem prije liječenja umirali kada su primali Herceptin.
- su ikada primali druge tretmane protiv raka.
Ako primate Herceptin u kombinaciji s bilo kojim drugim lijekom koji se koristi za liječenje raka, poput paklitaksela, docetaksela, inhibitora aromataze, kapecitabina, 5-fluorouracila ili cisplatina, trebali biste pročitati i upute za uporabu ovih lijekova.
Djeca i adolescenti
Herceptin se ne preporučuje mlađima od 18 godina.
Interakcije Koji lijekovi ili hrana mogu promijeniti učinak Herceptina
Obavijestite svog liječnika, ljekarnika ili medicinsku sestru ako uzimate, nedavno ste uzimali ili biste mogli uzeti bilo koje druge lijekove.
Izlučivanje Herceptina iz tijela može potrajati do 7 mjeseci. Stoga biste trebali obavijestiti svog liječnika, ljekarnika ili medicinsku sestru da ste uzeli Herceptin ako počnete uzimati nove lijekove u roku od 7 mjeseci od prestanka terapije.
Upozorenja Važno je znati da:
Trudnoća
- Ako ste trudni, mislite da ste trudni ili planirate trudnoću, obavijestite svog liječnika, ljekarnika ili medicinsku sestru prije uzimanja ovog lijeka.
- Morate koristiti učinkovitu kontracepciju tijekom liječenja Herceptinom i najmanje 7 mjeseci nakon prestanka liječenja.
- Vaš će liječnik razgovarati s vama o rizicima i prednostima uzimanja Herceptina tijekom trudnoće.U rijetkim slučajevima, primijećeno je smanjenje (amnionske) tekućine koja okružuje dijete u razvoju u maternici u trudnica koje su liječene Herceptinom. Ovo stanje može biti štetno za bebu u maternici i bilo je povezano s nepotpunim sazrijevanjem pluća, što je rezultiralo fetalnom smrću.
Vrijeme za hranjenje
Nemojte dojiti tijekom uzimanja lijeka Herceptin i 7 mjeseci nakon posljednje doze lijeka Herceptin jer Herceptin može prenijeti bebi kroz majčino mlijeko. Prije uzimanja bilo kojeg lijeka pitajte svog liječnika ili ljekarnika za savjet.
Upravljanje vozilima i strojevima
Nije poznato hoće li Herceptin utjecati na vašu sposobnost upravljanja vozilima i rada sa strojevima. Međutim, ako osjetite simptome poput zimice ili vrućice, ne biste trebali voziti ili upravljati strojevima dok ti simptomi ne nestanu.
Doziranje i način uporabe Kako koristiti Herceptin: Doziranje
Prije početka liječenja liječnik će odrediti količinu HER2 u vašem tumoru. Herceptinom će se liječiti samo bolesnici s povišenim razinama HER2. Herceptin smije davati samo liječnik ili medicinska sestra. Vaš liječnik će propisati dozu i raspored liječenja koji vama odgovaraju. Doza Herceptina ovisi o vašoj tjelesnoj težini.
Postoje dvije različite vrste (formulacije) Herceptina:
- jedna se daje infuzijom u venu (intravenozna infuzija)
- drugi se daje injekcijom pod kožu (potkožna injekcija).
Važno je provjeriti naljepnicu proizvoda kako biste bili sigurni da se primjenjuje ispravna formulacija koju je propisao vaš liječnik. Herceptin intravenozna formulacija nije namijenjena za potkožnu primjenu i treba se primijeniti samo intravenoznom injekcijom.
Intravenska formulacija Herceptina primjenjuje se kao "intravenozna infuzija (" kapanje ") izravno u vaše vene. Prva doza liječenja daje se u razdoblju od 90 minuta, a zdravstveni radnik će vas tijekom primjene promatrati u slučaju nuspojava. Ako se prva doza dobro podnosi, sljedeće se doze mogu dati u razdoblju od 30 minuta (vidjeti dio 2 "Upozorenja i mjere opreza"). Broj infuzija koje ćete primiti ovisit će o vašem odgovoru na liječenje. Vaš će liječnik razgovaraj o tome s njom.
U pacijenata s ranim rakom dojke, metastatskim rakom dojke i metastatskim rakom želuca, Herceptin se daje svaka 3 tjedna. Herceptin se također može davati jednom tjedno za liječenje metastatskog raka dojke.
Kako biste izbjegli pogreške s lijekovima, važno je provjeriti naljepnice bočica kako biste bili sigurni da je lijek koji se priprema i primjenjuje Herceptin (trastuzumab), a ne trastuzumab emtansin.
Predoziranje Što učiniti ako ste uzeli previše Herceptina
Nema poznatih učinaka koji bi se mogli pripisati predoziranju Herceptinom.
Ako prestanete koristiti Herceptin
Nemojte prestati uzimati ovaj lijek bez prethodnog razgovora sa svojim liječnikom. Sve doze treba uzeti u pravo vrijeme svaki tjedan ili svaka tri tjedna (ovisno o rasporedu doziranja). To pomaže da lijek djeluje u najboljem slučaju.
Izlučivanje Herceptina iz tijela može potrajati i do 7 mjeseci. Stoga će vaš liječnik možda odlučiti nastaviti pratiti rad vašeg srca čak i nakon završetka liječenja.
Ako imate dodatnih pitanja o uporabi ovog lijeka, obratite se svom liječniku, ljekarniku ili medicinskoj sestri
Nuspojave Koje su nuspojave Herceptina
Kao i svi lijekovi, Herceptin može izazvati nuspojave, iako se one neće javiti kod svih. Neke od ovih nuspojava mogu biti ozbiljne i mogu zahtijevati hospitalizaciju.
Tijekom infuzije Herceptina mogu se pojaviti reakcije poput zimice, vrućice i drugih simptoma sličnih gripi. Ti su učinci vrlo česti (mogu se javiti u više od 1 na 10 osoba). Ostali simptomi povezani s infuzijom su: mučnina, povraćanje, bol, povećani mišići napetost i drhtavica, glavobolja, vrtoglavica, otežano disanje, piskanje, visoki ili niski krvni tlak, smetnje srčanog ritma (lupanje srca, ubrzani ili nepravilni otkucaji srca), oticanje lica ili usana, osip na koži i osjećaj umora. Neki od ovih simptoma mogu biti teški, a neki su pacijenti umrli (vidjeti dio 2 "Upozorenja i mjere opreza").
Ti se učinci uglavnom javljaju pri prvoj intravenskoj infuziji ("kapanje" u venu) i tijekom prvih nekoliko sati nakon početka infuzije. Općenito su privremeni. Zdravstveni radnik će vas nadzirati tijekom infuzije i najmanje šest sati nakon početka prve infuzije te dva sata nakon početka drugih infuzija. Ako osjetite reakciju, infuzija će se usporiti ili prekinuti, pa ćete možda dobiti tretman za suzbijanje neželjenih učinaka. Infuzija se može nastaviti nakon poboljšanja simptoma.
Povremeno, simptomi počinju više od šest sati nakon početka infuzije. Ako vam se to dogodi, odmah se obratite svom liječniku. Ponekad se simptomi mogu poboljšati, a kasnije se pogoršati.
Druge nuspojave mogu se pojaviti u bilo koje vrijeme tijekom liječenja Herceptinom, ne samo u vezi s infuzijom. Problemi sa srcem ponekad se mogu pojaviti tijekom liječenja, a povremeno i nakon završetka liječenja, a mogu biti ozbiljni. Oni uključuju slabljenje krvi. Srčani mišić koji može dovesti do zatajenja srca, upale (oticanje, crvenilo, vrućina i bol) sluznice srca i poremećaja srčanog ritma. To može dovesti do simptoma kao što su:
- nedostatak daha (čak i noću),
- kašalj,
- zadržavanje tekućine (oticanje) u nogama ili rukama,
- lupanje srca (ubrzan ili nepravilan rad srca).
Vaš liječnik će tijekom liječenja redovito nadzirati vaše srce, ali morate odmah obavijestiti svog liječnika ako primijetite bilo koji od gore navedenih simptoma.
Ako osjetite bilo koji od gore navedenih simptoma po završetku liječenja Herceptinom, trebate se obratiti svom liječniku i obavijestiti ga / je o svom prethodnom liječenju Herceptinom.
Vrlo česte nuspojave Herceptina (mogu se javiti u više od 1 na 10 osoba):
- infekcije
- proljev
- zatvor
- opekline u prsima (dispepsija)
- slabost
- kožni osip
- bol u prsima
- bolovi u trbuhu
- bol u zglobovima
- nizak broj crvenih krvnih stanica i bijelih krvnih stanica (koje pomažu u borbi protiv infekcija) ponekad povezan s groznicom
- mišićna bol
- konjunktivitis
- pretjerano suzenje
- krvarenje iz nosa
- curenje iz nosa
- gubitak kose
- tremor
- navale vrućine
- vrtoglavica
- problemi s noktima
- gubitak težine
- gubitak apetita
- nemogućnost spavanja (nesanica)
- Promijenjen okus
- Nizak broj trombocita
- Utrnulost ili trnci prstiju na rukama i nogama
- Crvenilo, oteklina ili mjehurići u ustima i / ili grlu
- Bol, oteklina, crvenilo ili utrnulost ruku i / ili stopala
Česte nuspojave Herceptina (mogu se javiti u do 1 na 10 osoba):
- alergijske reakcije
- suha usta i koža
- infekcije grla
- suhe oči
- infekcije mjehura i kože
- znojenje
- Šindre
- umor i malaksalost
- upala sinusa
- bio zabrinut
- upala gušterače ili jetre
- depresija
- bubrežni poremećaji
- promjene u razmišljanju
- povećan mišićni tonus ili napetost (hipertonija)
- astma
- bol u rukama i / ili nogama
- plućni poremećaji
- svrbežni osip
- bol u leđima
- pospanost
- bol u vratu
- modrice
- bolovi u kostima
- hemoroidi
- akne
- svrbež
- grčevi u nogama
Manje česte nuspojave Herceptina mogu se pojaviti u do 1 na 100 osoba:
- gluhoća
- osip s pšenicom
Rijetke nuspojave Herceptina: mogu se javiti u do 1 na 1000 osoba:
- slabost
- žutica
- upala / ožiljci pluća
Ostale nuspojave prijavljene pri uporabi lijeka Herceptin: učestalost se ne može procijeniti iz dostupnih podataka:
- abnormalnosti ili promjene u zgrušavanju krvi
- anafilaktičke reakcije
- visoke razine kalija
- oticanje mozga
- oticanje ili krvarenje iza očiju
- oticanje srčane membrane
- usporen rad srca
- šok
- abnormalni srčani ritam
- dišne poteškoće
- zatajenje disanja
- akutno nakupljanje tekućine u plućima
- akutno sužavanje dišnih putova
- abnormalno snižavanje razine kisika u krvi
- oticanje grla
- otežano disanje u ležećem položaju
- oštećenje / zatajenje jetre
- oticanje lica, usana i grla
- zatajenje bubrega abnormalno snižavanje razine tekućine oko djeteta u maternici
- neuspjeh razvoja pluća u maternici
- abnormalni razvoj bubrega u maternici
Neke od nuspojava koje se javljaju mogu biti posljedica raka dojke. Ako primate Herceptin u kombinaciji s kemoterapijom, neke od ovih nuspojava mogu biti posljedica kemoterapije.
Ako primijetite bilo koju od nuspojava, obavijestite svog liječnika, ljekarnika ili medicinsku sestru.
Prijavljivanje nuspojava
Ako dobijete bilo koju nuspojavu, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.Ovo uključuje sve moguće nuspojave koje nisu navedene u ovoj uputi. Nuspojave možete prijaviti i izravno putem nacionalnog sustava za prijavu navedenih u Dodatku V. Nuspojave koje možete pomoći pružiti više informacija o sigurnosti ovog lijeka.
Istek i zadržavanje
Čuvajte ovaj lijek izvan pogleda i dohvata djece.
Nemojte koristiti ovaj lijek nakon isteka roka valjanosti navedenog na kutiji i na bočici iza oznake EXP. Rok valjanosti odnosi se na zadnji dan tog mjeseca.
Čuvati u hladnjaku (2 ° C - 8 ° C).
Infuzijske otopine treba koristiti odmah nakon razrjeđivanja. Nemojte koristiti Herceptin ako primijetite bilo kakve čestice ili promjenu boje prije primjene.
Lijekovi se ne smiju odlagati u otpadne vode ili u kućni otpad. Pitajte svog ljekarnika kako baciti lijekove koje više ne koristite. To će pomoći u zaštiti okoliša.
Sastav i farmaceutski oblik
Što Herceptin sadrži
- Djelatna tvar je trastuzumab.Svaka bočica sadrži 150 mg trastuzumaba koji se mora otopiti u 7,2 ml vode za injekcije, a rezultirajuća otopina sadrži približno 21 mg / ml trastuzumaba.
- Pomoćni sastojci su L-histidin hidroklorid, L-histidin, α dihidrat, α-trehaloza, polisorbat 20.
Kako Herceptin izgleda i sadržaj pakiranja
Herceptin je prašak za koncentrat za otopinu za infuziju koji se isporučuje u staklenoj bočici zatvorenoj gumenim čepom koji sadrži 150 mg trastuzumaba. Prašak je bijela do svijetložuta liofilizirana kuglica. Svako pakiranje sadrži 1 bočicu praha.
Upute o izvoru: AIFA (Talijanska agencija za lijekove). Sadržaj objavljen u siječnju 2016. Prisutne informacije možda nisu ažurne.
Da biste imali pristup najnovijoj verziji, preporučljivo je pristupiti web stranici AIFA-e (Talijanska agencija za lijekove). Odricanje od odgovornosti i korisne informacije.
01.0 NAZIV LIJEKA
HERCEPTIN 150 MG U PRAHU ZA KONCENTRAT ZA RJEŠENJE ZA INFUZIJU
02.0 KVALITATIVNI I KOLIČINSKI SASTAV
Jedna bočica sadrži 150 mg trastuzumaba, humaniziranog monoklonalnog protutijela IgG1, proizvedenog staničnom kulturom sisavaca (stanice jajnika kineskog hrčka) u suspenziji, pročišćenom afinitetnom kromatografijom i ionskom izmjenom, sa specifičnim postupcima inaktivacije i uklanjanja virusa.
Rekonstituirana otopina Herceptina sadrži 21 mg / ml trastuzumaba.
Za potpuni popis pomoćnih tvari (vidjeti dio 6.1).
03.0 FARMACEUTSKI OBLIK
Prašak za koncentrat za otopinu za infuziju.
Bijeli do svijetložuti liofilizirani prah.
04.0 KLINIČKI PODACI
04.1 Terapeutske indikacije
Rak dojke
Metastatski rak dojke
Herceptin je indiciran za liječenje odraslih pacijenata s HER2 pozitivnim metastatskim rakom dojke (MBC):
• kao monoterapija za liječenje pacijenata koji su primili najmanje dva režima kemoterapije za metastatsku bolest. Prethodno primijenjena kemoterapija morala je sadržavati najmanje jedan antraciklin i jedan taksan, osim ako je pacijent neprikladan za takve tretmane. Pacijenti pozitivni na hormonske receptore također nisu uspjeli reagirati na hormonsku terapiju, osim ako je pacijent neprikladan za takve tretmane.
• u kombinaciji s paklitakselom za liječenje pacijenata koji nisu primili kemoterapiju zbog svoje metastatske bolesti i kod kojih liječenje antraciklinima nije indicirano.
• u kombinaciji s docetakselom za liječenje pacijenata koji nisu primili kemoterapiju zbog svoje metastatske bolesti.
• u kombinaciji s inhibitorom aromataze u liječenju bolesnika u postmenopauzi s MBC pozitivnim na hormonske receptore koji prethodno nisu liječeni trastuzumabom.
Rani stadij raka dojke
Herceptin je indiciran za liječenje odraslih pacijenata s HER2 pozitivnim ranim rakom dojke (EBC):
• nakon operacije, kemoterapije (neoadjuvantne ili adjuvantne) i radioterapije (ako je primjenjivo) (vidjeti dio 5.1)
• nakon adjuvantne kemoterapije doksorubicinom i ciklofosfamidom, u kombinaciji s paklitakselom ili docetakselom.
• u kombinaciji s adjuvantnom kemoterapijom s docetakselom i karboplatinom.
• u kombinaciji s neoadjuvantnom kemoterapijom, nakon koje slijedi adjuvantna terapija Herceptinom, u lokalno uznapredovaloj bolesti (uključujući upalni oblik) ili u tumorima promjera> 2 cm (vidjeti dijelove 4.4 i 5.1).
Herceptin se smije koristiti samo u bolesnica s metastatskim ili ranim stadijem raka dojke čiji tumori pokazuju prekomjernu ekspresiju HER2 ili amplifikaciju gena HER2 kako je utvrđeno točnim i potvrđenim testom (vidjeti dijelove 4.4 i 5.1).
Metastatski rak želuca
Herceptin u kombinaciji s kapecitabinom ili 5-fluorouracilom i cisplatinom indiciran je za liječenje odraslih pacijenata s metastatskim adenokarcinomom želuca ili gastroezofagealnog spoja HER2 pozitivnim koji prethodno nisu primali antikancerogeno liječenje zbog metastatske bolesti.
Herceptin se smije davati samo pacijentima s metastatskim rakom želuca (MGC) čiji tumori imaju prekomjernu ekspresiju HER2, definiranu kao rezultat IHC2 + i potvrđenu rezultatom SISH ili FISH, ili definiranu kao rezultat IHC3 +. Moraju se koristiti točne i potvrđene metode određivanja (vidjeti dijelove 4.4 i 5.1).
04.2 Doziranje i način primjene
Mjerenje ekspresije HER2 obvezno je prije početka terapije (vidjeti dijelove 4.4 i 5.1). Liječenje Herceptinom treba započeti samo liječnik s iskustvom u primjeni citotoksične kemoterapije (vidjeti dio 4.4), a smije ga provoditi samo zdravstveni radnik .
Važno je provjeriti označavanje lijeka kako bi se osiguralo da se pacijentu daje ispravna formulacija (intravenozna ili potkožna fiksna doza) kako je propisano. Herceptin intravenozna formulacija nije namijenjena za potkožnu primjenu i treba se primijeniti samo intravenoznom infuzijom.
Prijelaz s liječenja Herceptin intravenoznom formulacijom na liječenje s Herceptin potkožnim oblikom i obratno, davano svaka tri tjedna (q3w), ispitivano je u studiji MO22982 (vidjeti dio 4.8).
Kako biste izbjegli pogreške s lijekovima, važno je provjeriti naljepnice bočica kako biste bili sigurni da je lijek koji pripremate i primjenjujete Herceptin (trastuzumab), a ne Kadcyla (trastuzumab emtansin).
Doziranje
Metastatski rak dojke
Administracija svaka tri tjedna
Preporučena početna učitavajuća doza je 8 mg / kg tjelesne težine.Preporučena doza održavanja u intervalima od tri tjedna je 6 mg / kg tjelesne težine, počevši tri tjedna nakon punjenja.
Tjedna administracija
Preporučena početna učitavajuća doza Herceptina je 4 mg / kg tjelesne težine. Preporučena tjedna doza održavanja Herceptina je 2 mg / kg tjelesne težine, počevši tjedan dana nakon punjenja.
Primjena u kombinaciji s paklitakselom ili docetakselom
U ključnim studijama (H0648g, M77001) paklitaksel ili docetaksel primijenjeni su dan nakon prve doze Herceptina (za dozu pogledajte Sažetak opisa svojstava proizvoda (SmPC) paklitaksela ili docetaksela) i odmah nakon sljedećih doza Herceptina ako je prethodna Doza Herceptina se dobro podnosila.
Primjena u kombinaciji s inhibitorom aromataze
U ključnoj studiji (BO16216) Herceptin i anastrozol primijenjeni su od 1. dana. Nije bilo ograničenja u pogledu vremena primjene Herceptina i anastrozola (za dozu vidjeti SmPC za anastrozol ili druge inhibitore aromataze).
Rani stadij raka dojke
Administracija svaka tri tjedna i tjedno
Kada se primjenjuje tri puta tjedno, preporučena početna učitavajuća doza Herceptina je 8 mg / kg tjelesne težine. Preporučena doza održavanja Herceptina u intervalima od tri tjedna je 6 mg / kg tjelesne težine, počevši tri tjedna nakon punjenja.
U tjednoj primjeni (početna učitavajuća doza od 4 mg / kg, zatim 2 mg / kg jednom tjedno) istodobno s paklitakselom nakon kemoterapije s doksorubicinom i ciklofosfamidom.
Vidjeti dio 5.1 za dozu kombinirane kemoterapije.
Metastatski rak želuca
Administracija svaka tri tjedna
Preporučena početna učitavajuća doza je 8 mg / kg tjelesne težine. Preporučena doza održavanja u intervalima od tri tjedna je 6 mg / kg tjelesne težine, počevši tri tjedna nakon punjenja.
Metastatski i rani stadij raka dojke i metastatski rak želuca
Trajanje liječenja
Pacijentice s metastatskim rakom dojke ili metastatskim rakom želuca trebaju se liječiti Herceptinom do progresije bolesti. Pacijentice s ranim karcinomom dojke trebaju se liječiti Herceptinom 1 godinu ili dok se ne dogodi recidiv, ovisno o tome što se dogodi prije. Ne preporučuje se produljenje liječenja u EBC -u više od jedne godine (vidjeti dio 5.1).
Smanjenje doze
U kliničkim ispitivanjima nije bilo smanjenja doze Herceptina. Pacijenti mogu nastaviti terapiju lijekom Herceptin tijekom razdoblja reverzibilne mijelosupresije izazvane kemoterapijom, ali ih je tijekom tog razdoblja potrebno pomno pratiti radi komplikacija povezanih s neutropenijom. Za smanjenje ili odgodu doziranja pogledajte SmPC paklitaksela, docetaksela ili inhibitora aromataze.
Ako se postotak izbacivajuće frakcije lijeve klijetke (LVEF) smanji ≥ 10 bodova od početne vrijednosti i padne ispod 50%, doziranje treba obustaviti i procjenu LVEF -a ponoviti u roku od približno 3 tjedna. Ako se LVEF ne poboljša ili dodatno smanji ili ako se razvije simptomatsko kongestivno zatajenje srca (CHF), potrebno je ozbiljno razmotriti prekid liječenja Herceptinom, osim ako koristi za svakog pojedinog bolesnika prevladavaju rizike. Sve te pacijente morat će pregledati kardiolog i vremenom ih pratiti.
Propuštene doze
Ako je pacijent propustio dozu Herceptina tjedan dana ili manje, uobičajenu dozu održavanja Herceptina (tjedno: 2 mg / kg, svaka 3 tjedna: 6 mg / kg) treba dati što je prije moguće. Ne čekajte sljedeći zakazani ciklus. Naknadne doze održavanja Herceptina treba primijeniti 7 ili 21 dan kasnije, ovisno o odgovarajućem režimu doziranja: tjedno ili svaka tri tjedna.
Ako je pacijent propustio dozu Herceptina više od jednog tjedna, novu punu dozu Herceptina treba dati za približno 90 minuta (tjedna primjena: 4 mg / kg, primjena svaka 3 tjedna: 8 mg / kg) čim moguće. Naknadne doze održavanja Herceptina (tjedna primjena: 2 mg / kg, primjena svaka 3 tjedna: 6 mg / kg) trebale bi se primijeniti 7 ili 21 dan kasnije, ovisno o odgovarajućem režimu doziranja: tjedno ili svaka tri tjedna.
Posebne populacije
Farmakokinetičke studije nisu provedene u starijoj populaciji i u ispitanika s bubrežnom ili jetrenom disfunkcijom. U populacijskoj farmakokinetičkoj analizi dob i bubrežno oštećenje nisu promijenili dostupnost trastuzumaba.
Pedijatrijska populacija
Nema naznaka za specifičnu primjenu Herceptina u pedijatrijskoj populaciji.
Način primjene
Punu dozu Herceptina treba primijeniti kao 90 -minutnu intravensku infuziju. Nemojte primjenjivati kao intravensku injekciju ili intravenozni bolus. Intravensku infuziju Herceptina trebaju primjenjivati zdravstveni radnici obučeni za liječenje anafilaksije i u prisutnosti hitne opreme. Bolesnike je potrebno promatrati najmanje šest sati nakon početka prve infuzije i dva sata nakon početka sljedećih infuzija zbog simptoma, poput vrućice i zimice ili drugih simptoma povezanih s infuzijom (vidjeti dijelove 4.4 i 4.8. Ovi simptomi mogu kontrolirati zaustavljanjem infuzije ili usporavanjem brzine. Infuzija se može nastaviti nakon ublažavanja simptoma.
Ako se početna opterećujuća doza dobro podnosi, sljedeće se doze mogu primijeniti kao 30 -minutna infuzija.
Za upute o rekonstituciji Herceptin intravenozne formulacije prije primjene, vidjeti dio 6.6.
04.3 Kontraindikacije
• Poznata preosjetljivost na trastuzumab, mišje bjelančevine ili bilo koju od pomoćnih tvari navedenih u dijelu 6.1.
• Pacijenti s teškom dispnejom u mirovanju, zbog komplikacija uznapredovalih malignih bolesti, ili pacijenti koji zahtijevaju dodatnu terapiju kisikom.
04.4 Posebna upozorenja i mjere opreza pri uporabi
Kako bi se poboljšala sljedivost bioloških lijekova, komercijalni naziv i broj serije primijenjenog proizvoda moraju biti jasno zabilježeni (ili deklarirani) u zdravstvenom kartonu pacijenta.
Testiranje na HER2 mora se provesti u specijaliziranom laboratoriju koji može jamčiti odgovarajuću validaciju analitičkih postupaka (vidjeti dio 5.1).
Trenutno nema podataka iz kliničkih ispitivanja o ponovnom liječenju pacijenata koji su prethodno bili izloženi Herceptinu radi adjuvantnog liječenja.
Srčana disfunkcija
Opće razmatranje
Pacijenti liječeni Herceptinom imaju povećan rizik od razvoja srčane insuficijencije (klasa II-IV prema New York Heart Association [NYHA]) ili asimptomatska srčana disfunkcija. Ti su događaji primijećeni u bolesnika liječenih samo Herceptinom ili u kombiniranoj terapiji s paklitakselom ili docetakselom, osobito nakon kemoterapije antraciklinima (doksorubicin ili epirubicin). Oni su umjerenog do teškog intenziteta i povezani su sa smrću (vidjeti odlomak 4.8). Osim toga, potreban je poseban oprez pri liječenju pacijenata s povećanim srčanim rizikom, npr. hipertenzija, potvrđena bolest koronarnih arterija, CHF, frakcija izbacivanja lijeve klijetke (LVEF) u starosti.
Svi kandidati za liječenje Herceptinom, a osobito pacijenti koji su prethodno bili izloženi liječenju antraciklinom i ciklofosfamidom (AC), trebali bi proći osnovnu procjenu srčanog statusa, uključujući anamnezu i fizički pregled, elektrokardiogram (EKG), ehokardiogram i / ili snimanje s višestrukim ulazom (MUGA) ili MRI. Praćenje može pomoći u identificiranju pacijenata kod kojih se razvije srčana disfunkcija. Procjenu srčane funkcije, provedenu na način početne, treba ponoviti svaka 3 mjeseca tijekom liječenja i svakih 6 mjeseci nakon prestanka liječenja do 24 mjeseca nakon posljednje primjene Herceptina.
Na temelju populacijske farmakokinetičke analize svih dostupnih podataka (vidjeti dio 5.2), trastuzumab može ostati u cirkulaciji do 7 mjeseci nakon prestanka uzimanja Herceptina. Bolesnici koji primaju antracikline nakon završetka liječenja Herceptinom mogu imati povećan rizik od srčane disfunkcije. Ako je moguće, liječnici trebaju izbjegavati terapiju antraciklinima do 7 mjeseci nakon prestanka primjene Herceptina.Ukoliko se koriste antraciklini, potrebno je pomno pratiti rad srca pacijenta.
Formalnu kardiološku procjenu treba razmotriti u pacijenata koji su imali kardiološke probleme nakon početnog pregleda. Tijekom liječenja u svih pacijenata (npr. Svakih 12 tjedana) potrebno je pratiti rad srca. Praćenje može pomoći u identifikaciji pacijenata kod kojih se razvije srčana disfunkcija. Pacijenti koji razviju asimptomatsku srčanu disfunkciju mogu imati koristi od češćeg praćenja (npr. Svakih 6-8 tjedana). U slučaju pacijenata koji prijavljuju kontinuirano smanjenje funkcije lijeve klijetke, ali ostaju asimptomatski, liječnik bi trebao razmotriti prekid terapije ako nije primijećena klinička korist od terapije lijekom Herceptin.
Sigurnost nastavka ili ponovnog uvođenja lijeka Herceptin u pacijenata s poremećajima rada srca nije ispitana u prospektivnim studijama. Ako se LVEF smanji ≥ 10 bodova od početne vrijednosti i padne ispod 50%, doziranje treba obustaviti i LVEF ponovno procijeniti u roku od otprilike 3 tjedna. Ako LVEF to učini ako se ne poboljša ili dalje opada, ili se razvije simptomatski CHF, treba ozbiljno razmotriti prekid liječenja Herceptinom, osim ako se smatra da koristi za pojedinog pacijenta nadmašuju rizike Ove bolesnike treba procijeniti kardiolog i pratiti ih s vremenom.
Ako se tijekom liječenja Herceptinom pojavi simptomatsko zatajenje srca, potrebno ga je liječiti standardnom terapijom lijekovima za CHF. Većina pacijenata koji su razvili koronarnu srčanu insuficijenciju ili asimptomatsku srčanu disfunkciju u ključnim studijama poboljšali su se standardnim liječenjem inhibitorom angiotenzin konvertirajućeg enzima (ACE) ili blokatorom angiotenzinskih receptora (ARB) i beta blokatorom Većina pacijenata sa srčanim simptomima i dokazima kliničke koristi povezane s Herceptinom liječenje je nastavilo terapiju bez daljnjih srčanih kliničkih događaja.
Metastatski rak dojke
Herceptin se ne smije davati istodobno s antraciklinima u kontekstu MBC -a.
Pacijenti s MBC koji su prethodno primali antracikline također su u opasnosti od srčane disfunkcije tijekom liječenja Herceptinom, iako je taj rizik manji nego kod istodobne primjene Herceptina i antraciklina.
Rani stadij raka dojke
Za pacijente s EBC -om, kardiološku procjenu, provedenu na način početne, treba ponoviti svaka 3 mjeseca tijekom liječenja i svakih 6 mjeseci nakon prestanka liječenja, do 24 mjeseca nakon posljednje primjene Herceptina. U bolesnika koji primaju kemoterapiju na bazi antraciklina preporučuje se dodatno praćenje, koje bi se trebalo provoditi godišnje do 5 godina nakon posljednje primjene Herceptina, ili duže ako se primijeti kontinuirano smanjenje LVEF-a.
Pacijenti s anamnezom infarkta miokarda (MI), anginom pektoris koja zahtijeva liječenje, prethodnom ili trenutnom CHF (NYHA klasa II-IV), kardiomiopatijom LVEF-a, srčanom aritmijom koja zahtijeva liječenje, klinički značajnom valvularnom bolesti srca, slabom kontrolom hipertenzije (kontrolirana hipertenzija odgovarajućim standardnim medicinskim tretmanom) i hemodinamski značajni perikardni izljev isključeni su iz ključnih studija adjuvantnog i neoadjuvantnog EBC liječenja s Herceptinom. Stoga se liječenje ne može preporučiti u ovih pacijenata.
Pomoćno liječenje
Herceptin se ne smije davati istodobno s antraciklinima u kontekstu adjuvantnog liječenja.
Povećana incidencija simptomatskih i asimptomatskih srčanih događaja primijećena je u bolesnica s ranim karcinomom dojke kada se Herceptin primjenjivao nakon kemoterapije na bazi antraciklina u usporedbi s primjenom docetaksela i neantraciklin karboplatina, a bio je izraženiji kada se Herceptin primjenjivao istodobno s taksanima nego kada se uzastopno primjenjuju na taksane. Bez obzira na primijenjeni režim, većina simptomatskih srčanih događaja dogodila se unutar prvih 18 mjeseci. U jednoj od 3 ključne studije u kojima je pratiti medijana 5,5 godina (BCIRG006) primijećeno je trajno povećanje kumulativne stope simptomatskih srčanih događaja ili LVEF -a u bolesnika koji su primali Herceptin istodobno s taksanom nakon terapije antraciklinima do 2,37% u usporedbi s približno 1. 1% u dvije usporedbe oružja (antraciklin plus ciklofosfamid nakon čega slijede taksan i taksan, karboplatin i Herceptin).
Četiri velike studije provedene u adjuvantnom okruženju identificirale su čimbenike srčanog rizika uključujući: stariju dob (> 50 godina), nizak LVEF (antihipertenzivni lijekovi. U bolesnika liječenih Herceptinom nakon završetka adjuvantne kemoterapije, rizik od srčane disfunkcije povezan je sa veća kumulativna doza antraciklina dana prije početka terapije Herceptinom i indeks tjelesne mase (BMI)> 25 kg / m2.
Neoadjuvantno-adjuvantno liječenje
U bolesnika s EBC-om koji su kandidati za neoadjuvantno-adjuvantno liječenje, Herceptin se treba primjenjivati istodobno s antraciklinima samo u bolesnika koji se nisu liječili kemoterapijom i samo s niskim dozama antraciklina, tj. Najvećim kumulativnim dozama doksorubicina 180 mg / m2 ili epirubicina 360 mg / m2.
Ako su se bolesnici istodobno liječili punim nizom niskih doza antraciklina i Herceptina u neoadjuvantnom okruženju, nakon operacije se ne smije davati daljnja citotoksična kemoterapija. U drugim situacijama odluka o potrebi dodatne citotoksične kemoterapije mora se donijeti prema individualnim čimbenicima.
Dosadašnje iskustvo istodobne primjene trastuzumaba s niskim dozama antraciklinskih režima ograničeno je na dvije studije (MO16432 i BO22227).
U ključnoj studiji MO16432, Herceptin je primijenjen istodobno s neoadjuvantnom kemoterapijom, koja je sadržavala tri ciklusa doksorubicina (kumulativna doza od 180 mg / m2).
Učestalost simptomatske srčane disfunkcije bila je 1,7% u kraku koji je sadržavao Herceptin.
Ključna studija BO22227 osmišljena je kako bi pokazala neinferiornost liječenja potkožnom formulacijom Herceptina u usporedbi s intravenoznom formulacijom Herceptina koja se temelji na ko-primarnim krajnjim točkama PK i učinkovitosti (Ctrom trastuzumaba ciklusa 8 prije doze i stopom pCR-a pri konačnoj operaciji, respektivno) (vidjeti dio 5.1 SmPC -a potkožne formulacije Herceptin). U ključnoj studiji BO22227, Herceptin je primijenjen istodobno s neoadjuvantnom kemoterapijom koja je sadržavala četiri ciklusa epirubicina (kumulativna doza od 300 mg / m2); pri medijanu praćenja od 40 mjeseci, incidencija kongestivnog zatajenja srca bila je 0,0% u intravenoznoj ruci lijekom Herceptin.
Kliničko iskustvo u bolesnika starijih od 65 godina je ograničeno.
Reakcije povezane s infuzijom i preosjetljivost
Prijavljene su ozbiljne nuspojave povezane s infuzijom Herceptina, uključujući dispneju, hipotenziju, piskanje, hipertenziju, bronhospazam, supraventrikularnu tahiaritmiju, smanjenu zasićenost kisikom, anafilaksu, respiratorni distres, urtikariju i angioedem (vidjeti dio 4.8). Premedikacija se može koristiti za smanjenje rizika od takvih događaja. Većina ovih događaja događa se tijekom ili unutar 2,5 sata od početka prve infuzije. Ako dođe do infuzijske reakcije, infuziju Herceptina treba prekinuti ili usporiti brzinu infuzije, a bolesnika pratiti do smanjenja svih uočenih simptoma (vidjeti dio 4.2. ). Ovi se simptomi mogu liječiti analgeticima / antipireticima, poput meperidina ili paracetamola, ili s antihistaminicima poput difenhidramina. Većina pacijenata doživjela je povlačenje simptoma, te su nakon toga primili dodatne infuzije Herceptina. Ozbiljne reakcije uspješno su liječene sa potporna terapija, poput kisika, beta -agonista i kortikosteroida. U rijetkim slučajevima, te su reakcije bile povezane s kliničkim tijekom koji je kulminirao smrtonosnim ishodom. Pacijenti koji dožive dispneju u mirovanju, zbog komplikacija uznapredovalih tumora i komorbiditeta, mogu biti pod većim rizikom više da doživi smrtonosnu reakciju na infuziju. Stoga se ti bolesnici ne smiju liječiti Herceptinom (vidjeti dio 4.3).
Također su zabilježena početna poboljšanja praćena kliničkim pogoršanjem i odgođene reakcije s brzim kliničkim pogoršanjem. Smrt se dogodila unutar nekoliko sati i do tjedan dana nakon infuzije. U vrlo rijetkim slučajevima, pacijenti su doživjeli početak infuzijskih reakcija i plućne simptome više od šest sati nakon početka infuzije Herceptina. Pacijente ih treba upozoriti na mogućnost takve odgođen početak i treba ih uputiti da se jave svom liječniku ako se to dogodi.
Plućni događaji
Tijekom primjene lijeka Herceptin u razdoblju nakon stavljanja lijeka u promet zabilježeni su teški plućni događaji (vidjeti dio 4.8). Ti su događaji povremeno bili fatalni. Prijavljeni su i slučajevi intersticijske plućne bolesti uključujući plućne infiltrate, sindrom akutnog respiratornog distresa, upalu pluća., Pluća upala, pleuralni izljev, respiratorni distres, akutni plućni edem i respiratorno zatajenje. Čimbenici rizika povezani s intersticijskom bolešću pluća uključuju prethodnu ili istodobnu terapiju s drugim anti-neoplastičnim tretmanima kao što su taksani, gemcitabin, vinorelbin i radioterapija, za koje je takva povezanost već poznata Ovi se događaji mogu pojaviti u kontekstu infuzijske reakcije ili imaju odgođeni početak. Pacijenti koji dožive dispneju u mirovanju, zbog komplikacija uznapredovalih tumora i komorbiditeta, mogu imati veći rizik od doživljavanja događaja. Ovi pacijenti nti se stoga ne smije liječiti Herceptinom (vidjeti dio 4.3). U prisutnosti upale pluća treba biti oprezan, osobito u bolesnika koji se istodobno liječe taksanima.
04.5 Interakcije s drugim lijekovima i drugi oblici interakcija
Nisu provedena formalna ispitivanja interakcija lijekova. U kliničkim ispitivanjima nisu primijećene klinički značajne interakcije između Herceptina i istodobno primijenjenih lijekova.
Učinak trastuzumaba na farmakokinetiku drugih antineoplastika
Farmakokinetički podaci iz studija BO15935 i M77004 u žena s HER2 pozitivnim metastatskim rakom dojke ukazuju na to da se izloženost paklitakselu i doksorubicinu (i njihovim glavnim metabolitima 6-α hidroksil-paklitakselu, POH i doksorubicinol, DOL) nije promijenila zbog prisutnosti trastuzumaba (IV opterećujuća doza 8 mg / kg ili 4 m / kg nakon čega slijedi 6 mg / kg q3w ili 2 mg / kg q1w IV, respektivno).
Međutim, trastuzumab može povećati ukupnu izloženost metabolita doksorubicina (7-deoksi-13 dihidro-doksorubicinon, D7D). Bioaktivnost D7D i klinički učinak povećanja ovog metabolita nisu bili jasni.
Podaci iz studije JP16003, u jednoj ruci s Herceptinom (IV učitavajuća doza 4 mg / kg i IV 2 mg / kg tjedno) i docetakselom (60 mg / m2 IV), provedeni u Japanki s HER2 pozitivnim metastatskim rakom dojke, sugeriraju da istodobna primjena Herceptina nije imala utjecaja na farmakokinetiku docetaksela u jednoj dozi. JP19959 je podstudija studije BO18255 (ToGA) provedena na japanskim pacijentima i ženama s uznapredovalim rakom želuca radi proučavanja farmakokinetičkog profila kapecitabina i cisplatina primijenjenih sa ili bez Herceptina. Rezultati ovog podstudija ukazuju na to da se izloženost bioaktivnim metabolitima (npr. 5-FU) kapecitabina nije promijenila istodobnom primjenom monoterapije cisplatinom ili cisplatina s Herceptinom. Međutim, sam kapecitabin pokazao je veće koncentracije i dulji poluživot u kombinaciji s Herceptinom. Podaci također ukazuju na to da se farmakokinetika cisplatina nije promijenila istodobnom primjenom kapecitabina ili kapecitabina u kombinaciji s Herceptinom.
Farmakokinetički podaci iz studije H4613g / GO01305 u bolesnica s metastatskim ili lokalno uznapredovalim neoperabilnim HER2-pozitivnim karcinomom dojke ukazuju na to da trastuzumab nije utjecao na farmakokinetiku karboplatina.
Učinci antineoplastike na farmakokinetiku trastuzumaba
Usporedbom simuliranih serumskih koncentracija trastuzumaba nakon monoterapije Herceptinom (4 mg / kg puna doza / 2 mg / kg q1w IV) i serumskih koncentracija primijećenih kod Japanki s HER2 pozitivnim metastatskim rakom dojke (studija JP16003) pokazalo se da istodobna primjena docetaksela nije imala učinka o farmakokinetici trastuzumaba.
Usporedba farmakokinetičkih podataka iz dvije studije II. Faze (BO15935 i M77004) i jedne studije III. Faze (H0648g), u kojoj su bolesnici istodobno primali Herceptin i paklitaksel, te dvije studije II. Faze u kojima se Herceptin primjenjivao kao monoterapija (W016229 i MO16982), u žena s HER2 pozitivnim metastatskim rakom dojke, ukazuje da pojedinačne i srednje najniže koncentracije trastuzumaba u serumu variraju unutar i između studija, ali nije jasan učinak istodobne primjene paklitaksela na farmakokinetiku trastuzumaba.Usporedba farmakokinetičkih podataka trastuzumaba iz studije M77004 u kojoj su žene s HER2-pozitivnim metastatskim rakom dojke primale istodobno liječenje s Herceptinom, paklitakselom i doksorubicinom, te farmakokinetičkim podacima trastuzumaba u studijama u kojima se Herceptin primjenjivao sam (H0649g) ili u kombinaciji s antraciklinom plus ciklofosfamid ili paklitaksel (studija H0648g), sugeriralo je da doksorubicin i paklitaksel nemaju utjecaja na farmakokinetiku trastuzumaba.
Farmakokinetički podaci iz studije H4613g / GO01305 ukazuju na to da karboplatin nema utjecaja na farmakokinetiku trastuzumaba.
Čini se da istodobna primjena anastrozola nije utjecala na farmakokinetiku trastuzumaba.
04.6 Trudnoća i dojenje
Žene u reproduktivnoj dobi
Žene u reproduktivnoj dobi treba upozoriti na potrebu korištenja učinkovite kontracepcije tijekom liječenja Herceptinom i 7 mjeseci nakon završetka liječenja (vidjeti dio 5.2).
Trudnoća
Reprodukcijske studije provedene su na majmunima cynomolgus u dozama do 25 puta većim od tjedne ljudske doze održavanja od 2 mg / kg Herceptina za intravenoznu primjenu i nije otkrilo nikakve dokaze o smanjenoj plodnosti ili oštećenju ploda. Prijenos trastuzumaba posteljicom opažen je tijekom razvojnog razdoblja. rani fetus (20-50. dana trudnoće) ) i kasno (120-150 dana trudnoće). Nije poznato može li Herceptin utjecati na reproduktivnu sposobnost. Budući da studije o reprodukciji na životinjama ne predviđaju uvijek učinke na "muškarce, Herceptin treba izbjegavati u trudnoći, osim ako su moguće koristi za majku" nadmašuju potencijalne rizike za fetus.
Nakon stavljanja lijeka u promet prijavljeni su poremećaji bubrežnog razvoja i / ili funkcije povezani s oligohidramnionom, od kojih su neki povezani s fatalnom fetalnom plućnom hipoplazijom, u trudnica liječenih Herceptinom. U slučaju trudnoće, ženu treba obavijestiti o mogućnosti štete po fetus. Pomno praćenje multidisciplinarnog tima poželjno je ako se trudnica liječi Herceptinom ili ako dođe do trudnoće tijekom liječenja Herceptinom ili unutar 7 mjeseci nakon posljednje doze lijeka.
Vrijeme za hranjenje
Studija na majmunima Cynomolgus tijekom laktacije, u dozama 25 puta većim od tjedne doze održavanja za ljude od 2 mg / kg Herceptin intravenozne formulacije, pokazalo se da se trastuzumab izlučuje u mlijeku. Prisutnost trastuzumaba u serumu majmuna novorođenčeta nije bila povezana s nikakvim štetnim učincima na rast ili razvoj od rođenja do 1 mjeseca starosti. Nije poznato izlučuje li se trastuzumab u majčinom mlijeku kod ljudi. Budući da se ljudski IgG1 izlučuje u majčino mlijeko, a potencijalni rizik od oštećenja novorođenčeta nije poznat, žene ne bi trebale dojiti tijekom terapije Herceptinom i 7 mjeseci nakon posljednje doze.
Plodnost
Nema dostupnih podataka o plodnosti.
04.7 Utjecaj na sposobnost upravljanja vozilima i rada sa strojevima
Herceptin nema ili ima zanemariv utjecaj na sposobnost upravljanja vozilima i rada sa strojevima. Međutim, pacijente koji razviju simptome povezane s infuzijom (vidjeti dio 4.4) treba savjetovati da ne voze i ne rade sa strojevima dok se simptomi ne povuku.
04.8 Nuspojave
Sažetak sigurnosnog profila
Najozbiljnije i / ili najčešće nuspojave prijavljene do sada s primjenom Herceptina (intravenozna formulacija i potkožna formulacija) uključuju: srčanu disfunkciju, infuzijske reakcije, hematotoksičnost (osobito neutropeniju), infekcije i plućne nuspojave.
Tablični popis nuspojava
U ovom su odjeljku korištene sljedeće kategorije učestalosti: vrlo česte (≥1 / 10), česte (≥1 / 100,
U tablici 1 prikazane su nuspojave prijavljene pri uporabi intravenske primjene Herceptina samog ili u kombinaciji s kemoterapijom u ključnim kliničkim ispitivanjima i u razdoblju nakon stavljanja lijeka u promet.
Svi uključeni izrazi odnose se na najveći postotak uočen u ključnim kliničkim studijama.
Tablica 1: Neželjeni učinci prijavljeni pri intravenskoj primjeni Herceptina samih ili u kombinaciji s kemoterapijom u ključnim kliničkim ispitivanjima (N = 8386) i u razdoblju nakon stavljanja lijeka u promet
+ Ukazuje na nuspojave prijavljene u vezi sa smrtonosnim ishodom.
1 Označava nuspojave prijavljene uglavnom u vezi s reakcijama povezanim s infuzijom. Nema specifičnih postotaka za njih.
* Promatrano uz kombiniranu terapiju nakon liječenja antraciklinima, u kombinaciji s taksanima.
Opis specifičnih nuspojava
Srčana disfunkcija
Zastoj srca (NYHA klasa II-IV) česta je nuspojava povezana s primjenom Herceptina i povezana je sa smrtonosnim ishodom (vidjeti dio 4.4). Znakovi i simptomi srčane disfunkcije, poput dispneje, ortopneje, pojačanog kašlja, plućnog edema, s3 galopa, smanjene frakcije izbacivanja ventrikula, primijećeni su u bolesnika liječenih Herceptinom (vidjeti dio 4.4).
U 3 ključna klinička ispitivanja s Herceptinom kao pomoćnim sredstvom u kombinaciji s kemoterapijom, učestalost srčane disfunkcije stupnja 3/4 (posebno simptomatsko kongestivno zatajenje srca) bila je slična u bolesnika koji su primali samo kemoterapiju (npr. Oni koji nisu primali Herceptin) i u pacijenata koji su primali Herceptin uzastopno nakon taksana (0,3-0,4 %). Najveći postotak opažen je kod pacijenata koji su primali Herceptin istodobno s taksanom (2,0 %). Iskustvo s istodobnom primjenom Herceptina i niskim dozama antraciklinskih režima u neoadjuvantnom okruženju je ograničeno (vidi odjeljak 4.4).
Kada se Herceptin davao nakon završetka adjuvantne kemoterapije, zatajenje srca NYHA klase III-IV primijećeno je u 0,6% pacijenata u liječenoj ruci tijekom jedne godine nakon medijana praćenja od 12 mjeseci. U studiji BO16348, nakon medijana praćenja od 8 godina, učestalost teške CHF (NYHA klase III i IV) u jednogodišnjoj skupini liječenja Herceptinom bila je 0,8%, a stopa disfunkcije lijeve klijetke bila je blago simptomatska i asimptomatska 4,6% .
Ozbiljna reverzibilnost CHF -a opažena je u 71,4% pacijenata liječenih Herceptinom (definirano kao niz od najmanje dvije uzastopne vrijednosti LVEF ≥50% nakon događaja). Reverzibilnost je dokazana u 79,5% pacijenata. Blago simptomatskih i asimptomatskih disfunkcija lijeve klijetke Približno 17% događaja povezanih sa srčanom disfunkcijom dogodilo se nakon završetka liječenja Herceptinom.
U ključnim studijama o liječenju metastatskih bolesti intravenoznim pripravkom Herceptin, učestalost srčanih disfunkcija varirala je između 9% i 12% kada se lijek primjenjivao u kombinaciji s paklitakselom u usporedbi s 1% - 4% samo za paklitaksel. U monoterapiji stopa je bila 6% - 9%. Najveća učestalost srčane disfunkcije dogodila se u bolesnika koji su primali Herceptin istodobno s antraciklinima / ciklofosfamidom (27%), a bila je značajno veća nego sa samo antraciklinima / ciklofosfamidom (7% - 10%). U kasnijoj kliničkoj studiji s prospektivnim praćenjem rada srca utvrđeno je da je incidencija simptomatskog kongestivnog zatajenja srca 2,2% u bolesnika liječenih Herceptinom i docetakselom u usporedbi s 0% u bolesnika liječenih monoterapijom docetakselom. Dio pacijenata (79% ) koji su razvili srčanu disfunkciju u ovim kliničkim ispitivanjima poboljšali su se nakon standardnog liječenja za kongestivno zatajenje srca.
Reakcije na infuziju, reakcije alergijskog tipa i preosjetljivost
Procjenjuje se da će otprilike 40% pacijenata liječenih Herceptinom doživjeti neki oblik infuzijske reakcije.Međutim, većina infuzijskih reakcija je blagog do umjerenog intenziteta (NCI-CTC bodovni sustav) i imaju tendenciju da se jave na početku liječenja, tj. Tijekom jedne infuzije , dva i tri, s manje učestalosti u sljedećim infuzijama. Takve reakcije uključuju zimicu, vrućicu, dispneju, hipotenziju, piskanje, bronhospazam, tahikardiju, smanjenu zasićenost kisikom, respiratorni distres, osip, mučninu, povraćanje i glavobolju (vidjeti dio 4.4). Stopa reakcija povezanih s infuzijom svih stupnjeva varirala je u različitim studijama ovisno o indikacijama, načinu prikupljanja podataka i primjeni trastuzumaba istodobno s kemoterapijom ili monoterapijom.
Teške anafilaktičke reakcije koje zahtijevaju hitne dodatne intervencije obično se mogu pojaviti tijekom prve i druge infuzije Herceptina (vidjeti dio 4.4) i bile su povezane sa smrtonosnim ishodom.
U izoliranim slučajevima opažene su anafilaktoidne reakcije.
Hematotoksičnost
Febrilna neutropenija i leukopenija vrlo su često uočeni događaji. Uobičajeno razvijajuće se nuspojave uključuju: anemija, trombocitopenija i neutropenija. Učestalost epizoda hipoprotrombinemije nije poznata. Rizik od neutropenije može se neznatno povećati pri primjeni trastuzumaba s docetakselom nakon terapije antraciklinima.
Plućni događaji
Ozbiljne plućne nuspojave javljaju se povezane s primjenom Herceptina i povezane su sa smrtonosnim ishodom. One uključuju, ali nisu ograničene na, plućne infiltrate, sindrom akutnog respiratornog distresa, upalu pluća, upalu pluća, pleuralni izljev, respiratorni distres, akutnu plućnu bolest edem i zatajenje disanja (vidjeti dio 4.4).
Pojedinosti o mjerama za smanjenje rizika koje su u skladu s Europskim planom upravljanja rizicima predstavljene su u Posebnim upozorenjima i mjerama opreza za uporabu (odjeljak 4.4).
Imunogenost
U uvjetima neoadjuvantno-adjuvantnog EBC liječenja, 8,1% (24/296) pacijenata liječenih intravenoznim Herceptinom razvilo je antitijela protiv trastuzumaba (bez obzira na prisutnost antitijela na početku). Neutralizirajuća protutijela na trastuzumab otkrivena su u uzorcima nakon početka ispitivanja u 2 od 24 bolesnika liječena intravenoznim Herceptinom.
Klinička važnost ovih antitijela je nepoznata; međutim, čini se da ta antitijela nisu ugrozila farmakokinetiku, učinkovitost (utvrđenu kompletnim patološkim odgovorom [pCR]) i sigurnost intravenoznog primjene Herceptina određenu pojavom reakcija povezanih s davanjem (ARR).
Nema dostupnih podataka o imunogenosti za Herceptin kod raka želuca.
Prelazak s liječenja Herceptin intravenoznom formulacijom na liječenje s Herceptin potkožnim oblikom i obrnuto
Studija MO22982 ispitivala je prijelaz s liječenja Herceptin intravenoznom formulacijom na liječenje Herceptin potkožnom formulacijom s primarnim ciljem procjene sklonosti pacijenata za intravenoznu ili potkožnu primjenu trastuzumaba. U pokusu su analizirane 2 kohorte (jedna je tretirana potkožnom formulacijom u bočici, a druga potkožnom formulacijom putem uređaja za isporuku) koristeći cross-over dizajn s dvije ruke, pri čemu je 488 pacijenata randomizirano u jednu od dvije različite sekvence liječenja Herceptinom koje su dobivale svaki tri tjedna (iv [Ciklusi 1-4] → sc [Ciklusi 5-8] ili sc [Ciklusi 1-4] → iv [Ciklusi 5-8]). Osobe koje nisu liječene Herceptinom IV (20,3%) ili prethodno izložene IV Herceptinu (79,7%). Za IV → sc sekvencu (kombinirane kohorte formulacije potkožne bočice i formulacije uređaja za potkožnu primjenu) stope povezane s nuspojavama (svih stupnjeva) opisane su prije prelaska (ciklusi 1-4) i nakon prebacivanja (ciklusi 5-8) kao 53,8% naspram 56,4%; za sekvencu sc → ev (kombinirane kohorte scina bočica i s.c. putem uređaja za isporuku), stope nuspojava (svih stupnjeva) opisane su prije prebacivanja i nakon prebacivanja kao 65,4% u odnosu na 48,7%.
Prije prelaska (ciklusi 1-4), stope početka ozbiljnih nuspojava, nuspojava 3. stupnja i prekid liječenja zbog nuspojava bile su niske (
Prijavljivanje sumnji na nuspojave
Izvještavanje o sumnji na nuspojave koje se jave nakon odobrenja lijeka važno je jer omogućuje kontinuirano praćenje omjera koristi i rizika lijeka. Od zdravstvenih djelatnika se traži da prijave sve sumnje na nuspojave putem nacionalnog sustava za prijavljivanje. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Predoziranje
U kliničkim studijama na ljudima nisu zabilježeni slučajevi predoziranja. U kliničkim ispitivanjima nisu primijenjene pojedinačne doze Herceptina, veće od 10 mg / kg. Do ove razine doze su se dobro podnosile.
05.0 FARMAKOLOŠKA SVOJSTVA
05.1 Farmakodinamička svojstva
Farmakoterapijska skupina: Antineoplastična sredstva, monoklonska protutijela, ATC oznaka: L01XC03
Trastuzumab je rekombinantno humanizirano monoklonsko protutijelo IgG1 protiv receptora 2 humanog epitelnog faktora rasta (HER2). Prekomjerna ekspresija HER2 opažena je u 20% -30% primarnih karcinoma dojke. Studije o stopama pozitivnosti HER2 u karcinomu želuca (GC) otkrivene imunohistokemijom (IHC) i hibridizacijom in situ fluorescentna (FISH) ili hibridizacija in situ kromogeni (CISH) pokazali su da postoji "široka varijabilnost pozitivnosti HER2 u rasponu od 6,8% do 34,0% za IHC i 7,1% do 42,6% za FISH." Studije su pokazale da bolesnice s rakom dojke s prekomjernom ekspresijom HER2 imaju kraće preživljenje bez bolesti od pacijenata s rakom bez prekomjerne ekspresije HER2. Izvanstanična domena receptora (ECD, p105) može se otpustiti u krvotok i mjeriti u uzorcima seruma.
Mehanizam djelovanja
Trastuzumab se veže s "visokim afinitetom i specifičnošću za poddomenu IV, perimembransku regiju izvanstanične domene HER2. Vezanje trastuzumaba za HER2 inhibira signaliziranje HER2 neovisno o ligandu i sprječava proteolitičko cijepanje njegove izvanstanične domene, mehanizam aktivacije HER2 Posljedično, trastuzumab je pokazao oboje in vitro kod životinja, kako bi mogao inhibirati proliferaciju stanica humanih tumora koje pretjerano eksprimiraju HER2. Nadalje, trastuzumab je moćan posrednik stanično posredovane citotoksičnosti ovisne o antitijelima (ADCC). In vitro Pokazalo se da se ADCC posredan trastuzumabom preferirano vrši na tumorske stanice s prekomjernom ekspresijom HER2 nad tumorskim stanicama koje ne pretjerano eksprimiraju HER2.
Otkrivanje prekomjerne ekspresije HER2 ili pojačanja gena HER2
Otkrivanje prekomjerne ekspresije HER2 ili pojačanja gena HER2 kod raka dojke
Herceptin se smije koristiti samo u bolesnika s rakom s prekomjernom ekspresijom HER2 ili amplifikacijom gena HER2 kako je utvrđeno točnim i potvrđenim testom. Prekomjerna ekspresija HER2 mora se otkriti imunohistokemijskim (IHC) pregledom fiksiranih presjeka tumora (vidjeti dio 4.4). Pojačanje gena HER2 mora se otkriti hibridizacijom in situ fluorescencijom (FISH) ili hibridizacijom in situ kromogeni (CISH) fiksiranih presjeka tumora.Pacijenti koji pokazuju izraženu prekomjernu ekspresiju HER2 s naznakom IHC ocjene 3+ ili pozitivnog rezultata FISH ili CISH kandidati su za liječenje Herceptinom.
Kako bi se osigurali točni i ponovljivi rezultati, ispitivanja se moraju provesti u specijaliziranim laboratorijima koji mogu jamčiti validaciju analitičkih postupaka.
Preporučeni sustav za bodovanje modela označavanja IHC -a je onaj prikazan u tablici 2:
Tablica 2 Preporučeni sustav za bodovanje IHC uzoraka označavanja u raku dojke
Općenito, FISH test se smatra pozitivnim ako je omjer broja kopija gena HER2 po tumorskoj stanici prema broju kopija kromosoma 17 veći ili jednak 2 ili ako postoji više od 4 kopije HER2 gen za tumorsku stanicu ako se kao referenca ne koristi kromosom 17.
Općenito, CISH test se smatra pozitivnim ako postoji više od 5 kopija gena HER2 po jezgri u više od 50% stanica raka.
Za potpune upute o izvođenju i tumačenju ispitivanja pogledajte letke koji se nalaze u validiranim ispitnim pakiranjima FISH i CISH. Mogu se primijeniti i službene preporuke o testiranju HER2.
Za bilo koju drugu metodu koja se može koristiti za procjenu ekspresije proteina ili gena HER2, analize bi trebale provoditi samo laboratoriji koji osiguravaju optimalnu učinkovitost potvrđenih metoda. Takve metode moraju biti jasne, precizne i dovoljno točne da pokažu prekomjernu ekspresiju HER2 i moraju razlikovati umjerenu (razina 2+) od visoke (razina 3+) prekomjernu ekspresiju HER2.
Otkrivanje prekomjerne ekspresije HER2 ili pojačanja gena HER2 kod raka želuca
Za utvrđivanje prekomjerne ekspresije ili amplifikacije HER2 gena HER2 trebao bi se koristiti samo točan i potvrđen test. IHC se preporučuje kao prvi test, a u slučajevima gdje je također potrebna procjena amplifikacije gena HER2, treba se koristiti in situ hibridizacija iona srebra (SISH) ili FISH tehnika. Međutim, preporučuje se tehnologija SISH koja omogućuje paralelnu procjenu histologije i morfologije tumora. Kako bi se osigurala valjanost postupaka ocjenjivanja i dobivanje točnih i ponovljivih rezultata, HER2 test mora se provesti u laboratoriju s obučenim osobljem. Cjelovite upute o izvođenju testa i tumačenju rezultata nalaze se u tehničkom listu proizvoda koji se isporučuje s testovima koji se koriste za ocjenjivanje HER2.
U ToGA studiji (BO18255), pacijenti čiji su tumori bili IHC3 + ili FISH pozitivni definirani su kao HER2-pozitivni i stoga su uključeni u studiju. Na temelju rezultata kliničkih studija, pozitivni učinci bili su ograničeni na bolesnike s višom razinom prekomjerne ekspresije proteina HER2, definirane kao 3+ s IHC ili 2+ s IHC i pozitivan rezultat FISH.
U studiji usporedbe metodologije (studija D008548) uočen je visok stupanj slaganja (> 95%) između SISH i FISH tehnika za određivanje amplifikacije gena HER2 u pacijenata s rakom želuca.
Prekomjerna ekspresija HER2 mora se odrediti imunohistokemijskim (IHC) ispitivanjem fiksiranih presjeka tumora.Pojačanje gena HER2 mora se otkriti hibridizacijom in situ, pomoću SISH -a ili FISH -a, na fiksnim presjecima tumora.
Preporučeni sustav za bodovanje modela označavanja IHC -a je onaj prikazan u tablici 3:
Tablica 3 Preporučeni sustav za bodovanje IHC oznaka za karcinom želuca
Općenito, SISH ili FISH testovi smatraju se pozitivnim ako je omjer broja kopija gena HER2 po tumorskoj stanici prema broju kopija kromosoma 17 veći ili jednak 2.
Klinička učinkovitost i sigurnost
Metastatski rak dojke
Herceptin se samostalno koristio u kliničkim ispitivanjima u pacijenata s MBC s tumorima koje karakterizira prekomjerna ekspresija HER2 i neuspjeh jednog ili više prethodnih režima kemoterapije za metastatsku bolest (samo Herceptin).
Herceptin se također koristio u kombinaciji s paklitakselom ili docetakselom za liječenje metastatskih bolesti koje se nisu liječile kemoterapijom. Pacijenti prethodno liječeni adjuvantnom kemoterapijom na bazi antraciklina liječeni su paklitakselom (175 mg / m2 primijenjenim u obliku 3-satne infuzije) sa ili bez Herceptina. U ključnoj studiji s docetakselom (100 mg / m2 u obliku infuzije od 1 sata) sa ili bez Herceptina, 60% pacijenata prethodno je primalo adjuvantnu kemoterapiju na bazi antraciklina. Pacijenti su liječeni Herceptinom do progresije bolesti.
Učinkovitost Herceptina u kombinaciji s paklitakselom u pacijenata koji prethodno nisu primali adjuvantnu terapiju antraciklinima nije ispitivana. Međutim, kombinacija Herceptina i docetaksela bila je učinkovita, bez obzira na to jesu li bolesnici prethodno primali adjuvantnu terapiju ili nisu. S antraciklinima.
Metoda koja se koristi za analizu prekomjerne ekspresije HER2 i utvrđivanje podobnosti pacijenata za sudjelovanje u ključnim kliničkim ispitivanjima monoterapije Herceptinom i Herceptinom plus paklitakselom upotrijebila je HER2 imunohistokemijsko bojenje fiksiranog materijala iz tumora dojke, koristeći mišja monoklonska protutijela CB11 i 4D5. Ta su tkiva fiksirana u formalinu ili Bouin -ov fiksator. Ova metoda ispitivanja koja se koristila u kliničkim studijama i provedena u središnjem laboratoriju koristila je ljestvicu od 0 do 3+. Uključeni su pacijenti klasificirani po 2+ ili 3+ bojenju, dok su oni s 0 ili 1+ bojenjem isključeni Više od 70% upisanih pacijenata imalo je 3+ "prekomjernu ekspresiju". Dobiveni podaci ukazuju na to da su korisni učinci bili veći u bolesnika s višom razinom prekomjerne ekspresije HER2 (3+).
Primarna metoda ispitivanja koja se koristila za određivanje pozitivnosti na HER2 u ključnoj studiji s docetakselom, sa ili bez Herceptina, bila je imunohistokemija. Manji broj pacijenata testiran je hibridizacijom. in situ u fluorescenciji (FISH). U ovom je istraživanju 87% uključenih pacijenata karakteriziralo IHC3 + bolest, a 95% IHC3 + i / ili FISH-pozitivna bolest.
Tjedna primjena kod metastatskog raka dojke
Rezultati učinkovitosti monoterapije i kombiniranih studija sažeti su u tablici 4:
Tablica 4 Rezultati učinkovitosti iz studija monoterapije i kombinirane terapije
TTP = vrijeme do progresije; "n.a." ukazuje da se nije moglo ocijeniti ili da još nije postignuto.
1 Studija H0649g: IHC3 + subpopulacije pacijenata
2 Studija H0648g: Subpopulacije pacijenata s IHC3 +
3 Studija M77001: Populacija koja se namjerava liječiti, rezultati nakon 24 mjeseca
Kombinirano liječenje Herceptinom anastrozolom
Herceptin je ispitivan u kombinaciji s anastrozolom za prvu liniju liječenja pacijenata u postmenopauzi s HER2 pozitivnim na hormonske receptore s prekomjernom ekspresijom MBC (npr. Estrogenski receptor (ER) i / ili receptor progesterona (PR)). Preživljavanje bez progresije udvostručilo se u lijeku Herceptin u kombinaciji s anastrozolom u usporedbi s grupom samo s anastrozolom (4,8 mjeseci u odnosu na 2,4 mjeseca). Za ostale parametre, poboljšanja primijećena u kombiniranoj skupini bila su: ukupni odgovor (16,5% naspram 6,7%), klinička korist (42,7% naspram 27,9%), vrijeme do progresije (4, 8 mjeseci naspram 2,4 mjeseca). Nije bilo razlike između dva kraka u smislu vremena do odgovora i trajanja odgovora. Srednje ukupno preživljenje produženo je za 4,6 mjeseci u bolesnika u kombiniranoj skupini. Razlika nije bila statistički značajna, međutim više od polovice pacijenata uključenih samo u anastrozolsku ruku liječeno je režimom koji je sadržavao Herceptin nakon progresije bolesti.
Primjena svaka tri tjedna kod metastatskog raka dojke
Podaci o učinkovitosti iz usporednih studija monoterapije i kombinirane terapije sažeti su u donjoj tablici 5:
Tablica 5. Rezultati učinkovitosti iz neusporednih studija provedenih u monoterapiji i u kombiniranoj terapiji
TTP = vrijeme do progresije; "n.a." ukazuje da se nije moglo ocijeniti ili da još nije postignuto.
1. Studija WO16229: 8 mg / kg opterećujuća doza, nakon čega slijedi 6 mg / kg svaka 3 tjedna
2. Studija MO16982: opterećujuća doza 6 mg / kg tjedno 3 puta; zatim 6 mg / kg svaka 3 tjedna
3. Studija BO15935
4. Studija MO16419
Mjesta progresije
Stopa progresije jetre bila je značajno smanjena u bolesnika liječenih kombinacijom Herceptin-paklitaksel u usporedbi s samim paklitakselom (21,8% naspram 45,7%; p = 0,004). Više je pacijenata liječenih Herceptinom i paklitakselom pokazalo progresiju središnjeg živčanog sustava u usporedbi s bolesnicima liječenima sam paklitaksel (12,6% naspram 6,5%; p = 0,377).
Rani stadij raka dojke (adjuvantna postavka)
Rak dojke u ranoj fazi definira se kao invazivni, nemetastatski primarni rak dojke.
Upotreba Herceptina u kontekstu adjuvantne terapije ispitivana je u 4 velike, multicentrične, randomizirane studije:
• Studija BO16348 osmišljena je za usporedbu liječenja Herceptinom svaka tri tjedna tijekom jedne i dvije godine u odnosu na promatranje samo u bolesnika s HER2 pozitivnim EBC -om nakon operacije, standardne kemoterapije i radioterapije (ako je primjenjivo). Također je napravljena usporedba između liječenja Herceptinom jedne godine i liječenja Herceptinom dvije godine. Pacijenti koji su namjeravali primati Herceptin dobili su početnu učitavajuću dozu od 8 mg / kg, zatim 6 mg / kg svaka tri tjedna tijekom jedne godine ili dvije godine.
• Studije NSAPB B-31 i NCCTG N9831, uključujući zbirnu analizu, osmišljene su za procjenu kliničke korisnosti kombiniranja liječenja Herceptinom s paklitakselom nakon AC kemoterapije; osim toga, studija NCCTG N9831 također je evaluirala sekvencijalno dodavanje Herceptina u odnosu na AC → P kemoterapiju u pacijenata s HER2 pozitivnom EBC nakon operacije.
• Studija BCIRG 006 osmišljena je za procjenu povezanosti liječenja Herceptinom s docetakselom nakon AC kemoterapije ili docetaksela i karboplatina u bolesnika s HER2 pozitivnom EBC nakon operacije.
Početni karcinom dojke u studiji HERA bio je ograničen na operabilan, primarni, invazivni adenokarcinom dojke s pozitivnim aksilarnim limfnim čvorovima ili negativnim aksilarnim limfnim čvorovima, ako ima tumor promjera najmanje 1 cm.
U objedinjenoj analizi NSAPB B-31 i NCCTG N9831, EBC je bio ograničen na žene s operabilnim rakom dojke visokog rizika, definiranog kao HER2 pozitivan i pozitivan na aksilarnim limfnim čvorovima ili HER2 pozitivan i aksilarni limfni čvor s visokim karakteristikama rizika (veličina tumora > 1 cm i ER negativan ili veličina tumora> 2 cm, bez obzira na hormonski status).
U studiji BCIRG 006, HER2 pozitivan EBC bio je ograničen na čvorno pozitivne ili čvorno negativne pacijente s visokim rizikom definiranim kao odsutno zahvaćanje limfnih čvorova (pN0) i najmanje 1 od sljedećeg: veličina tumora veća od 2 cm, estrogenski receptori i progesteron negativan, histološki i / ili nuklearni stupanj 2-3 ili stariji
Tablica 6 sažima rezultate djelotvornosti iz studije BO16348 nakon medijalnog praćenja od 12 mjeseci *i 8 godina **:
Tablica 6 Rezultati učinkovitosti iz studije BO16348
* Jednogodišnja primarna krajnja točka DFS-a u odnosu na promatranje dosegla je zadanu statističku granicu
** Konačna analiza (uključujući ukrštanje 52% pacijenata iz promatračke ruke na Herceptin)
*** Postoji ukupna razlika u uzorku zbog malog broja pacijenata randomiziranih nakon graničnog datuma za analizu medijana za 12 mjeseci
Rezultati privremene analize učinkovitosti premašili su unaprijed utvrđenu statističku granicu protokola za usporedbu Herceptina tijekom jedne godine u odnosu na promatranje. Nakon medijana praćenja od 12 mjeseci, omjer opasnosti (HR) za preživljavanje bez bolesti (DFS) iznosio je 0,54 (95% CI 0,44-0,67) što predstavlja apsolutnu korist, u smislu dvogodišnje stope preživljavanja bez bolesti, od 7,6 postotnih bodova (85, 8% naspram 78,2%) u korist skupine lijeka Herceptin.
Nakon medijana praćenja od 8 godina, provedena je konačna analiza koja je otkrila da je liječenje s Herceptinom tijekom jedne godine bilo povezano sa smanjenjem rizika za 24% u usporedbi sa samim promatranjem (HR = 0,76, CI na 95% 0,67 - 0,86) predstavlja apsolutnu korist u smislu osmogodišnje stope preživljavanja bez progresije bolesti od 6,4 postotnih bodova u korist liječenja Herceptinom tijekom jedne godine.
U ovoj konačnoj analizi, produljenje liječenja Herceptinom za dvije godine nije pokazalo nikakvu dodatnu korist u odnosu na liječenje za godinu dana [HR DFS u 2-godišnjoj naspram 1-godišnje populacije namjere liječenja (ITT) = 0,99 (95% CI: 0,87 - 1,13), p -vrijednost = 0,90 i HR OS = 0,98 (0,83 - 1,15); p -vrijednost = 0,78] Stopa asimptomatske disfunkcije lijeve klijetke povećana je u skupini za liječenje 2 godine (8,1% naspram 4,6% u više bolesnika imalo je najmanje jedan štetni događaj stupnja 3 ili 4 u dvogodišnjoj skupini liječenja (20,4%) u odnosu na godinu dana liječenja (16,3%).
U studijama NSAPB B-31 i NCCTG N9831, Herceptin je primijenjen u kombinaciji s paklitakselom, nakon AC kemoterapije.
Istodobno su davani doksorubicin i ciklofosfamid:
• intravenski potisni doksorubicin, 60 mg / m2, primijenjen svaka 3 tjedna tijekom 4 ciklusa.
• intravenozni ciklofosfamid, 600 mg / m2 tijekom 30 minuta, primijenjen svaka 3 tjedna tijekom 4 ciklusa
Paclitaxel, u kombinaciji s Herceptinom, primijenjen je na sljedeći način:
• intravenski paklitaksel - 80 mg / m2 kao kontinuirana intravenska infuzija, koja se daje jednom tjedno tijekom 12 tjedana,
ili
• intravenski paklitaksel - 175 mg / m2 u obliku kontinuirane intravenske infuzije, primijenjen jednom svaka 3 tjedna tijekom 4 ciklusa (1. dan svakog ciklusa).
Rezultati učinkovitosti iz združene analize NSAPB B-31 i NCCTG 9831 u vrijeme konačne analize DFS * sažeti su u Tablici 7. Prosječno trajanje praćenja bilo je 1,8 godina za bolesnike u AC grupi → P i 2,0 godine za pacijente u ruci AC → PH.
Tablica 7 Sažetak rezultata učinkovitosti iz objedinjene analize NSABP B-31 i NCCTG 9831 u vrijeme konačne analize DFS-a *
A: doksorubicin; C: ciklofosfamid; P: paklitaksel; H: trastuzumab
* Pri prosječnom trajanju praćenja od 1,8 godina za bolesnike u skupini AC → P i 2,0 godine za bolesnike u skupini AC → PH.
** P-vrijednost za OS nije prelazila unaprijed utvrđenu statističku granicu za usporedbu AC → PH u odnosu na AC → P.
U odnosu na "krajnja točka primarni, DFS, dodavanjem Herceptina kemoterapiji paklitakselom rezultiralo je smanjenjem rizika od ponavljanja bolesti za 52%. Omjer opasnosti prevodi se u apsolutnu korist, u smislu stope preživljavanja bez bolesti u 3 godine od 11,8% (87,2% u odnosu na 75,4 %) u korist AC → PH (Herceptin) kraka.
U vrijeme ažuriranja sigurnosti, nakon medijana praćenja od 3,5-3,8 godina, "analiza DFS-a ponovno je potvrdila opseg koristi prikazane u konačnoj analizi DFS-a. križanje Herceptina u kontrolnoj skupini, dodavanje Herceptina kemoterapiji paklitakselom rezultiralo je smanjenjem rizika od ponavljanja bolesti za 52%. Dodavanje Herceptina kemoterapiji paklitakselom također je rezultiralo smanjenjem recidiva bolesti od 37%. rizik od smrti.
Konačna unaprijed planirana analiza OS-a iz kombinirane analize studija NSABP B-31 i NCCTG 9831 provedena je u vrijeme 707 smrti (medijan praćenja 8,3 godine u skupini AC → PH). U usporedbi s onom primijećenom pri liječenju AC → P, liječenje AC → PH rezultiralo je statistički značajnim poboljšanjem OS-a (stratificirani HR = 0,64; 95% CI [0,55-0,74]; p-vrijednost log-rank
Konačni rezultati OS-a iz zbirne analize NSABP B-31 i NCCTG 9831 sažeti su u donjoj tablici 8.
Tablica 8 Konačna analiza ukupnog preživljavanja iz kombinirane analize NSABP B-31 i NCCTG 9831
A: doksorubicin; C: ciklofosfamid; P: paklitaksel; H: trastuzumab
DFS analiza je također provedena u konačnoj analizi OS -a koja je proizašla iz kombinirane analize NSABP B -31 i NCCTG N9831. Ažurirani rezultati DFS analize (stratificirani HR = 0,61; 95% CI [0,54 - 0,69]) pokazali su Korist od DFS -a slična je onoj koja je uočena u konačnoj primarnoj analizi DFS -a, unatoč 24,8% pacijenata koji su prešli AC → P ruku na terapiju Herceptinom. Stopa preživljavanja bez bolesti od 77,2% (95% CI: 75,4% - 79,1% ) u skupini AC → PH procijenjena je na 8 godina, s apsolutnom koristi od 11,8% u usporedbi s grupom AC → P.
U studiji BCIRG 006 Herceptin je davan u kombinaciji s docetakselom, nakon kemoterapije AC (AC → DH) ili u kombinaciji s docetakselom i karboplatinom (DCarbH).
Docetaksel je primijenjen na sljedeći način:
• intravenski docetaksel - 100 mg / m2 kao 1 -satna intravenska infuzija koja se daje svaka 3 tjedna tijekom 4 ciklusa (2. dan prvog ciklusa docetaksela, zatim 1. dan svakog sljedećeg ciklusa)
ili
• intravenski docetaksel - 75 mg / m2 kao 1 -satna intravenska infuzija, koja se daje svaka 3 tjedna tijekom 6 ciklusa (2. dan prvog ciklusa, zatim 1. dan svakog sljedećeg ciklusa)
slijedi:
• karboplatin - pri ciljanoj AUC = 6 mg / ml / min primijenjen kao intravenska infuzija u trajanju od 30-60 minuta ponavlja se svaka 3 tjedna tijekom ukupno šest ciklusa
Herceptin se davao jednom tjedno u kombinaciji s kemoterapijom, a nakon toga svaka 3 tjedna ukupno 52 tjedna.
Rezultati učinkovitosti iz BCIRG-a 006 sažeti su u tablice 9 i 10. Srednje trajanje praćenja bilo je 2,9 godina u skupini AC → D i 3,0 godine u svakoj skupini AC → DH i DCarbH.
Tablica 9 Sažetak analiza učinkovitosti iz studije BCIRG 006 AC → D protiv AC → DH
AC → D = doksorubicin u kombinaciji s ciklofosfamidom, zatim docetaksel; AC → DH = doksorubicin u kombinaciji s ciklofosfamidom, zatim docetaksel u kombinaciji s trastuzumabom; CI = interval pouzdanosti.
Tablica 10 Sažetak analiza učinkovitosti iz studije BCIRG 006 AC → D protiv DCarbH
AC → D = doksorubicin u kombinaciji s ciklofosfamidom, zatim docetaksel; DCarbH = docetaksel, karboplatin i trastuzumab; CI = interval pouzdanosti
U studiji BCIRG 006 koja se odnosi na "krajnja točka primarni, DFS, omjer opasnosti prevodi se u apsolutnu korist, u smislu trogodišnjeg preživljavanja bez bolesti, od 5,8 postotnih bodova (86,7% naspram 80,9%) u korist AC → DH skupine (Herceptin) i 4,6 postotnih bodova (85,5% naspram 80,9%) u korist ruke DCarbH (Herceptin) u odnosu na AC → D.
U studiji BCIRG 006, 213/1075 pacijenata u skupini DCarbH (TCH), 221/1074 pacijenata u grupi AC DH (AC TH) i 217/1073 u skupini AC → D (AC T) imalo je Karnofskyjev učinak ≤ 90 (80 ili 90). U ovoj podskupini pacijenata nije primijećena nikakva korist od preživljavanja bez bolesti (DFS) (omjer opasnosti = 1,16; 95% CI [0,73, 1,83] za DCarbH (TCH) u odnosu na AC skupinu. D (AC T); omjer opasnosti 0,97; 95% CI [0,60, 1,55] za AC DH (AC TH) naspram AC D kraka).
Osim toga, provedena je analiza post-hoc eksplorativni podaci iz zajedničke analize (JA) NSABP B-31 / NCCTG N9831 i kliničke studije BCIRG006, koji kombiniraju DFS i simptomatske srčane događaje, sažeto u Tablici 11:
Tablica 11 Analiza post-hoc istraživanje rezultata zajedničke analize (JA) NSABP B-31 / NCCTG N9831 i kliničke studije BCIRG006, kombinirajući DFS i simptomatske srčane događaje
A: doksurobicin; C: ciklofosfamid; P: paklitaksel; D: docetaksel; Ugljikohidrati: karboplatin; H: trastuzumab
CI = interval pouzdanosti
* U vrijeme konačne analize DFS-a. Medijan trajanja praćenja bio je 1,8 godina u skupini AC → P i 2,0 godine u skupini AC → PH.
Rani stadij raka dojke (neoadjuvantno-adjuvantni kontekst)
Do danas nema dostupnih rezultata koji bi uspoređivali učinkovitost Herceptina primijenjenog s kemoterapijom u adjuvantnom okruženju s neoadjuvantnim / adjuvantnim okruženjem.
U kontekstu neoadjuvantno-adjuvantnog liječenja, studija MO16432, multicentrično, randomizirano kliničko ispitivanje, osmišljena je za procjenu kliničke učinkovitosti istodobne primjene Herceptina s neoadjuvantnom kemoterapijom koja sadrži i antraciklin i taksan, nakon čega slijedi Herceptin kao pomoćno sredstvo. na ukupno 1 godinu liječenja. Studija je uključivala pacijente s nedavno dijagnosticiranom lokalno uznapredovalom (stadij III) ili upalnom EBC. Bolesnici s tumorima HER2 + randomizirani su na neoadjuvantnu kemoterapiju istodobno s neoadjuvantno-adjuvantnom terapijom Herceptinom ili samo neoadjuvantnom kemoterapijom.
U studiji MO16432, Herceptin (učitavajuća doza od 8 mg / kg, nakon čega slijedi 6 mg / kg u održavanju svaka 3 tjedna) primijenjen je istodobno s 10 tijekova neoadjuvantne kemoterapije, kako slijedi:
• doksorubicin 60 mg / m2 i paklitaksel 150 mg / m2, primijenjeni svaka 3 tjedna kroz 3 ciklusa,
slijedi
• Paclitaxel 175 mg / m2 primijenjen svaka 3 tjedna kroz 4 ciklusa,
slijedi
• CMF 1. i 8. dan svaka 4 tjedna kroz 3 ciklusa,
nakon operacije slijedi
• dodatni tečajevi pomoćnog lijeka Herceptin (nakon završetka 1 godine terapije).
Rezultati učinkovitosti iz studije MO16432 sažeti su u Tablici 12. Srednje trajanje praćenja u skupini liječenom Herceptinom bilo je 3,8 godina.
Tablica 12 Rezultati učinkovitosti iz studije MO16432
* definirano kao odsutnost invazivnog karcinoma u dojci i aksilarnim limfnim čvorovima
Procijenjena je apsolutna korist od 13 postotnih bodova u korist grupe Herceptin u smislu trogodišnje stope preživljavanja bez događaja (65% naspram 52%).
Metastatski rak želuca
Herceptin je ispitivan u randomiziranoj, otvorenoj, fazi III ToGA studiji (BO18255) u kombinaciji s kemoterapijom u odnosu na samo kemoterapiju.
Kemoterapija se provodi na sljedeći način:
• kapecitabin - 1000 mg / m2 oralno dva puta dnevno tijekom 14 dana svaka 3 tjedna kroz 6 ciklusa (večer od prvog dana do jutra 15. dana svakog ciklusa)
ili
• Intravenski 5 -fluorouracil - 800 mg / m2 / dan u obliku kontinuirane intravenske infuzije tijekom 5 dana, koja se daje svaka 3 tjedna tijekom 6 ciklusa (dan 1 do 5 svakog ciklusa)
Svaki od dva lijeka primijenjen je sa:
• cisplatin - 80 mg / m2 svaka 3 tjedna tijekom 6 ciklusa, dan 1. dana svakog ciklusa.
Rezultati učinkovitosti iz studije BO18225 sažeti su u tablici 13:
Tablica 13 Rezultati učinkovitosti iz studije BO18225
FP + H: Fluoropirimidin / cisplatin + Herceptin
FP: fluoropirimidin / cisplatin
omjer izgledi
U studiju su uključeni pacijenti koji prethodno nisu bili liječeni zbog lokalno uznapredovalog ili recidiva i / ili metastatski neoperabilnog HER2 pozitivnog adenokarcinoma želuca ili gastroezofagealnog spoja, a nisu kandidati za kurativno liječenje. L "krajnja točka primarno je bilo ukupno preživljavanje, definirano kao vrijeme od datuma randomizacije do datuma smrti iz bilo kojeg uzroka. U vrijeme analize, umrlo je ukupno 349 randomiziranih pacijenata: 182 pacijenta (62,8%) u kontrolnoj skupini i 167 pacijenata (56,8%) u skupini liječenoj, povezanoj s temeljnim tumorom.
Post-hoc analiza podskupina pokazuje da su pozitivni učinci liječenja ograničeni na tumore s višom razinom proteina HER2 (IHC 2 + / FISH + ili IHC 3+). Srednje ukupno preživljenje u podskupini s visokom razinom prekomjerne ekspresije HER2 bilo je 11,8 mjeseci u odnosu na 16 mjeseci, HR 0,65 (95% CI 0,51-0,83), a preživljenje bez progresije bilo je 5,5 mjeseci naspram 7,6 mjeseci, HR 0,64 (95% CI 0,51-0,79) u skupini FP u odnosu na grupu FP + H, respektivno. ukupno preživljenje bilo je 0,75 (95% CI 0,51-1,11) u skupini IHC2 + / FISH + i 0,58 (95% CI 0,41-0,81) u skupini IHC3 + / FISH +.
U eksplorativnoj analizi podskupina provedenoj u studiji ToGA (BO18255) nije bilo očite ukupne koristi od preživljenja dodavanjem Herceptina u bolesnika s početnim ECOG PS 2 [HR 0,96 (95% CI 0, 51-1,79)], nemjerljivo [ HR 1,78 (95% CI 0,87-3,66)] i lokalno uznapredovale [HR 1,20 (95% CI 0,29-4,97)] bolesti.
Pedijatrijska populacija
Europska agencija za lijekove ukinula je obvezu podnošenja rezultata studija s Herceptinom u svim podskupinama u pedijatrijskoj populaciji za karcinom želuca i dojke (vidjeti dio 4.2 za informacije o pedijatrijskoj uporabi).
05.2 Farmakokinetička svojstva
Farmakokinetika trastuzumaba procijenjena je analizom populacijskog farmakokinetičkog modela koristeći združene podatke od 1582 ispitanika s HER2-pozitivnim MBC-om, EBC-om ili uznapredovalim karcinomom želuca (AGC) ili drugim rakom. Te zdravih dobrovoljaca u 18 studija I, II i III. u kojem je primijenjen Herceptin IV. Za opis koncentracije / vremenskog profila korišten je model s dva odjeljka s paralelnom linearnom i nelinearnom eliminacijom iz središnjeg odjeljka. Zbog nelinearne eliminacije ukupni klirens se povećavao sa smanjenjem koncentracije. Stoga, za trastuzumab se ne može zaključiti da postoji konstantna vrijednost vremena poluvijek. t1 / 2 opada sa smanjenjem koncentracija u rasponu doza (vidi tablicu 16.) Pacijenti s MBC i EBC imali su slične vrijednosti farmakokinetičkih parametara [npr. klirens (CL), volumen odjeljka na središnju (Vc) i populacijski predviđenu izloženost u stabilnom stanju (Cmin, Cmax i AUC)]. Linearni klirens iznosio je 0,136 L / dan za MBC, 0,112 L / dan za EBC i 0,176 L / dan za AGC. Vrijednosti parametara nelinearne eliminacije bile su 8,81 mg / dan za maksimalnu brzinu eliminacije (Vmax) i 8,92 mcg / mL za Michaelis-Mentenovu konstantu (Km) za bolesnike s MBC, EBC i AGC. Volumen središnjeg odjeljka bio je 2,62 l za bolesnike s MBC i EBC i 3,63 l za bolesnike s AGC. Uz primarni oblik tumora, konačni populacijski farmakokinetički model identificirao je tjelesnu težinu, serumsku aspartat aminotransferazu i albumin kao statistički kovarijantne značajne učinke koji utječu na izloženost trastuzumabu. Međutim, veličina učinka ovih kovarijata na izloženost trastuzumabu sugerirala je malo vjerojatan klinički značajan učinak na koncentracije trastuzumaba.
Vrijednosti izloženosti predviđene populacijskom farmakokinetikom (medijana s 5. do 95. percentilom) i vrijednosti farmakokinetičkih parametara u klinički značajnim koncentracijama (Cmax i Cmin) za bolesnike s MBC, EBC i AGC liječene odobrenim režimima doziranja q1w (tjedno doziranje) i q3w (doziranje svaka tri tjedna) prikazani su u tablici 14 (ciklus 1), tablici 15 (ravnotežno stanje) i tablici 16 (farmakokinetički parametri).
Tablica 14 Farmakokinetičke vrijednosti za populaciju predviđene izloženosti u ciklusu 1 (medijan 5 - 95. percentil) za režime liječenja Herceptinom IV u pacijenata s MBC, EBC i AGC
Tablica 15 Vrijednosti farmakokinetičke izloženosti u stanju mirovanja (5. - 95. percentil) za populaciju predviđene u stacionarnom stanju za režime liječenja Herceptinom IV u pacijenata s MBC, EBC i AGC
* Cmin, ss - Cmin u stanju mirovanja
** Cmax, ss = Cmax u ustaljenom stanju
*** vrijeme na 90% ustaljenog stanja
Tablica 16 Vrijednosti farmakokinetičkih parametara predviđenih za populaciju u stanju mirovanja za IV režime liječenja Herceptinom u pacijenata s MBC, EBC i AGC
Ispiranje trastuzumabom
Razdoblje ispiranja trastuzumaba procjenjivano je nakon intravenske primjene q1w ili q3w primjenom populacijskog farmakokinetičkog modela. Rezultati ovih simulacija pokazuju da će najmanje 95% pacijenata postići koncentraciju
Cirkulirajući topljivi antigen
Istraživačke analize kovarijata s podacima za samo jednu podskupinu pacijenata pokazale su da su ispitanici s višom razinom HER2-ECD topivog antigena (SHED) imali brži (niži Km) nelinearni klirens (p SGOT / AST; utjecaj topivog antigena na klirens može se pripisati SGOT / AST razine.
Nema podataka o razini cirkulirajuće izvanstanične domene receptora HER2 (topljivi antigen) u serumu pacijenata s rakom želuca.
05.3 Pretklinički podaci o sigurnosti
Nije bilo dokaza o jednokratnoj ili ponovljenoj toksičnosti ovisnoj o dozama u studijama koje su trajale do 6 mjeseci, niti o reproduktivnoj toksičnosti u studijama teratologije, plodnosti ili toksičnosti kod žena u posljednjem razdoblju trudnoće / placentnom prolazu. Herceptin nije genotoksičan.A Studija trehaloze, jednog od glavnih pomoćnih sastojaka formulacije, nije otkrila nikakvu toksičnost.
Dugotrajna istraživanja na životinjama nisu provedena kako bi se utvrdio kancerogeni potencijal Herceptina, niti kako bi se utvrdili njegovi učinci na plodnost muškaraca.
06.0 FARMACEUTSKE INFORMACIJE
06.1 Pomoćne tvari
L-histidin hidroklorid
L-histidin
a, a-trehaloza dihidrat
polisorbat 20
06.2 Nekompatibilnost
Ovaj lijek se ne smije miješati ili razrjeđivati s drugim lijekovima osim onih navedenih u odjeljku 6.6.
Nemojte razrjeđivati otopinama glukoze jer one uzrokuju nakupljanje proteina.
06.3 Razdoblje valjanosti
4 godine
Nakon rekonstitucije s vodom za injekcije, rekonstituirana otopina ostaje fizički i kemijski stabilna 48 sati na 2 ° C do 8 ° C. Ostaci rekonstituirane otopine moraju se odbaciti.
Herceptin otopine za infuziju u vrećicama od polivinil klorida, polietilena ili polipropilena koje sadrže 9 mg / ml (0,9%) otopine natrijevog klorida za injekcije ostaju fizički i kemijski stabilne 24 sata na temperaturama koje ne prelaze 30 ° C.
S mikrobiološkog gledišta, rekonstituiranu otopinu i otopinu za infuziju Herceptina treba odmah upotrijebiti. Proizvod se ne smije skladištiti nakon rekonstitucije i razrjeđivanja, osim ako je to učinjeno u kontroliranim i validiranim aseptičnim uvjetima. Ako se proizvod ne koristi odmah, vrijeme i uvjeti skladištenja u uporabi su odgovornost korisnika.
06.4 Posebne mjere pri skladištenju
Čuvati u hladnjaku (2 ° C - 8 ° C)
Za uvjete skladištenja nakon prvog otvaranja, vidjeti odjeljke 6.3 i 6.6.
06.5 Priroda neposrednog pakiranja i sadržaj pakiranja
Bočica Herceptin:
Jedna bočica od prozirnog stakla tipa I od 15 ml s zatvaračem od butilne gume presvučene fluorom sadrži 150 mg trastuzumaba.
Svako pakiranje sadrži jednu bočicu.
06.6 Upute za uporabu i rukovanje
Pridržavajte se odgovarajućih aseptičkih tehnika. Svaka bočica Herceptina rekonstituira se sa 7,2 ml sterilne vode za injekcije (nije isporučeno). Izbjegavajte uporabu drugih otapala za rekonstituciju. To daje 7,4 ml otopine s jednom dozom, koja sadrži približno 21 mg / ml trastuzumaba, s pH od približno 6,0. Višak volumena od 4% jamči aspiraciju iz bočice programiranog doza od 150 mg.
Tijekom postupka rekonstitucije Herceptinom se mora pažljivo rukovati. Prekomjerno pjenjenje uzrokovano tijekom rekonstitucije ili tresenja rekonstituirane otopine može uzrokovati probleme s količinom Herceptina koja se može izvući iz bočice.
Rekonstituirana otopina ne smije se zamrznuti.
Upute za rekonstituciju:
1) Sterilnom štrcaljkom polako ubrizgajte 7,2 ml vode za injekcije u bočicu koja sadrži liofilizirani Herceptin, usmjeravajući mlaz prema liofiliziranoj tvari.
2) Polako zavrtite bočicu kako biste olakšali rekonstituciju. NE TREŠAJTE!
Lagano pjenjenje tijekom rastvaranja nije neuobičajeno. Ostavite bočicu da stoji uspravno oko 5 minuta. Nakon rekonstitucije, Herceptin poprima izgled bistre, bezbojne do svijetložute otopine bez vidljivih čestica.
Odredite volumen potrebne otopine:
• na temelju početne doze od 4 mg trastuzumaba / kg tjelesne težine ili naknadne tjedne doze od 2 mg trastuzumaba / kg tjelesne težine:
• na temelju početne doze od 8 mg trastuzumaba / kg tjelesne težine ili naknadne doze od 6 mg trastuzumaba / kg tjelesne težine svaka 3 tjedna:
Izvucite potrebnu količinu otopine iz bočice i dodajte je u infuzijsku vrećicu koja sadrži 250 ml 0,9% -tne otopine natrijevog klorida. Nemojte koristiti otopine koje sadrže glukozu (vidjeti dio 6.2). Vrećicu treba pažljivo preokrenuti kako bi se otopina pomiješala kako se ne bi pjenilo. Nakon pripreme infuziju treba odmah primijeniti. Ako se razrijedi prema aseptičnim metodama, može se čuvati 24 sata (čuvati ispod 30 ° C).
Otopine za parenteralnu primjenu trebaju se prije primjene vizualno pregledati na čestice ili promjenu boje.
Herceptin je samo za jednokratnu upotrebu jer proizvod ne sadrži konzervanse. Neiskorišteni lijek i otpad nastao iz ovog lijeka moraju se zbrinuti u skladu s lokalnim propisima.
Nisu uočene nekompatibilnosti između vrećica Herceptin i polivinil klorida, polietilena ili polipropilena.
07.0 Nositelj odobrenja za stavljanje u promet
Roche Registration Limited
6 Sokolov put
Park Shire
Vrtni grad Welwyn
AL7 1TW
UK
08.0 BROJ DOZVOLE ZA PROMET
EU/1/00/145/001
034949014
09.0 DATUM PRVOG ODOBRENJA ILI OBNOVLJIVANJA ODOBRENJA
Datum prve autorizacije: 28. kolovoza 2000
Datum posljednje obnove: 28. kolovoza 2010. godine
10.0 DATUM REVIZIJE TEKSTA
Rujna 2015